Blood:韩为东等合作报告了三联方案治疗复发/难治性经典霍奇金淋巴瘤的最新研究结果!
时间:2024-08-08 12:01:27 热度:37.1℃ 作者:网络
DNA甲基转移酶抑制剂地西他滨联合抗PD-1 (DP)治疗复发/难治性经典霍奇金淋巴瘤(cHL)有效。然而,一部分患者在DP治疗后出现了原发性耐药性或复发/进展。
2024年8月2日,中国人民解放军总医院韩为东、Nie Jing共同通讯在Blood在线发表题为“Epigenetic agents plus anti-PD-1 reshapes tumor microenvironment and restores antitumor efficacy in Hodgkin lymphoma”的研究论文,该研究评估了一项由组蛋白去乙酰化酶抑制剂西达本胺、地西他滨和抗PD-1 camrelizumab (CDP)组成的三联方案在52例既往接受过DP治疗的复发/难治性cHL患者中的疗效和安全性。

程序性细胞死亡-1 (PD-1)阻断疗法重新激活抗肿瘤免疫,并已批准用于复发/难治性经典霍奇金淋巴瘤(cHL)患者,这些患者在自体干细胞移植(ASCT)后失败或不符合移植条件。大多数(65-87%)复发/难治性cHL患者获得临床缓解,20-30%的患者获得完全缓解(CR)和持久缓解。为了进一步提高CR率,研究人员探索了包括抗pd -1在内的各种联合方案。之前报道过DNA甲基转移酶(DNMT)抑制剂地西他滨联合抗PD-1 camrelizumab治疗复发/难治性cHL5的抗PD-1 治疗-naïve患者的CR率高达71%,中位无进展生存期(PFS)为35个月。然而,cHL患者亚群主要表现为耐药,一部分患者在抗PD-1治疗后出现获得性耐药。PD-1抑制剂在cHL中的有效作用和耐药性的潜在机制仍不清楚。
CHL是一种独特的恶性肿瘤,其特征是罕见的癌性霍奇金里德/斯滕伯格(HRS)细胞散布在丰富的免疫细胞中。HRS细胞,肿瘤的一小部分(1%),创造一个肿瘤支持和免疫抑制的环境。在HRS细胞中检测到染色体9p24.1位点的普遍遗传改变,通过PD-L1、JAK/STAT和NFκB信号过度激活,这有助于cHL患者对抗PD-1治疗的高反应性。病理上,HRS细胞主要以CD30 (TNFRSF8)的表达为特征。先前的文献报道了PD-L1+CD30+ HRS细胞与广泛浸润的PD-1 +CD4+ T细胞在一个特殊的玫瑰花状cHL生态位中接触,并在cHL微环境中发现了LAG3+CD4+ T细胞的调控亚群。然而,由于HRS细胞在cHL肿瘤中的稀缺性,探索HRS细胞在肿瘤内的异质性及其与免疫治疗后cHL逃逸的关系仍然具有挑战性。
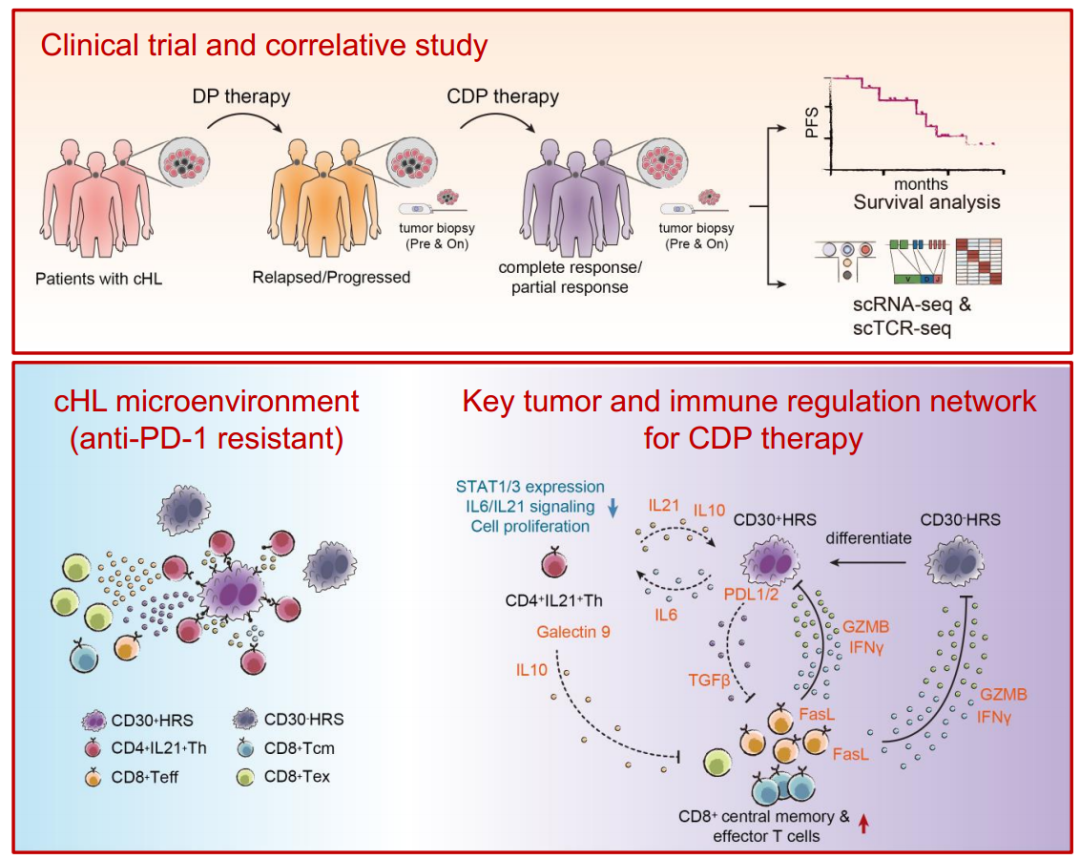
机理模式图(图源自Blood)
在这里,研究人员报道了CDP治疗的临床结果,并利用配对cHL样本的单细胞RNA测序(scRNA-seq)进一步研究了CDP治疗的抗肿瘤机制。CDP治疗耐受性良好,客观缓解率为94% (95% CI, 84-99%), 50% (95% CI, 36-64%)的患者达到完全缓解(CR)。值得注意的是,所有对既往DP治疗不耐受的患者在CDP治疗后均表现出治疗反应,尽管他们的CR率低于对既往DP治疗有反应的患者。总体而言,CDP治疗后的中位无进展生存期为29.4个月。通过治疗前和治疗后cHL肿瘤活检的单细胞RNA测序,观察到罕见的恶性Hodgkin Reed/Sternberg (HRS)样细胞的异质性。
经典的CD30+ HRS样细胞与丰富的免疫抑制IL-21+CD4+ T辅助细胞相互作用,形成一个支持其生存的正反馈循环。相比之下,CD30-HRS样细胞群对抗PD-1免疫治疗表现出潜在的耐药性。CDP治疗通过抑制STAT1/3信号通路,促进多种肿瘤反应性CD8+ T细胞的活化,抑制IL21+CD4+ T细胞的增殖,从而减轻其免疫抑制作用。这些发现有助于深入了解cHL微环境对抗PD-1耐药的影响,并强调了双重表观免疫治疗在克服免疫治疗耐药方面的治疗效果。
免责声明:iNature专注于最新的研究进展。本文仅作信息交流之目的,文中观点不代表iNature立场,亦不代表iNature支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
参考消息:
https://doi.org/10.1182/blood.2024024487


