CDD:上海交通大学朱敏敏等团队合作揭示了PRMT6/STAT1/ACSL1轴促进糖尿病肾病中的铁死亡
时间:2024-08-18 06:00:42 热度:37.1℃ 作者:网络
高血糖诱导的铁死亡是糖尿病肾病(DN)患者肾功能损害的重要因素。此外,靶向铁死亡对DN的治疗具有临床意义。然而,铁死亡的有效治疗靶点尚未确定。
2024年8月13日,上海交通大学朱敏敏、Zhang Jianhua,湖州市中心医院孟志鹏共同通讯在Cell Death & Differentiation 在线发表题为“The PRMT6/STAT1/ACSL1 axis promotes ferroptosis in diabetic nephropathy”的研究论文。该研究表明PRMT6和STAT1共同调节ACSL1的转录,诱导磷脂-多不饱和脂肪酸(PL-PUFAs)的产生,从而参与DN的铁死亡。研究发现提示PRMT6/STAT1/ACSL1轴是预防和治疗DN的一个新的治疗靶点。
研究旨在探讨蛋白精氨酸甲基转移酶6 (PRMT6)在DN中调节铁死亡的确切作用。研究使用了由野生型和PRMT6敲除(PRMT6−/−)小鼠组成的小鼠DN模型。转录组学和脂质组学分析,以及各种分子生物学方法,被用来确定PRMT6调节DN中铁死亡的潜在机制。研究结果表明,PRMT6下调通过对DN中铁死亡的调节参与肾功能障碍和肾细胞死亡。此外,PRMT6的减少通过上调酰基辅酶A合成酶长链家族成员1 (ACSL1)的表达诱导脂质过氧化,最终导致铁死亡。此外,还研究了PRMT6与信号换能器和转录激活因子1 (STAT1)相互作用共同调控ACSL1转录的分子机制。用STAT1特异性抑制剂氟达拉滨治疗可以延缓DN的进展,研究观察到PRMT6和STAT1协同调节ACSL1转录介导高血糖细胞的铁凋亡。

糖尿病肾病(DN)是糖尿病最具破坏性的并发症之一,具有多种致病因素,如上皮-间质转化、线粒体损伤和细胞凋亡。目前,肾病占需要肾脏替代治疗的个体的20-40%,每年在全世界造成95万多人死亡。因此,确定参与DN进展的新分子途径和预防或减缓肾功能障碍的潜在治疗靶点至关重要。最近的证据表明,人肾小球内皮细胞(HGECs)和肾小管细胞的损伤显著导致肾功能障碍,这是肾病患者预后的重要预测因素。此外,蛋白精氨酸甲基转移酶(PRMT)功能障碍在肾纤维化和急性肾损伤等肾脏病理过程中起着重要作用。PRMTs是一组将底物蛋白的精氨酸残基甲基化的酶。组蛋白是PRMT的重要底物,PRMT家族的成员也可以甲基化非组蛋白。PRMT6是一种I型PRMT,它不对称地将蛋白质底物二甲基化在精氨酸残基上。它在表观遗传调控中起着关键作用。PRMT6在多种组织中表达,但主要在肾脏中表达,PRMT6的失调与肾脏疾病、癌症和心脏营养不良有关,研究PRMT6参与DN的表观遗传机制至关重要。
值得注意的是,铁死亡是DN的一个显著特征,导致肾细胞损失。铁死亡是一种新型的铁依赖性程序性细胞死亡。当细胞膜上的不饱和脂肪酸被二价铁或酯氧化酶作用时,导致脂质过氧化,最终导致细胞死亡。铁死亡是由细胞氧化还原环境的不平衡引发的,这通常是抗氧化剂谷胱甘肽耗尽或谷胱甘肽过氧化物酶失活的结果。重要的是,HGECs和近端小管上皮细胞(HK-2细胞)在介导铁死亡中起关键作用。此外,DN与细胞死亡的其他触发因素相关,这些触发因素可能通过高血糖记忆使疾病进展永续,因此强调需要针对DN中铁死亡的策略。
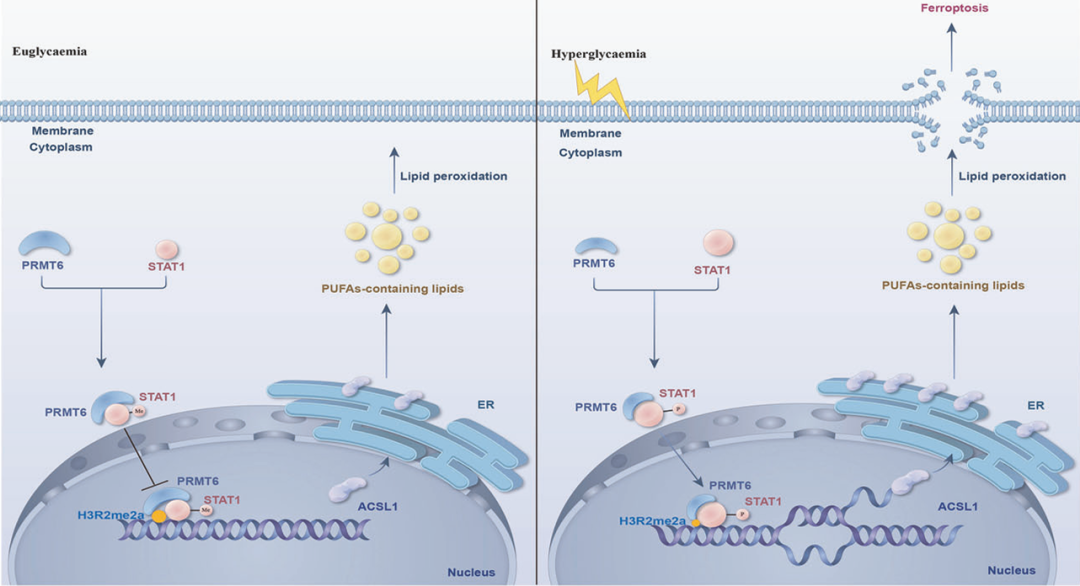
工作模型图(图源自Cell Death & Differentiation )
已经证明PRMT6通过调节铁死亡参与结核病的进展。因此,PRMT6是否通过调控铁死亡在DN中发挥作用值得进一步深入研究。近年来,磷脂-多不饱和脂肪酸(PL-PUFAs)对过氧化的敏感性及其与铁死亡的密切关系使其成为铁死亡的关键因素。已知酰基辅酶A合成酶长链(ACSL)家族调节进入合成或氧化途径的脂肪酸的命运。其中,ACSL4已被发现通过调节PL-PUFA代谢,在铁死亡的调控中起关键作用。最近,ACSL1被鉴定为一种新的铁死亡启动子。ACSL1的高表达导致脂肪酸β-氧化减少,从而导致肾脏中的脂质积累。此外,据报道,TBK1调节ACSL1的内质网(ER)易位,从而促进脂肪酸的再酯化,加速脂质过氧化。因此,ACSL1调控PL-PUFA代谢诱导DN铁死亡的具体机制值得进一步研究。
既往研究表明,糖尿病因子激活的JAK/STAT通路在调节细胞活化、增殖和分化中起着至关重要的作用。STAT1调节参与细胞增殖、氧化应激和凋亡的基因的表达。沉默STAT1已被证明可以逆转高糖引发的足细胞损伤。最近的研究表明,JAK-STAT1信号通路的激活与铁死亡有关。因此,STAT1可能通过介导铁死亡参与DN的进展。此外,STAT1的活性可以通过甲基化被甲基转移酶调节。研究PRMT6是否可以直接甲基化STAT1,调节STAT1活性参与DN也是必要的。研究发现了PRMT6/STAT1/ACSL1轴在DN中介导铁死亡的一个新的关键作用。
参考消息:
https://www.nature.com/articles/s41418-024-01357-8#Abs1


