读书报告丨急性呼吸窘迫综合征的肺超声预测模型:一项多中心前瞻性观察研究
时间:2024-08-19 20:00:43 热度:37.1℃ 作者:网络
一、摘要
理由:肺部超声(LUS)是诊断急性呼吸窘迫综合征(ARDS)的一种很有前景的工具,但缺乏经过外部验证的足够规模的研究。
目的:开发和验证用于诊断ARDS的数据驱动LUS评分,并将其性能与胸部X线摄影(CXR)进行比较。
方法:这项多中心前瞻性观察性研究纳入了有创通气ICU患者,分为推导队列和验证队列。三名评分者根据柏林标准对ARDS进行评分,分成各种亚分组。
结果:分别有324例(16%的ARDS)和129例(34%的ARDS)患者被纳入推导队列和验证队列。由专家小组诊断为ARDS参考试验中,LUS-ARDS评分,包括左、右LUS充气评分和前外侧胸膜线异常,在推导队列的某些患者和验证队列的所有患者中,受试者工作特征(ROC)曲线下面积分别为0.90(95%CI:0.85~0.95)和0.80(95%CI: 0.72~0.87)。在有影像学金标准胸部CT患者中,8名独立的CXR阅片者的诊断准确性符合LUS-ARDS评分的ROC曲线。
结论:经外部验证,LUS-ARDS评分可用于ARDS的准确诊断。在进一步验证后,LUS-ARDS评分可能是ARDS诊断的有用辅助手段。
二、介绍
急性呼吸窘迫综合征(ARDS)是由肺内原因和/或肺外原因引起的,以顽固性低氧血症为显著特征的临床综合,其死亡率约为40%。ARDS的诊断是基于柏林定义,该定义包括临床标准,要求胸部影像学上出现符合肺水肿的双侧阴影。胸部计算机断层扫描(CT)被认为是放射学评估肺水肿的金标准,但需要将危重患者转运至放射科,并且仅在少数患者中进行。胸部x线摄影(CXR)可以在ICU床旁进行,但对于CXR,两名医师对双侧阴影的一致性较差,因此导致了相互矛盾的诊断。
肺部超声(LUS)已被公认为一种可用于ICU患者诊断和监测的技术。LUS可以通过人工和解剖超声模式的半量化分数来估计光空气。虽然LUS已被广泛研究用于肺炎球菌、气泡或肺炎球菌的诊断,但ARDS诊断的证据很少。基加利修改了柏林定义,该定义依赖于双边LUS异常,旨在在获得文案、成像和其他资源有限的环境中改善ARDS诊断。
三、实验方法
接受治疗者
如果患者入住参与本研究的ICU,则纳入本研究至少24 h。排除标准如下:
-
筛选前7 d有创通气超过48 h;
-
气管切开术;
-
不适合纳入研究的临床情况(如放弃治疗或患有高度传染性疾病);
-
患者或家属反对参与研究。
研究程序
-
患者被纳入有创通气开始后48 h内。纳入日被视为第1天。纳入期间,进行LUS检查,收集患者特征、通气和气体交换参数。在纳入后24 h(第2天)重复该程序。
-
LUS检查
-
采用标准的12区域超声探头和临床可用的超声设备进行LUS。采用LUS充气评分对肺区进行评分。
-
A型:定义为胸膜线的水平重复(A线),得分为0。当两条以上间隔良好的B线覆盖胸膜线的50%以下时。B型:得分为1,当B线覆盖50%以上时,得分为2。C型:定义为实变的解剖图像或通气量完全(或接近完全)损失,大于2 cm,得分为3。伴有胸腔积液的C型评分为0,因为这更提示压迫性肺不张,而不是肺实变。所有肺部区域均根据异常胸膜线、胸膜下实变、动态空气支气管图和胸腔积液进行评分(存在时为1,不存在时为0)。
-
有四个以上缺失区域的患者被排除在分析之外。第1天的LUS检查用于分析,或者如果第1天没有检查,则使用第2天的LUS检查。
ARDS专家组分类——参考试验
来自ICU的3位在诊断和治疗ARDS方面具有丰富经验的专家独立评估了所有患者是否符合柏林ARDS标准。专家根据有创通气开始后72 h内获得的临床参数、血气分析和胸部影像学资料进行判断。根据专家之间的一致意见,将所有患者分为以下类别:①排除ARDS时为确定无ARDS;②诊断ARDS时为确定ARDS;③评分不确定时为专家之间存在冲突。共识诊断主要基于CT(如果有)或CXR图像。LUS检查被排除。
统计学
使用Mann-Whitney U检验或Fisher精确检验来检验各组之间的差异。使用R版本4.0.3和R studio接口进行数据分析。P<0.05为差异有统计学意义。
四、实验结果
研究共纳入519例患者,其中453例患者被分析(图1)。其中324例患者被纳入推导队列(阿姆斯特丹UMC), 129例患者被纳入验证队列(MUMC1)(图1)。
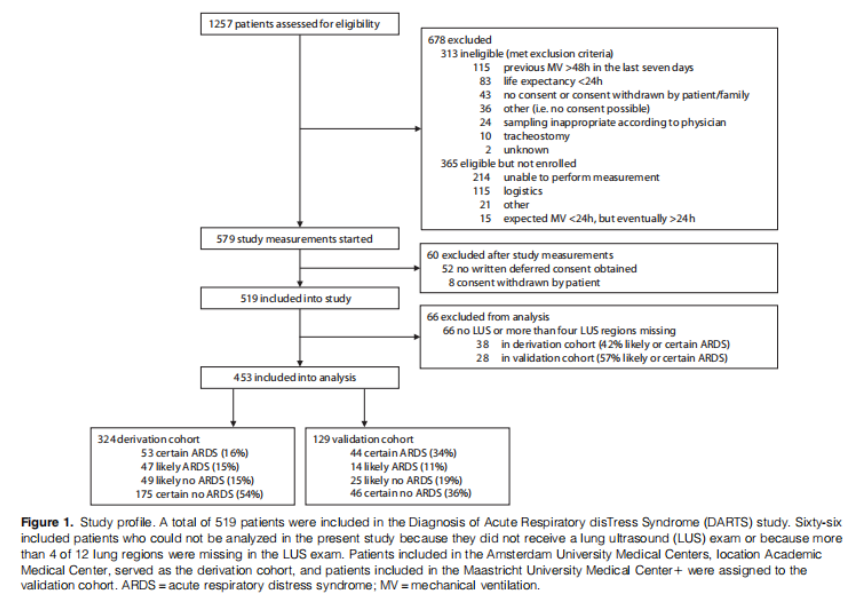
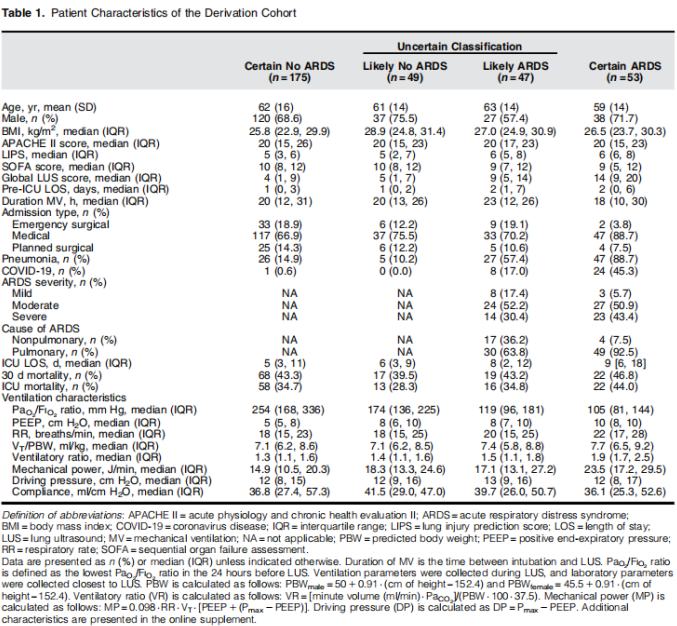
推导队列和验证队列的患者分别在有创通气开始后中位21小时(IQR:11 ~ 28)和中位23小时(IQR:17 ~ 33)接受扫描。推导队列和验证队列的患者特征和通气参数分别见表1和表2。
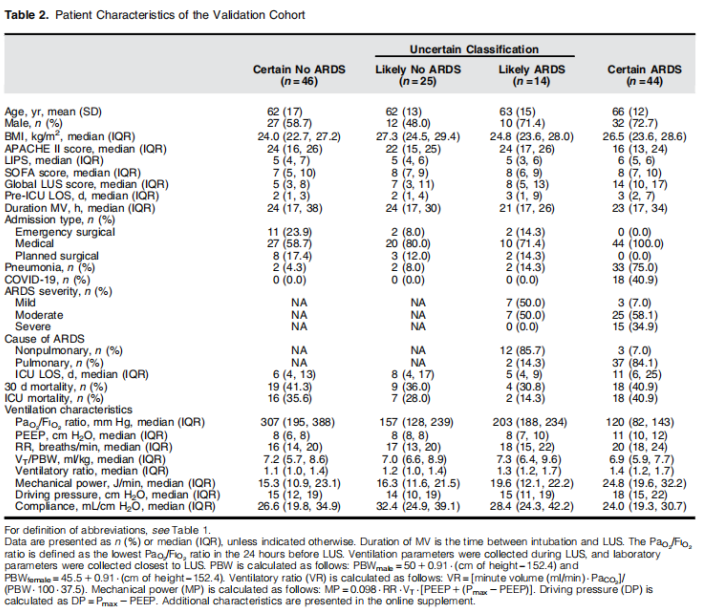
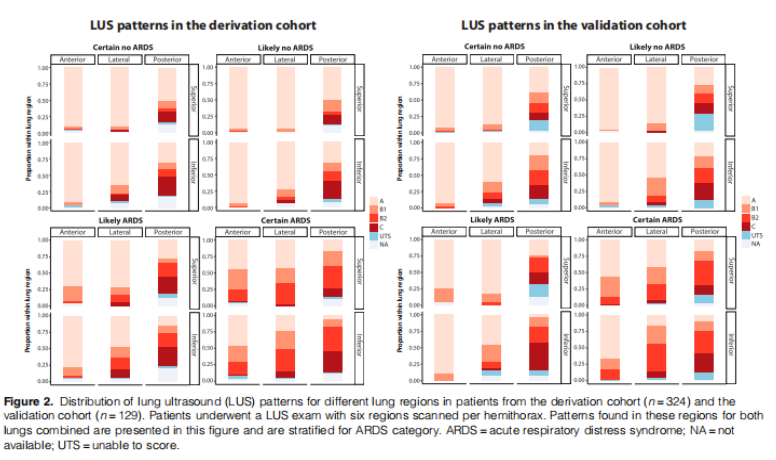
LUS模式在肺部区域的分布概述如图2所示,用于推导和验证队列。
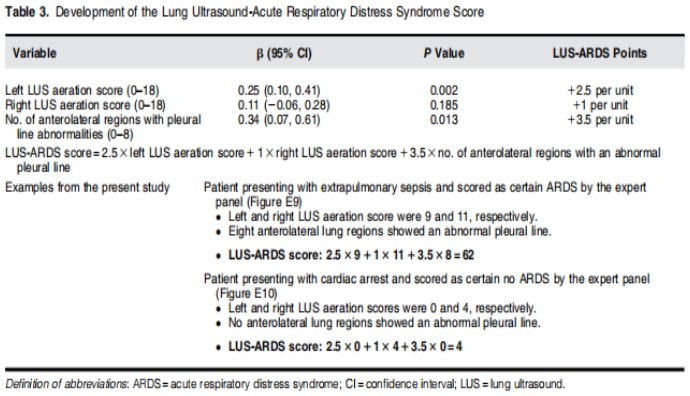
诊断ARDS的最终逻辑回归模型中包括的三个变量是左LUS通气评分(范围0~18)、右LUS通气得分(范围0~18)和胸膜线异常的前外侧肺区域数量(范围0~8)。将这些变量及其相应的逻辑回归系数转换为 LUS-ARDS评分(表3)。
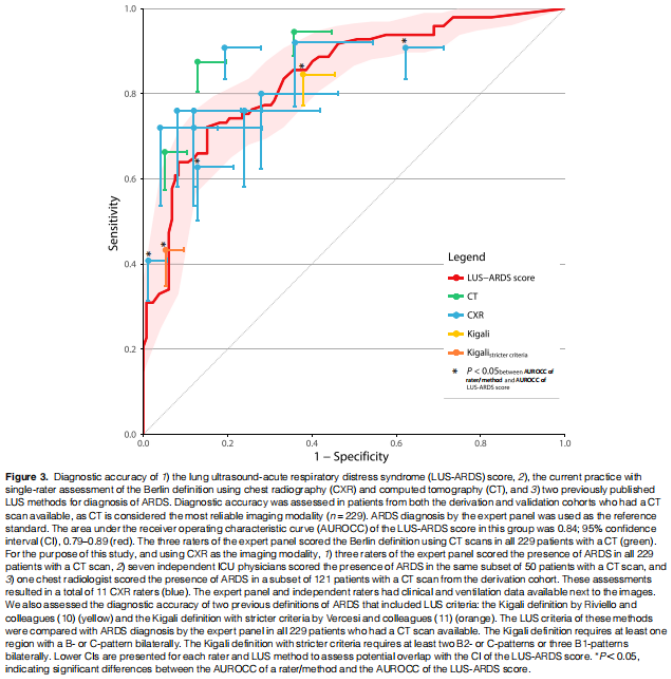
来自推导队列和验证队列的患者接受了CT扫描(n=229),被认为是金标准成像模式,LUS-ARDS评分的AUROCC为0.84(95%CI:0.79~0.89)(图3)。
在有CT扫描的验证队列患者中(n=65), auroc为0.82 (95%CI:0.72~0.93)。11名阅片者使用以CXR为影像学模式的柏林定义诊断ARDS的灵敏度和特异度符合LUS-ARDS评分的ROC曲线(图3)。
其中8名阅片者的评估未被纳入ARDS的共识诊断中,唯一一名准确度较高(尽管不显著)的阅片者由该专家参与面板,因此偏向于更高的准确性。之前提出的两种诊断ARDS的LUS方法表现出良好的性能,但在敏感性和特异性方面存在不平衡(图3)。
五、讨论
在这项多中心观察性研究中,发现LUS-ARDS评分结合了左、右LUS通气评分以及前外侧肺区胸膜线异常的评估,也经过了外部验证,为ARDS提供了良好的诊断准确性。LUS-ARDS评分在一组患者中显示出较高的诊断准确性,这些患者有胸部CT扫描,其表现与使用CXR作为成像方法的经验丰富的医生诊断的ARDS相当。对于那些由于专家的相互矛盾的评估而导致ARDS诊断不确定的患者,LUS-ARDS评分能够提供额外的信息,并通过协商一致的会议确定患有ARDS的可能性低和高的患者。
六、研究结果的应用
使用LUS-ARDS评分作为筛查和诊断工具可以改善目前临床实践中ARDS诊断不足的高数量,并增加这些患者适当治疗的使用。在很大比例的患者中,高和低LUS-ARDS评分可以分别准确诊断和排除ARDS。中间LUS-ARDS评分可以结合患者的临床和生理特征来提供ARDS概率的指导。当需要对ARDS的存在进行更明确的影像学诊断时,仍然可以进行CT扫描。
LUS还可以作为ARDS的主要诊断工具,用于CT扫描仪访问受限的环境,如低资源环境或人员或CT扫描仪过载的情况。
此外,LUS-ARDS评分显示出与经验丰富的医生对CXR的评估类似的表现,但观察者之间的诊断准确性没有变化,在每个临界点提供了客观的诊断准确性。
七、局限性
首先,没有在模型中包括所有先前发表的被认为是ARDS典型的LUS体征,因为在模型中的变量数量有限,并且其中一些LUS体征(如备用区域)没有前瞻性收集。
本研究中的分析没有针对LUS技术失败进行调整,因为指南指出,根据临床情况,调整技术失败是一种选择。10%的LUS检查中的技术失败确实反映了临床实践,并且由于LUS被认为是一种额外的成像工具,当LUS不可行时,CT和CXR仍然可以用于诊断患者的ARDS。
验证队列中接受CT扫描的患者数量有限,并且LUS-ARDS评分的诊断准确性在验证队列患者中仅略低。
在本研究中,ARDS患者中非肺部ARDS的比例较低,这与其他ARDS研究一致,但可能会限制这些患者LUS-ARDS评分的有效性。
最后,本研究中的LUS检查由3名专职超声医师进行。尽管本研究中的LUS技术被广泛使用,但当存在更多的互操作性可变性时,不能直接暗示LUS-ARDS评分在日常ICU实践中的有效性和可用性。
八、未来的发展方向
研究表明,联合使用PaO2/FiO2比值和呼气末正压水平已经进一步提高了诊断准确性。未来LUS ARDS评分可能通过数据进一步细化来自不同ARDS患病率的中心,以及通过添加其他有希望的变量。
九、结论
这项研究表明,基于左、右LUS通气评分的LUS评分以及肺前外侧区域异常胸膜线的存在可以用于准确诊断ARDS。LUS-ARDS评分的性能与有经验医师使用柏林定义和CXR诊断ARDS的性能相当,但在每个切点均具有可客观化的诊断准确性。当在其他队列中进一步验证时,LUS-ARDS评分可被视为ARDS诊断的有用辅助方法。


