【综述】| 鞘内注射治疗实体瘤脑膜转移的临床研究进展
时间:2024-09-01 06:00:55 热度:37.1℃ 作者:网络
[摘要] 脑膜转移(leptomeningeal metastasis,LM)是实体瘤患者的严重晚期并发症,常见于肺癌、乳腺癌及黑色素瘤患者中。近年来,由于诊断技术的进步,LM的诊出率逐渐上升。LM治疗的主要目标是维持患者的神经功能,改善生活质量,提高总生存率并延长无进展生存期。鞘内注射治疗是LM的主要治疗方法之一,能够直接将药物递送至蛛网膜下隙。传统的鞘内注射化疗药物包括甲氨蝶呤、阿糖胞苷及塞替哌等。随着新药研究的开展,多种化疗药物、靶向药物及免疫检查点抑制剂等也被尝试用于鞘内注射治疗。此外,不同的鞘内给药方式也给患者带来新希望。本文将对鞘内注射治疗LM的临床研究进展进行综述。
[关键词] 脑膜转移;鞘内注射;化疗;靶向治疗;免疫治疗
[Abstract] Leptomeningeal metastasis (LM) is a serious late complication in patients with solid tumors, which is common in patients with lung cancer, breast cancer and melanoma. In recent years, due to the progress of diagnosis, the diagnosis rate of LM has gradually increased. The main goal of the therapy is to maintain neurological function, improve the quality of life and the overall survival rate, and prolong the progression-free survival time of patients. Intrathecal therapy is one of the main treatments for LM, which can deliver drugs directly to the subarachnoid space. The traditional intrathecal drugs are methotrexate, cytarabine and thiotepa. With the development of new research, a variety of chemotherapeutic drugs, targeted drugs and immune checkpoint inhibitors have also been used in intrathecal therapy. In addition, different ways of intrathecal administration also bring new hope to patients. This article reviewed the clinical research progress of intrathecal therapy in the treatment of LM.
[Key words] Leptomeningeal metastasis; Intrathecal therapy; Chemotherapy; Targeted therapy; Immunotherapy
脑膜转移(leptomeningeal metastasis,LM)是实体瘤晚期并发症,患者预后极差。未经治疗的LM患者生存期仅为4~6周,而接受传统治疗的患者生存期可延长至4~6个月。LM的发生率通常因原发肿瘤类型的不同而有所差异,在实体瘤中的发生率为5%~8%,其中常见于肺癌、乳腺癌及黑色素瘤等[1-3]。大多数药物由于血-脑脊液屏障的通透性限制,在中枢神经系统中的浓度较低,无法达到预期疗效,使得肿瘤有机会在中枢神经系统中进一步生长,因此LM的治疗选择有限。鞘内注射治疗可以使药物直接到达蛛网膜下隙,从而增加脑脊液中的药物浓度。通过鞘内注射治疗能够延长LM患者的生存期,改善患者的神经系统症状。既往研究[4]表明,相较于未经治疗的LM患者,接受鞘内注射治疗的患者生存期可延长3~9个月。有研究[5]提出,当脑脊液中存在循环肿瘤细胞时,首先考虑鞘内注射治疗。欧洲神经肿瘤学协会(European Association of Neuro-Oncology,EANO)和欧洲肿瘤内科学会(European Society for Medical Oncology,ESMO)建议在没有血-脑脊液屏障功能障碍的情况下给予鞘内注射治疗[6]。此外,美国国立综合癌症网络(National Comprehensive Cancer Network,NCCN)指南推荐Karnofsky功能状态评分≥60分、无严重神经功能缺陷、全身肿瘤负荷小、可耐受系统治疗的LM患者接受鞘内注射治疗[7]。然而,由于前瞻性的临床研究数据较少,大多数据来自回顾性研究,因此目前仍缺乏治疗LM的标准鞘内注射治疗方案。
1 给药途径
鞘内注射是通过腰椎穿刺方式注射抗肿瘤药物,使药物绕过血-脑屏障直接到达蛛网膜下隙的一种治疗方法。由于鞘内注射药物只能在室管膜下扩散1~5 mm,因此鞘内注射治疗结节性LM的效果并不理想[8-9]。即使是在脑脊液回流通畅的情况下,也存在药物误入硬膜外间隙的风险。此外,重复腰椎穿刺不仅会增加术后并发症的风险,如出血、感染和腰椎穿刺后头痛,而且要求患者在每次操作后保持仰卧位4~6 h,会加重患者的治疗负担。
Ommaya囊是一种脑室引流装置,通过微创手术植入相连接的侧脑室引流管和皮下储液器。其优势在于保证药物进入脑室而非硬膜外或硬膜下,并且侵袭性更小,可增加患者的舒适度,操作便捷,能够提高患者的依从性和安全性。在脑脊液流动通畅的情况下,脑室内给药可使药物在蛛网膜下隙均匀分布。有研究[10]通过回顾分析比较腰椎穿刺及Ommaya囊两种给药方式,发现使用Ommaya囊组的患者生存期显著长于腰椎穿刺组(9.2个月 vs 4.0个月)。但在其他研究[5,11]中未能观察到Ommaya囊的生存优势,目前还没有证据表明脑室给药比腰椎穿刺途径更有利于生存。
脑脊液流动障碍是LM脑室内治疗的主要挑战。生理性脑脊液流动的缺乏及脑室和腰椎蛛网膜下隙之间的扩散距离过长,导致侧脑室注射药物的浓度梯度和转运时间延长。这种现象增加了药物向脑实质渗透的机会并导致脑病的发生。为了提高脑室内治疗药物在腰椎蛛网膜下隙的输送,有研究[12]尝试通过脑室-腰椎灌注(ventriculolumbar perfusion,VLP)的方式进行鞘内治疗,VLP能够将药物输送到常规方法无法到达的区域,潜在地增加了药物在脑脊液中的分布,并使药物在脑脊液中均匀分布,结果表明, VLP在缓解下肢感觉运动障碍和尿失禁方面比标准的经Ommaya囊治疗更有效。关于VLP的Ⅰ期研究[13]采用甲氨蝶呤(methotrexate,MTX)和人工脑脊液混合物持续输注(MTX剂量为 24 mg/d,灌注量为20 mL/h)的给药模式,发现与灌注相关的不良反应较轻,且不会引起剂量相关毒性。随后的Ⅱ期试验[14]结果显示,VLP能显著提高颅内压控制率(76%),改善患者临床症状,延长LM患者的生存期,但VLP化疗的不良反应发生率明显高于标准鞘内化疗。
2 药物选择
传统的鞘内注射药物主要为MTX、阿糖胞苷及塞替哌等。近年来,随着新的药物不断涌现,化疗药物如培美曲塞等被开发用于鞘内注射治疗。此外,靶向药物、细胞因子及免疫检查点抑制剂(immune checkpoint inhibitors,ICI)等也被尝试用于鞘内注射治疗。
2.1 传统鞘内注射化疗药物
MTX是一种叶酸类抗肿瘤药物,通过对二氢叶酸还原酶的抑制而达到抗肿瘤作用。MTX属于细胞周期特异性药物,主要作用于细胞周期的S期。MTX脑脊液半衰期为4.5~8.0 h。MTX鞘内治疗分为诱导、巩固和维持3个阶段,具体为诱导期4周(每周2次)、巩固期4周(每周1次)和维持期(每月1次)3个阶段,直至疾病进展,每次剂量为10~15 mg[15]。一项关于108例肺癌LM患者的回顾性研究[16]表明,经MTX鞘内注射化疗后,患者临床症状减轻且生活质量有所改善。此外,一项前瞻性研究[3]通过鞘内注射不同剂量(10、15 mg)的MTX观察LM患者的临床缓解率,发现适当增加MTX的剂量可以有效地缓解LM患者的临床症状。另一项随机对照试验[17]表明,联合应用MTX及阿糖胞苷鞘内注射治疗LM患者的有效率并不优于单药MTX,但对于不同类型的LM的缓解率有所不同。对于乳腺癌LM患者单药MTX组的缓解率(67%)显著高于联合组(25%),相反,对于肺癌LM则联合用药组的缓解率(86%)显著高于MTX组(50%)。鞘内注射MTX的主要临床不良反应为骨髓抑制、胃肠道反应及脑白质病变等[3]。值得注意的是,有临床研究[18]发现,同时给予鞘内注射化疗和全脑放疗可能增加神经系统的不良反应发生率,即放疗后鞘内注射MTX可能会增加发生脑白质病变的风险。因此,建议在全脑放疗前2~3周给予MTX鞘内注射化疗。
阿糖胞苷是一种嘧啶类核苷类似物,主要作用于细胞周期S期,可以通过抑制细胞DNA聚合及合成,干扰肿瘤细胞增殖。通常鞘内注射阿糖胞苷剂量为25~100 mg,诱导期每周注射2次,持续4周,巩固期每周注射1次,持续4周,维持阶段每月注射1次,直至疾病进展[15]。阿糖胞苷脂质体是阿糖胞苷的一种缓释制剂,能够在脑脊液中维持游离有效浓度至少10~14 d,因此只需要每2周注射1次[19]。一项鞘内注射阿糖胞苷脂质体治疗乳腺癌LM的回顾性研究[20]发现,接受鞘内注射阿糖胞苷脂质体的患者的生存期与MTX相似,但显著改善了患者的无进展生存率和生活质量。另一项关于鞘内注射阿糖胞苷联合全身治疗的临床试验[21]中,联合治疗组的中位生存期比全身化疗延长了3.3个月(7.3个月 vs 4.0个月),并且改善了LM相关的无进展生存期(3.8个月 vs 2.2个月)。多项临床研究[21-22]表明,阿糖胞苷的不良反应主要表现为化学性脑膜炎等。
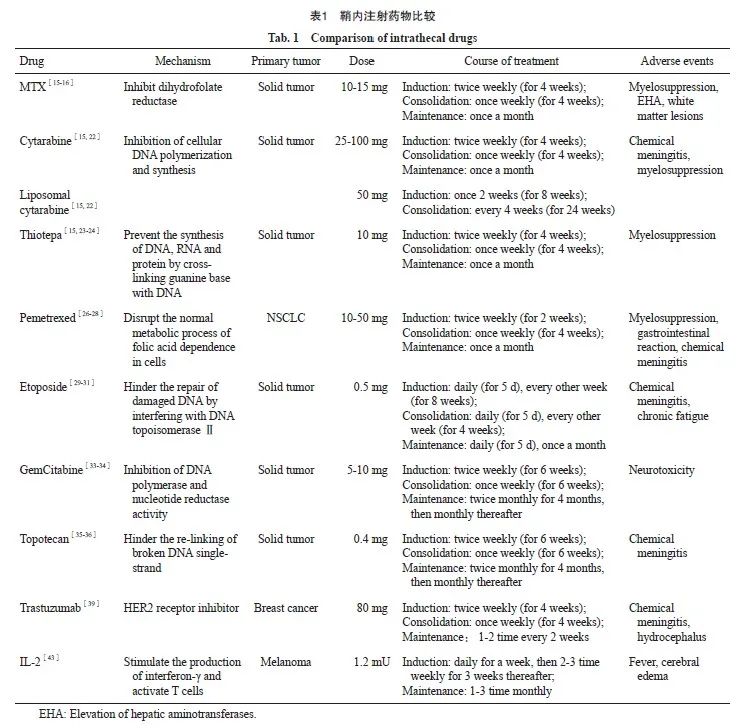
塞替哌是一种烷化剂,为细胞周期非特异性药物,主要通过鸟嘌呤碱基与DNA双联交联使DNA出现不可修复性损伤,从而阻止DNA、RNA及蛋白质的合成。通常鞘内注射塞替哌的剂量为10 mg,诱导方案为每周2次注射,持续4周,巩固方案为每周1次,持续4周,维持方案为每月1次,直到疾病进展[15]。关于鞘内注射塞替哌治疗LM的相关研究很少,通常作为LM一线治疗失败后的挽救性治疗方案。Rhun等[23]将塞替哌作为乳腺癌LM的二线治疗方案,安全性良好。Cho等[24]的回顾性研究发现,以鞘内注射MTX为基础的治疗失败后,挽救性鞘内注射塞替哌能够提高LM患者的临床缓解率且治疗相关不良反应较轻,主要表现为骨髓抑制(表1)。
2.2 鞘内注射化疗新药物
培美曲塞是一种抗叶酸类制剂,主要通过破坏细胞内叶酸依赖的正常代谢过程,抑制肿瘤细胞的复制及生长。培美曲塞作为非小细胞肺癌(non-small cell lung cancer,NSCLC)的一线治疗药物,细胞毒性较轻。动物实验[25]表明,1 mg/kg培美曲塞可安全地应用于大鼠的蛛网膜下隙,并建议鞘内注射培美曲塞在人体临床试验中的最佳起始量为5~10 mg。Fan等[26]首次评估培美曲塞用于NSCLC LM患者的疗效和安全性,Ⅰ/Ⅱ期临床试验提示临床有效率为84.6%,显著高于传统鞘内注射治疗(53.0% ~ 79.0%),并且生存期达9个月。这可能是由于培美曲塞能够抑制胸苷合成酶、二氢叶酸还原酶和甘氨酰胺核苷酸甲酰转移酶,较MTX等具有更广泛的抗肿瘤作用。此外,回顾性研究[27-28]表明,培美曲塞的不良反应主要表现为骨髓抑制、胃肠道反应及化学性脑膜炎。目前,关于培美曲塞治疗LM的临床试验(NCT05305885、NCT05289908、NCT03507244、NCT03101579)仍在不断开展中,其中有两项研究(NCT05305885、NCT03507244)正在探索培美曲塞联合放疗对LM患者预后的影响。
依托泊苷是一种DNA拓扑异构酶Ⅱ抑制剂,主要作用于细胞周期S期或G2期,通过干扰DNA拓扑异构酶Ⅱ,致使受损的DNA不能修复。Fleischhack等[29]的研究证明脑室内注射依托泊苷的耐受性良好,脑脊液药物峰值水平超过静脉输液的100倍以上。一项Ⅱ期临床试验[30]通过给予27例LM患者脑室内注射依托泊苷,进行8周诱导治疗后,26%的患者治疗有效且6个月神经系统无进展生存率为11%。这为鞘内注射依托泊苷作为挽救性鞘内化疗的可行性提供了初步证据。Park[31]报道了1例NSCLC LM患者在一线MTX鞘内注射治疗失败后使用依托泊苷鞘内注射治疗,发现该患者的磁共振成像(magnetic resonance imaging,MRI)检查结果、临床症状及脑脊液细胞学检查结果均有所改善。鞘内注射依托泊苷的不良反应表现为一过性的脑膜炎和慢性疲劳,而血液学毒性则相对少见[30]。
吉西他滨是一种胞嘧啶核苷衍生物,能够抑制DNA聚合酶和核苷酸还原酶的活性,被广泛用于治疗各种恶性肿瘤。动物实验的药代动力学研究[32]证明鞘内注射5 mg吉西他滨在脑脊液中的药物浓度是标准静脉化疗剂量下血浆浓度的200倍。Chen等[33]报道了1例NSCLC LM患者经脑室内注射吉西他滨治疗后未出现不良反应。Bernardi等[34]在一项临床研究中对不同恶性肿瘤来源的LM进行鞘内注射吉西他滨,发现吉西他滨在人体脑脊液中的药代动力学与动物实验不同。虽然该试验的起始剂量为动物实验的1/10,但是患者出现了剂量限制性神经毒性,阻碍了鞘内注射吉西他滨的进一步研究。
拓扑替康是一种抑制DNA拓扑异构酶Ⅰ的药物,通过阻碍断裂DNA单链的重新链接而发挥抗肿瘤活性。一项非随机单臂Ⅱ期临床试验[35]中,有62例LM患者接受了鞘内注射拓扑替康治疗,结果发现13例患者的脑脊液中肿瘤细胞消失,患者生存期为15周,然而有32%的患者出现了化学性脑膜炎。Salgia等[36]报道了1例人表皮生长因子受体2(human epidermal growth factor receptor 2,HER2)阴性的乳腺癌LM患者接受鞘内注射拓扑替康后,观察到脑脊液细胞学检查结果有所改善,但患者最后仍出现疾病进展(表1)。
2.3 鞘内注射靶向治疗药物
曲妥珠单抗是一种针对HER2的人源化单抗,主要用于治疗HER2阳性的转移性乳腺癌患者。由于曲妥珠单抗的相对分子质量大,在血-脑屏障的通透性差,因此接受曲妥珠单抗治疗的乳腺癌患者脑转移及LM的发生率增加[37]。虽然,LM患者血-脑屏障破坏有助于曲妥珠单抗进入脑脊液,但脑脊液中的药物浓度仍难以达到治疗所需水平。一项Ⅰ期临床试验[38]表明,在无剂量限制毒性的条件下,脑脊液中曲妥珠单抗的最大剂量水平为150 mg。另一项Ⅰ/Ⅱ期临床试验[39]显示,LM患者对每周2次鞘内注射曲妥珠单抗80 mg作为初始治疗的耐受性良好,且接受该治疗的HER2阳性乳腺癌患者的中位生存期为10.5个月,其疾病缓解率为17.9%。Zagouri等[40]对文献进行回顾性分析发现,鞘内注射曲妥珠单抗后患者的生存期达13.5个月,中枢神经系统无进展生存期为7.5个月。此外,在疾病进展后进行鞘内注射曲妥珠单抗治疗的LM患者中,有75%的患者疾病缓解。Figura等[41]通过比较鞘内注射曲妥珠单抗、化疗药物和全脑放疗的6和12个月的无进展生存率,结果显示,曲妥珠单抗组的无进展生存率显著升高,说明鞘内注射曲妥珠单抗治疗具有改善乳腺癌LM患者生存预后的潜力(表1)。
2.4 鞘内注射免疫治疗药物
白细胞介素-2(interleukin-2,IL-2)是一种细胞因子,通过刺激干扰素-γ的产生并激活细胞毒性T淋巴细胞来增强自然杀伤细胞的活性,从而诱导抗肿瘤活性。鞘内注射IL-2主要用于黑色素瘤LM患者[15]。静脉注射重组IL -2不足以产生维持体内淋巴因子激活的杀伤细胞(lymphokine-activated killer cell,LAK)。但鞘内注射LAK能抑制LM的发展。早期研究[42]未能发现LM患者从鞘内注射IL-2或IL-2联合LAK治疗中获益。后来,Glitza等[43]通过纳入43例接受鞘内注射IL-2的黑色素瘤LM患者,发现其中位生存期为7.8个月,1、2和5年生存率分别为36%、26%和13%,LM患者出现的主要不良反应为发热、寒战及颅内高压。然而,目前没有相关的前瞻性研究表明鞘内注射IL-2对LM有显著益处。
ICI主要通过阻断细胞毒性T淋巴细胞相关抗原4(cytotoxic T lymphocyte associated antigen-4,CTLA-4)、程序性死亡蛋白-1(programmed death-1,PD-1)及程序性死亡蛋白配体-1(programmed death ligand-1,PD-L1)来增强T淋巴细胞的抗肿瘤活性。ICI的相对分子质量大,难以渗透血-脑屏障,但有研究[44]认为ICI激活的T淋巴细胞能够透过血-脑屏障及血-脑脊液屏障。一项Ⅰ期临床试验[45]表明,对黑色素瘤LM患者分别给予鞘内注射5、20和50 mg纳武利尤单抗治疗后未观察到剂量限制性毒性,且中位总生存期为4.9个月,值得注意的是,有LM患者在接受首次鞘内注射ICI后生存期达143周。目前,关于鞘内注射ICI治疗LM的临床试验(NCT05112549、NCT055988)仍在进行中。NCT05112549是一项关于鞘内注射纳武单抗治疗LM的单臂Ⅰ期临床试验,主要探讨鞘内注射ICI的最大耐受剂量和安全性,并以总生存期为次要研究终点。NCT055988尝试鞘内注射双ICI,观测患者对鞘内注射PD-1抗体联合CTLA-4抗体的耐受性(表1)。
3 总结与展望
作为极具挑战性的癌症并发症之一,LM的诊疗困难,主要是基于现有专家共识。鞘内注射在LM的治疗上具有一定优势,然而,目前关于鞘内注射治疗的研究大多数是回顾性的,而前瞻性研究相对缺乏。因此,目前尚缺乏最佳的鞘内注射治疗方案。为进一步改善LM患者的生存预后,越来越多的研究尝试使用不同的化疗药物、靶向药物及ICI等进行鞘内注射。此外,药物递送技术的改进也为LM患者的诊疗带来了新希望。因此,深入研究LM发生、发展的生物学机制,尝试寻找新的生物标志物,进一步发现药物及其抵抗机制是十分必要的。
利益冲突声明:所有作者均声明不存在利益冲突
作者贡献声明:
黄思捷:参与文章选题,资料分析与解释,文章撰写及修改;
康勋:参与文章修改,对文章的知识性内容作审阅;
李文斌:指导文章选题,获取研究经费,对文章的知识性内容作审阅。
[参考文献]
[1]GANI C, MÜLLER A C, ECKERT F, et al. Outcome after whole brain radiotherapy alone in intracranial leptomeningeal carcinomatosis from solid tumors[J]. Al, 2012, 188(2): 148-153.
[2]RHUN E L, WELLER M, BRANDSMA D, et al. EANO-ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up of patients with leptomeningeal metastasis from solid tumours[J]. Ann Oncol, 2017, 28(suppl_4): iv84-iv99.
[3]HOU L, HAN W X, JIN J, et al. Clinical efficacy and safety of different doses of intrathecal methotrexate in the treatment of leptomeningeal carcinomatosis: a prospective and single-arm study[J]. Jpn J Clin Oncol, 2021, 51(12): 1715-1722.
[4]HERRLINGER U, FÖRSCHLER H, KÜKER W, et al. Leptomeningeal metastasis: survival and prognostic factors in 155 patients[J]. J Neurol Sci, 2004, 223(2): 167-178.
[5]MONTES DE OCA DELGADO M, CACHO DÍAZ B, SANTOS ZAMBRANO J, et al. The comparative treatment of intraventricular chemotherapy by ommaya reservoir vs. lumbar puncture in patients with leptomeningeal carcinomatosis[J]. Front Oncol, 2018, 8: 509.
[6]RHUN E L, WELLER M, VAN DEN BENT M, et al. Leptomeningeal metastasis from solid tumours: EANO-ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up[J]. ESMO Open, 2023, 8(5): 101624.
[7]HORBINSKI C, NABORS L B, PORTNOW J, et al. NCCN guidelines® insights: central nervous system cancers, version 2.2022[J]. J Natl Compr Canc Netw, 2023, 21(1): 12-20.
[8]NAYAK L, FLEISHER M, GONZALEZ-ESPINOZA R, et al. Rare cell capture technology for the diagnosis of leptomeningeal metastasis in solid tumors[J]. Neurology, 2013, 80(17): 1598-1605.
[9]SUBIRÁ D, SIMÓ M, ILLÁN J, et al. Diagnostic and prognostic significance of flow cytometry immunophenotyping in patients with leptomeningeal carcinomatosis[J]. Clin Exp Metastasis, 2015, 32(4): 383-391.
[10]PALMISCIANO P, WATANABE G, CONCHING A, et al. Intrathecal therapy for the management of leptomeningeal metastatic disease: a scoping review of the current literature and ongoing clinical trials[J]. J Neurooncol, 2022, 160(1): 79-100.
[11]LI H Y, ZHENG S N, LIN Y J, et al. Safety, pharmacokinetic and clinical activity of intrathecal chemotherapy with pemetrexed via the ommaya reservoir for leptomeningeal metastases from lung adenocarcinoma: a prospective phase Ⅰ study[J]. Clin Lung Cancer, 2023, 24(2): e94-e104.
[12]NAKAGAWA H, FUJITA T, KUBO S, et al. Ventriculolumbar perfusion chemotherapy with methotrexate and cytosine Arabinoside for meningeal carcinomatosis: a pilot study in 13 patients[J]. Surg Neurol, 1996, 45(3): 256-264.
[13]GWAK H S, LIM H S, SHIN S H, et al. Ventriculolumbar perfusion chemotherapy for the treatment of leptomeningeal carcinomatosis: a phase Ⅰ study with pharmacokinetic data[J]. Am J Clin Oncol, 2013, 36(5): 491-499.
[14]GWAK H S, JOO J, SHIN S H, et al. Ventriculolumbar perfusion chemotherapy with methotrexate for treating leptomeningeal carcinomatosis: a phase Ⅱ study[J]. Oncologist, 2014, 19(10): 1044-1045.
[15]BEAUCHESNE P. Intrathecal chemotherapy for treatment of leptomeningeal dissemination of metastatic tumours[J]. Lancet Oncol, 2010, 11(9): 871-879.
[16]吴 熙, 李峻岭, 肖建平, 等. 甲氨蝶呤鞘内注射化疗对肺癌脑膜转移的疗效分析[J]. 癌症进展, 2019, 17(8): 914-917.
WU X, LI J L, XIAO J P, et al. Analysis of the efficacy of intrathecal methotrexate for leptomeningeal metastases from lung cancer[J]. Oncol Prog, 2019, 17(8): 914-917.
[17]HITCHINS R N, BELL D R, WOODS R L, et al. A prospective randomized trial of single-agent versus combination chemotherapy in meningeal carcinomatosis[J]. J Clin Oncol, 1987, 5(10): 1655-1662.
[18]WANG N, BERTALAN M S, BRASTIANOS P K. Leptomeningeal metastasis from systemic cancer: review and update on management[J]. Cancer, 2018, 124(1): 21-35.
[19]FOWLER M J, COTTER J D, KNIGHT B E, et al. Intrathecal drug delivery in the era of nanomedicine[J]. Adv Drug Deliv Rev, 2020, 165/166: 77-95.
[20]RHUN E L, TAILLIBERT S, ZAIRI F, et al. A retrospective case series of 103 consecutive patients with leptomeningeal metastasis and breast cancer[J]. J Neurooncol, 2013, 113(1): 83-92.
[21]RHUN E L, WALLET J, MAILLIEZ A, et al. Intrathecal liposomal cytarabine plus systemic therapy versus systemic chemotherapy alone for newly diagnosed leptomeningeal metastasis from breast cancer[J]. Neuro Oncol, 2020, 22(4): 524-538.
[22]GAVIANI P, CORSINI E, SALMAGGI A, et al. Liposomal cytarabine in neoplastic meningitis from primary brain tumors: a single institutional experience[J]. Neurol Sci, 2013, 34(12):
2151-2157.
[23] RHUN E L, TAILLIBERT S, DEVOS P, et al. Salvage intracerebrospinal fluid thiotepa in breast cancer-related leptomeningeal metastases: a retrospective case series[J]. Anticancer Drugs, 2013, 24(10): 1093-1097.
[24] CHO K M, KIM Y J, KIM S H, et al. Salvage treatment with intracerebrospinal fluid thiotepa in patients with leptomeningeal metastasis after failure of methotrexate-based treatment[J]. Anticancer Res, 2015, 35(10): 5631-5638.
[25] SUN J M, NAM M H, CHUNG J Y, et al. Safety and pharmacokinetics of intrathecal administration of pemetrexed in rats[J]. Cancer Chemother Pharmacol, 2011, 68(2): 531-538.
[26] FAN C J, ZHAO Q Y, LI L, et al. Efficacy and safety of intrathecal pemetrexed combined with dexamethasone for treating tyrosine kinase inhibitor-failed leptomeningeal metastases from EGFR-mutant NSCLC-a prospective, openlabel, single-arm phase 1/2 clinical trial (unique identifier: ChiCTR1800016615)[J]. J Thorac Oncol, 2021, 16(8): 1359-1368.
[27] GENG D, GUO Q Q, HUANG S Y, et al. A retrospective study of intrathecal pemetrexed combined with systemic therapy for leptomeningeal metastasis of lung cancer[J]. Technol Cancer Res Treat, 2022, 21: 15330338221078429.
[28] 谢雨文, 徐 婷, 程弯弯, 等. 经Ommaya囊侧脑室注射培美曲塞治疗非小细胞肺癌伴软脑膜转移的疗效及其影响因素
[J]. 中华肿瘤防治杂志, 2023, 30(17): 1034-1039.
XIE Y W, XU T, CHENG W W, et al. Efficacy and influencing factors on intrathecal chemotherapy with pemetrexed via the Ommaya reservoir for leptomeningeal carcinomatosis from nonsmall cell lung cancer[J]. Chin J Cancer Prev Treat, 2023, 30(17): 1034-1039.
[29] FLEISCHHACK G, REIF S, HASAN C, et al. Feasibility of intraventricular administration of etoposide in patients with metastatic brain tumours[J]. Br J Cancer, 2001, 84(11): 1453-1459.
[30] CHAMBERLAIN M C, TSAO-WEI D D, GROSHEN S. Phase Ⅱ trial of intracerebrospinal fluid etoposide in the treatment of neoplastic meningitis[J]. Cancer, 2006, 106(9): 2021-2027.
[31] PARK M J. Prolonged response of meningeal carcinomatosis from non-small cell lung cancer to salvage intrathecal etoposide subsequent to failure of first-line methotrexate: a case report and literature review[J]. Am J Case Rep, 2015, 16: 224-227.
[32] EGORIN M J, ZUHOWSKI E G, MCCULLY C M, et al. Pharmacokinetics of intrathecal gemcitabine in nonhuman primates[J]. Clin Cancer Res, 2002, 8(7): 2437-2442.
[33] CHEN Y M, CHEN M C, TSAI C M, et al. Intrathecal gemcitabine chemotherapy for non-small cell lung cancer patients with meningeal carcinomatosis: a case report[J]. Lung Cancer, 2003, 40(1): 99-101.
[34] BERNARDI R J, BOMGAARS L, FOX E, et al. Phase Ⅰ clinical trial of intrathecal gemcitabine in patients with neoplastic meningitis[J]. Cancer Chemother Pharmacol, 2008, 62(2): 355-361.
[35] GROVES M D, GLANTZ M J, CHAMBERLAIN M C, et al. A multicenter phase Ⅱ trial of intrathecal topotecan in patients with meningeal malignancies[J]. Neuro Oncol, 2008, 10(2): 208-215.
[36] SALGIA S, FLEMING G F, LUKAS R V. Leptomeningeal carcinomatosis from breast cancer treated with intrathecal topotecan with concomitant intravenous eribulin[J]. J Clin Neurosci, 2014, 21(7): 1250-1251.
[37] STEMMLER H J, SCHMITT M, WILLEMS A, et al. Ratio of trastuzumab levels in serum and cerebrospinal fluid is altered in HER2-positive breast cancer patients with brain metastases and impairment of blood-brain barrier[J]. Anticancer Drugs, 2007, 18(1): 23-28.
[38] BONNEAU C, PAINTAUD G, TRÉDAN O, et al. Phase I feasibility study for intrathecal administration of trastuzumab in patients with HER2 positive breast carcinomatous meningitis[J]. Eur J Cancer, 2018, 95: 75-84.
[39] KUMTHEKAR P U, AVRAM M J, LASSMAN A B, et al. A phase Ⅰ/Ⅱ study of intrathecal trastuzumab in human epidermal growth factor receptor 2-positive (HER2-positive) cancer with leptomeningeal metastases: safety, efficacy, and cerebrospinal fluid pharmacokinetics[J]. Neuro Oncol, 2023, 25(3): 557-565.
[40] ZAGOURI F, SERGENTANIS T N, BARTSCH R, et al. Intrathecal administration of trastuzumab for the treatment of meningeal carcinomatosis in HER2-positive metastatic breast cancer: a systematic review and pooled analysis[J]. Breast Cancer Res Treat, 2013, 139(1): 13-22.
[41] FIGURA N B, RIZK V T, MOHAMMADI H, et al. Clinical outcomes of breast leptomeningeal disease treated with intrathecal trastuzumab, intrathecal chemotherapy, or whole brain radiation therapy[J]. Breast Cancer Res Treat, 2019, 175(3): 781-788.
[42] GLITZA I C, SMALLEY K S M, BRASTIANOS P K, et al. Leptomeningeal disease in melanoma patients: an update to treatment, challenges, and future directions[J]. Pigment Cell Melanoma Res, 2020, 33(4): 527-541.
[43] GLITZA I C, ROHLFS M, GUHA-THAKURTA N, et al. Retrospective review of metastatic melanoma patients with leptomeningeal disease treated with intrathecal interleukin-2[J]. ESMO Open, 2018, 3(1): e000283.
[44] FIGURA N B, RIZK V T, ARMAGHANI A J, et al. Breast leptomeningeal disease: a review of current practices and updates on management[J]. Breast Cancer Res Treat, 2019, 177(2): 277-294.
[45] GLITZA OLIVA I C, FERGUSON S D, BASSETT R JR, et al. Concurrent intrathecal and intravenous nivolumab in leptomeningeal disease: phase 1 trial interim results[J]. Nat Med, 2023, 29(4): 898-905.


