【衡道丨病例】乳头腺瘤(Nipple adenoma)如何诊断?
时间:2024-09-13 06:01:00 热度:37.1℃ 作者:网络
患者病史
患者女性,39岁,因左侧乳头溢液1年余来我院就诊,查体见乳头周围皮肤散在黑色斑点,乳头皮肤呈湿疹样改变,乳头见血性溢液。
影像检查
B超:左乳头明显凹陷伴强化,乳头后方病灶大小约0.8×1.0cm,拟BI-RADS 4A类。
术中所见
左乳头后方一圆形肿物约2cm,直接与乳头相连,开口于乳头,予以完整切除。
大体形态
术中冰冻送检“左乳头后方肿块”:乳腺组织一块,大小2.0×1.5×1.4cm,切面灰白淡黄相间,未见明显占位。
冰冻切片镜下形态
镜下可见一境界清楚的肿物,一部分区域细胞呈乳头状增生,另一部分区域呈实性不规则巢状分布,间质可见较多增生的纤维;
肿瘤细胞分布比较均匀,胞界不清,核深染,核大小比较一致,核仁不明显。
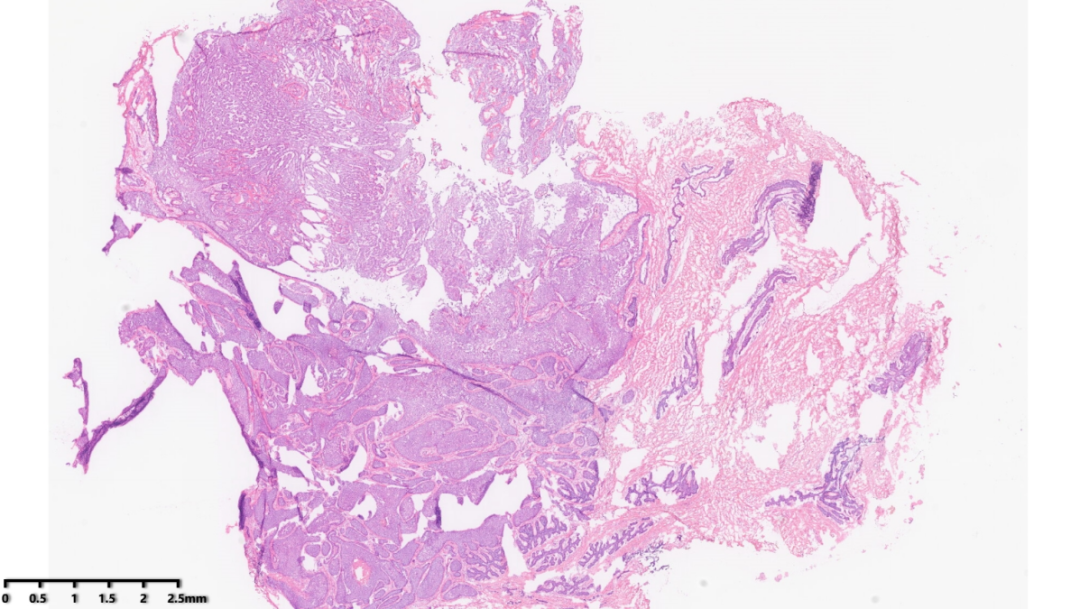
肿物与周围组织界限清楚
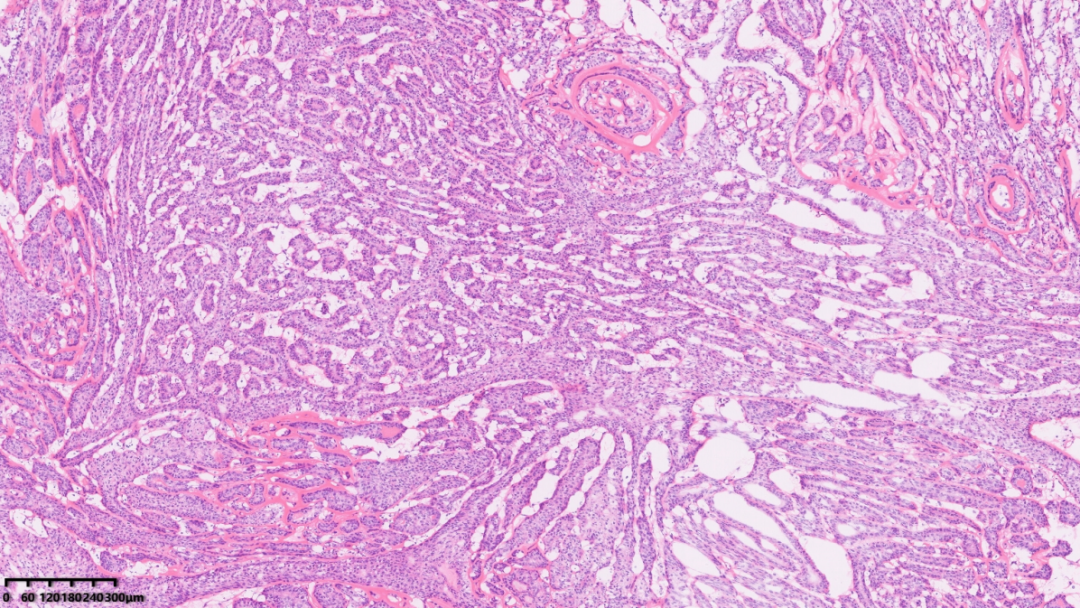
部分肿瘤呈乳头状增生
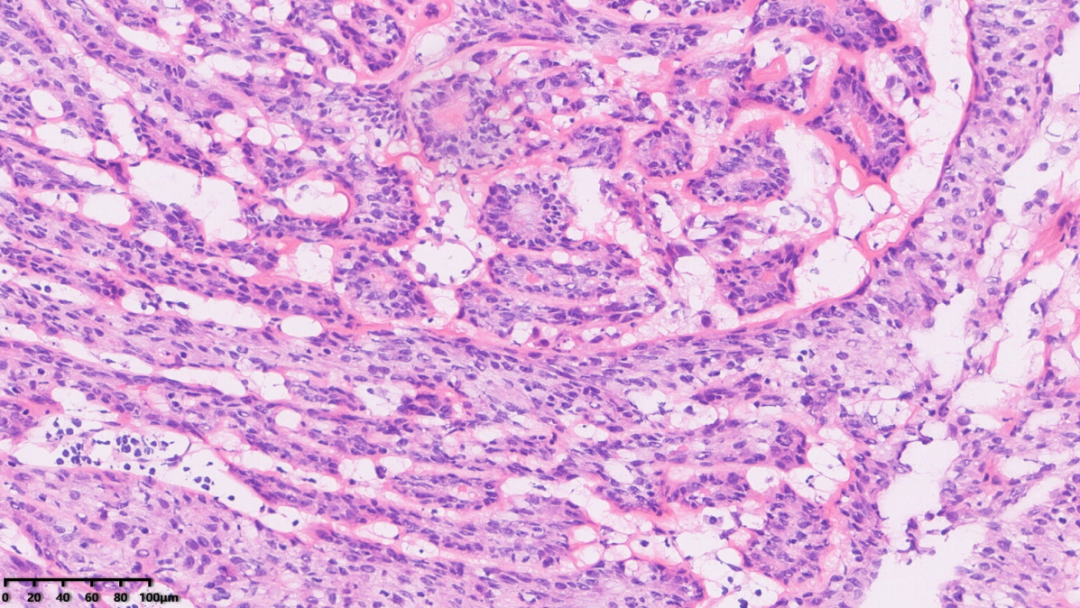
可见纤维脉管轴心
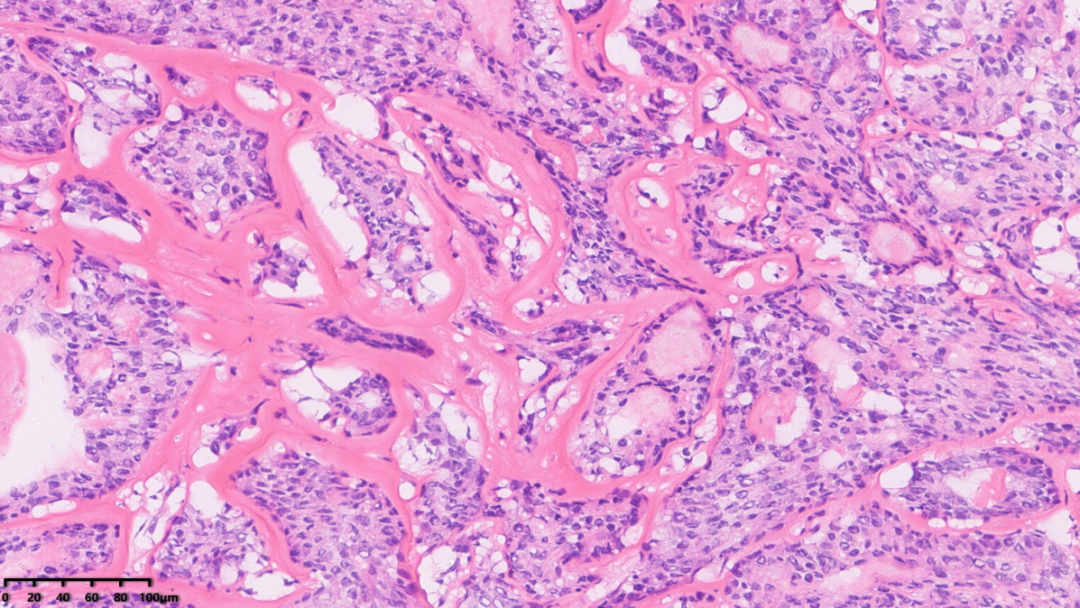
纤维间质分隔肿瘤,使其表现为“浸润性生长”
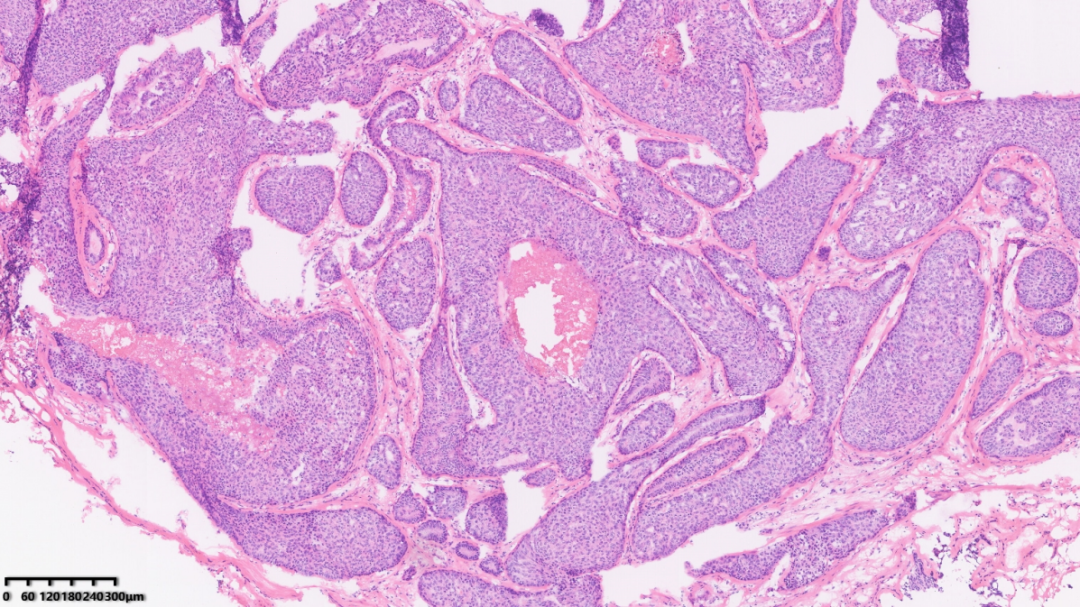
部分肿瘤呈不规则巢状排列
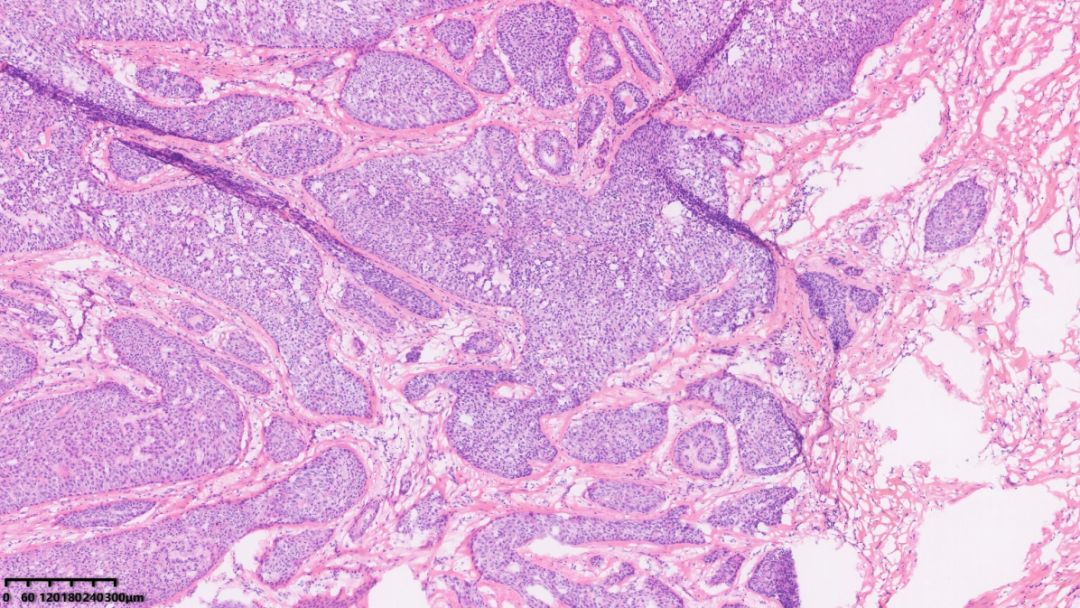
肿瘤巢团分布在纤维间质背景当中
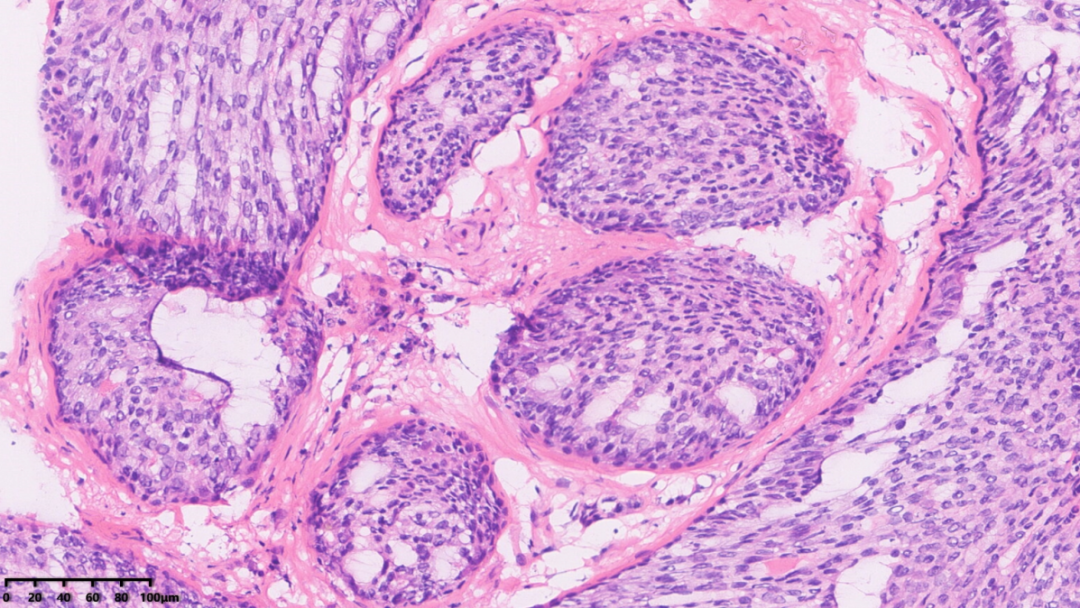
肿瘤巢团内可见不规则裂隙结构
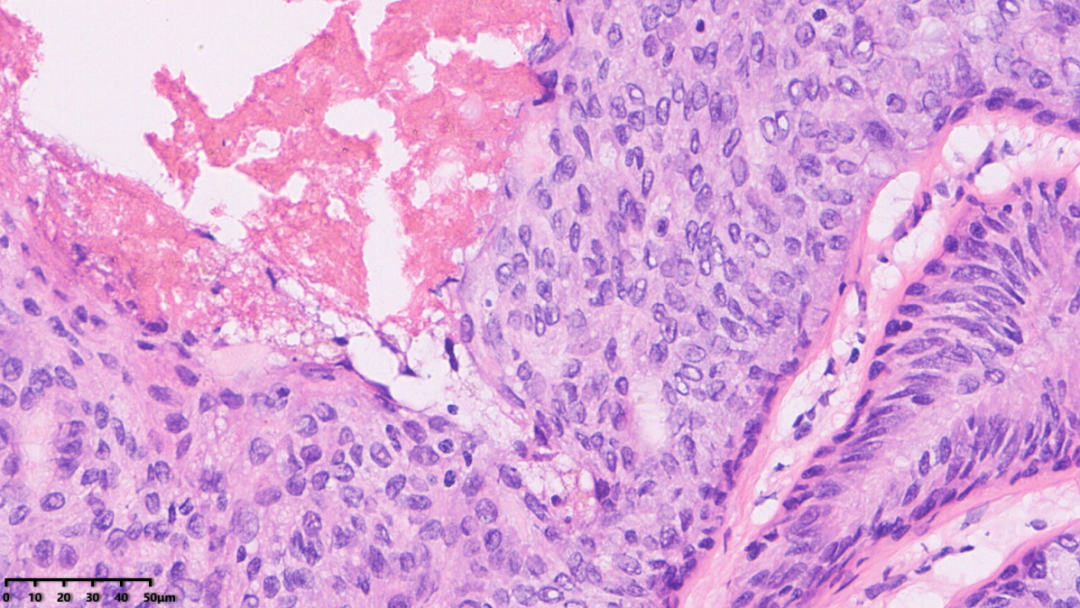
肿瘤细胞分布比较均匀,胞界不清,核大小比较一致,核仁不明显
冰冻诊断
“左乳头后方肿块”:导管内乳头状肿瘤,导管上皮增生较旺盛伴不典型增生,倾向为乳头状瘤,待石蜡及免疫组化检测进一步诊断。
石蜡切片镜下形态
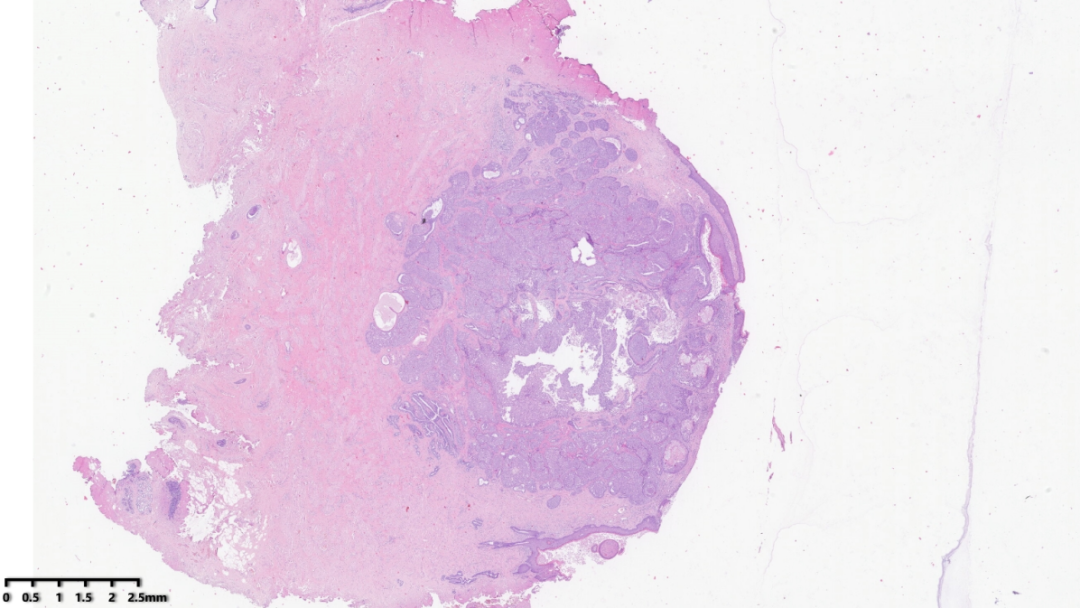
乳头下一境界清楚的肿物,与乳头相连,累及表面皮肤
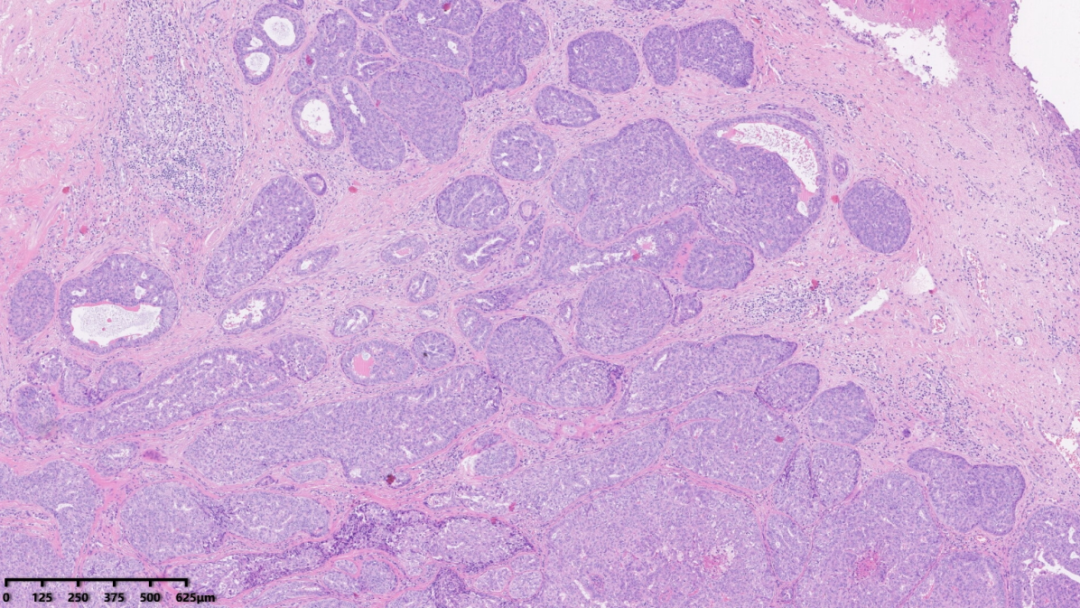
肿瘤呈巢团分布,背景中可见纤维间质增生伴淋巴细胞浸润
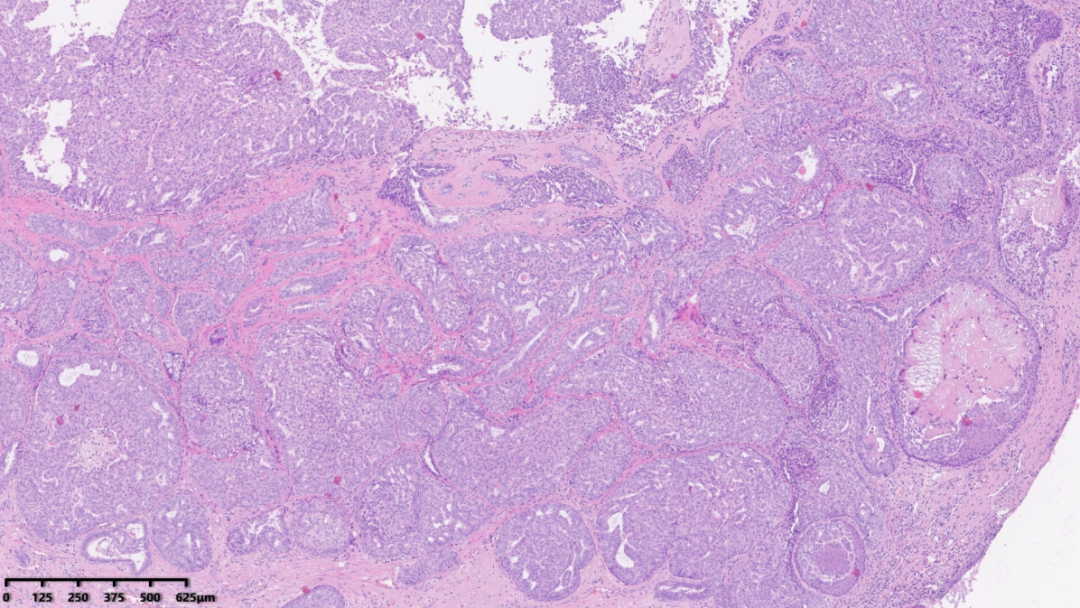
肿瘤巢团中可见较多的不规则裂隙结构
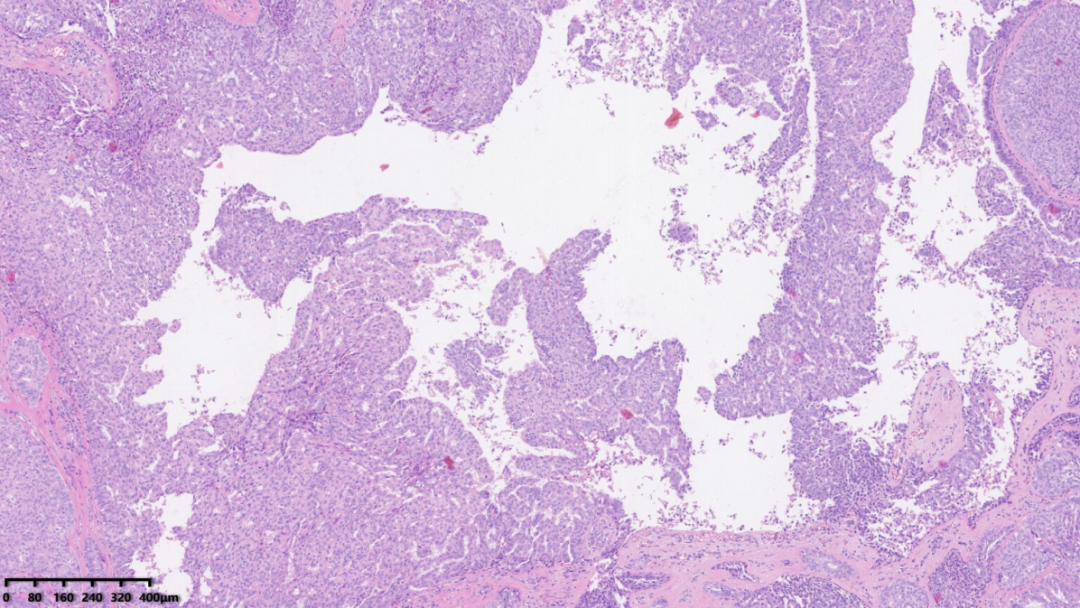
部分肿瘤呈乳头状增生
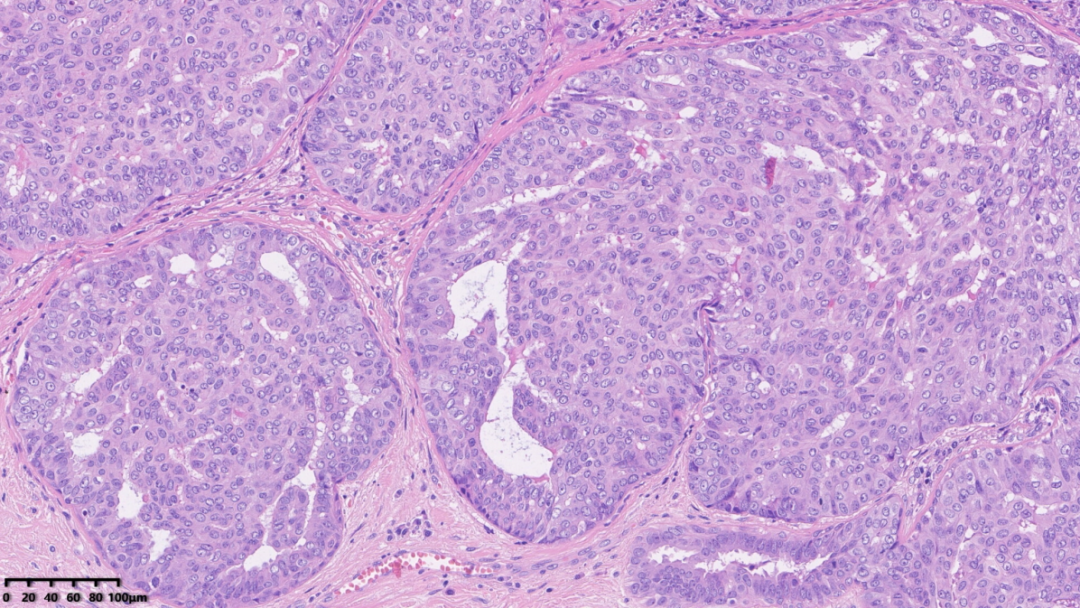
中倍镜下,可见肿瘤巢团中出现较多不规则开窗;另可见纤维脉管轴心
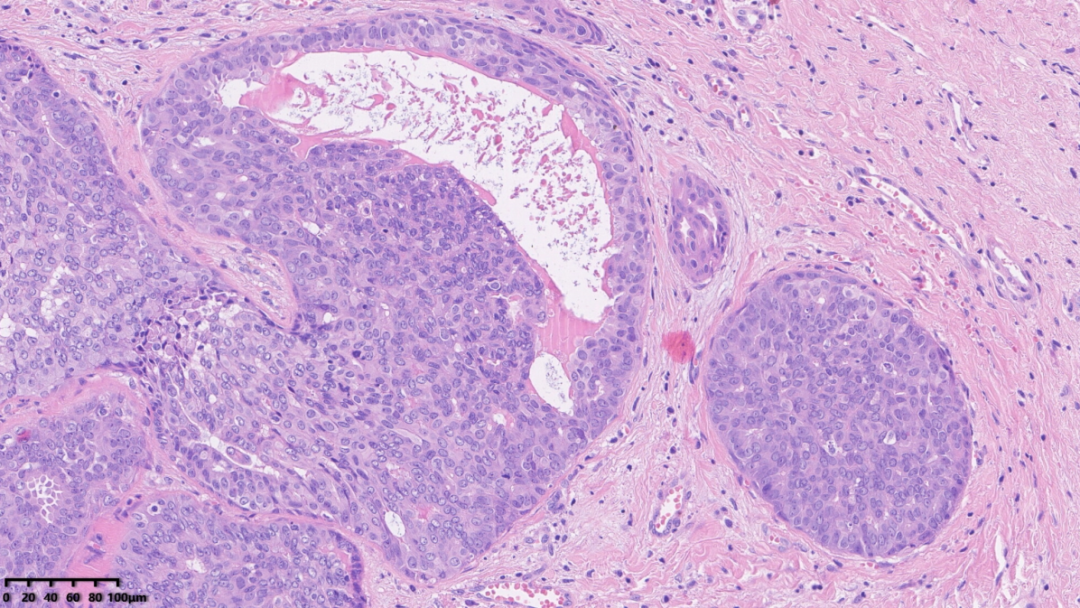
局部区域可见巢状结构似有融合
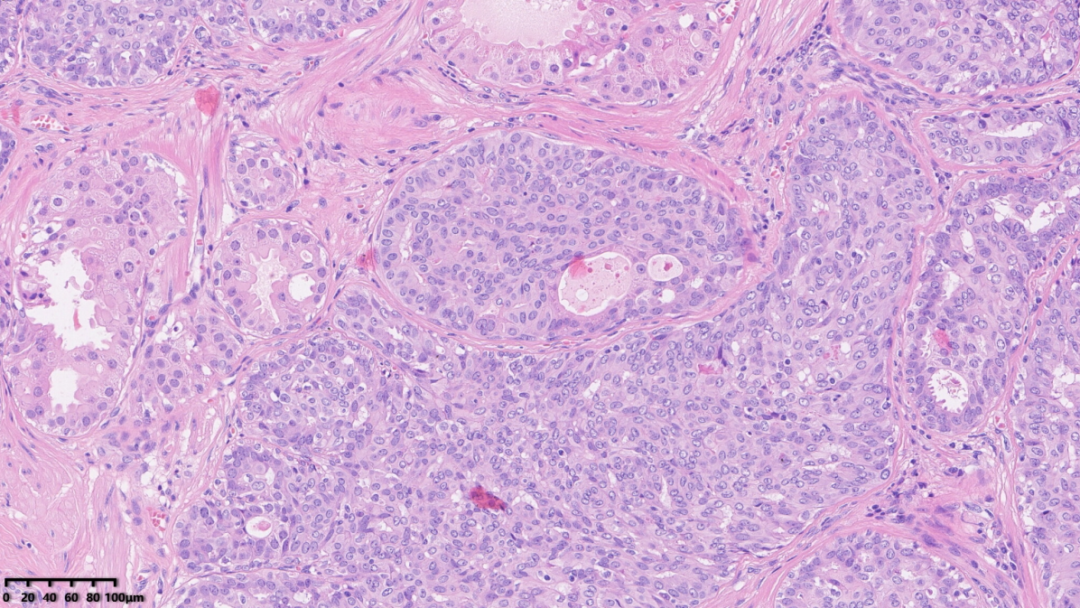
局部可见导管上皮大汗腺化生
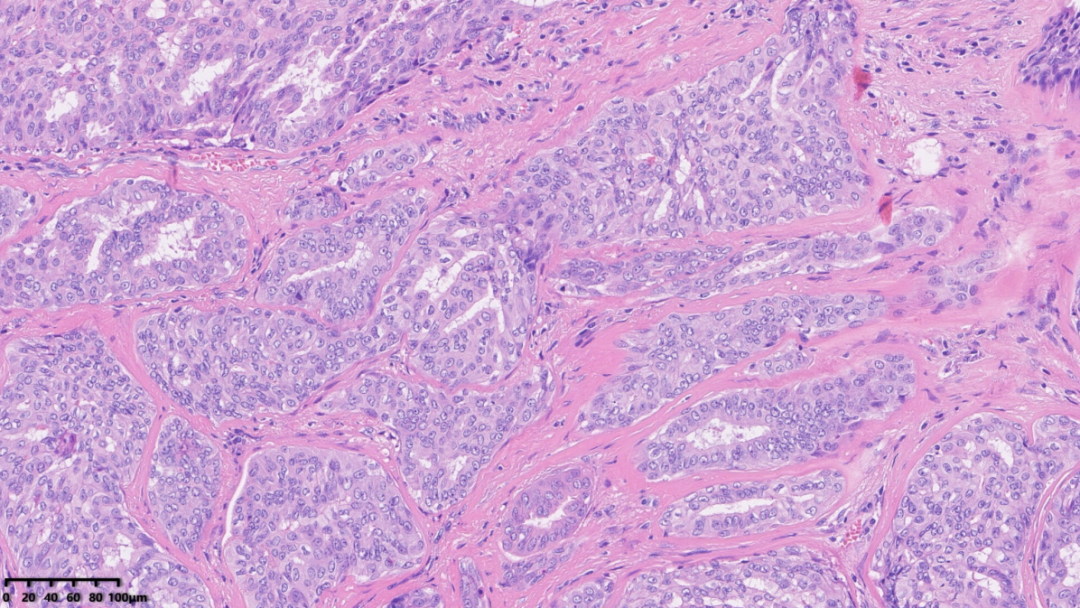
局部区域肿瘤呈假浸润性生长

可见腔内出现组织细胞以及少量坏死
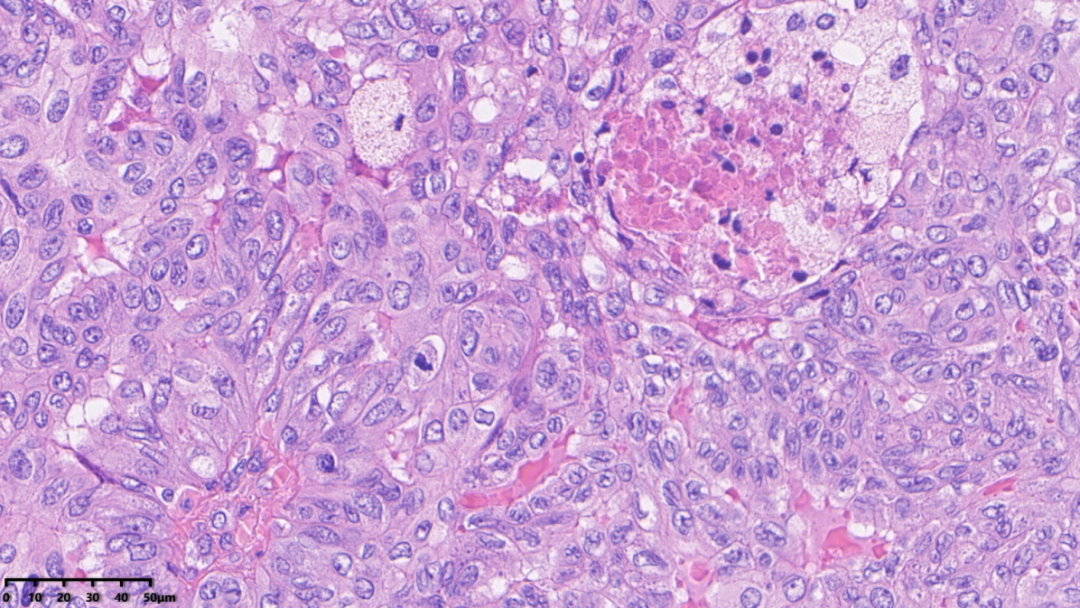
肿瘤细胞胞浆较丰富,细胞界限不清,部分区域排列较拥挤
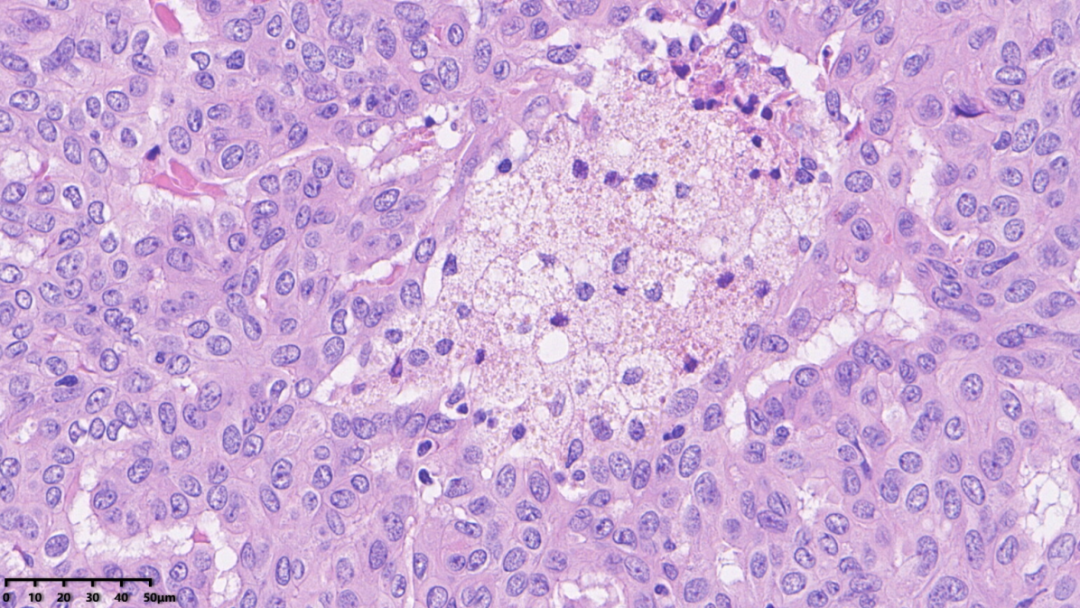
细胞核大小较一致,核仁不明显,未查见核分裂象
免疫组化
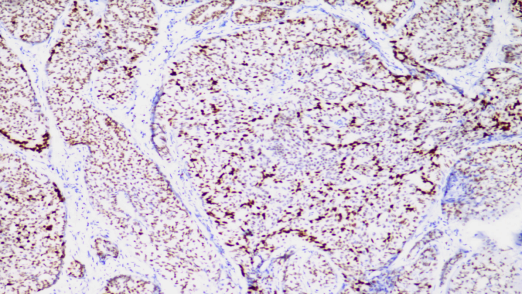
GATA-3,肿瘤细胞核阳性
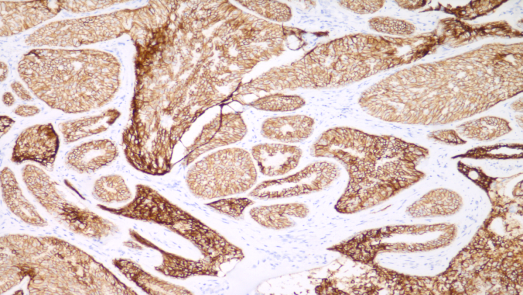
E-Cadherin,肿瘤细胞膜阳性
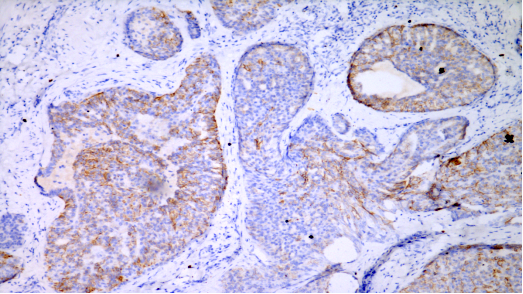
P120,部分阳性
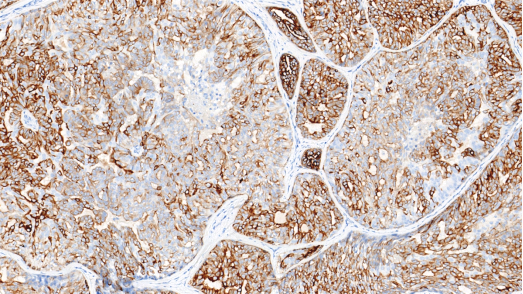
CK5/6,肿瘤细胞斑驳阳性
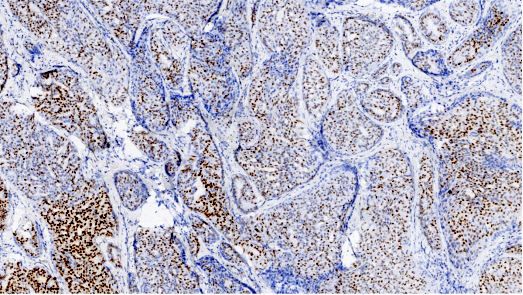
ER,部分肿瘤细胞阳性
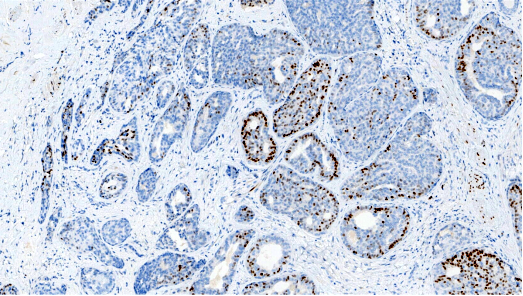
PR,部分肿瘤细胞阳性
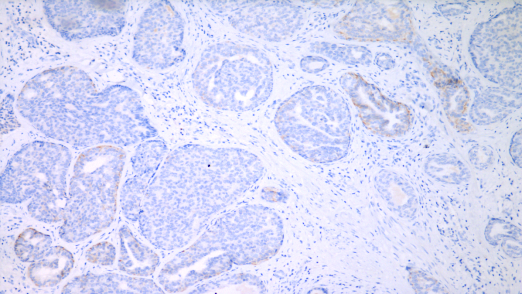
HER-2,1+
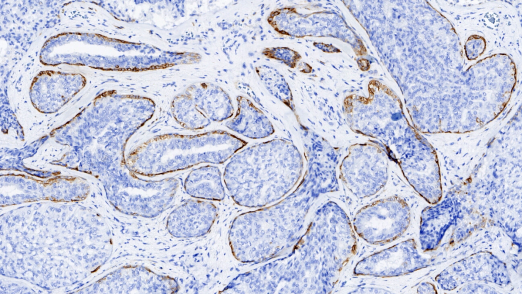
Calponin,肌上皮阳性
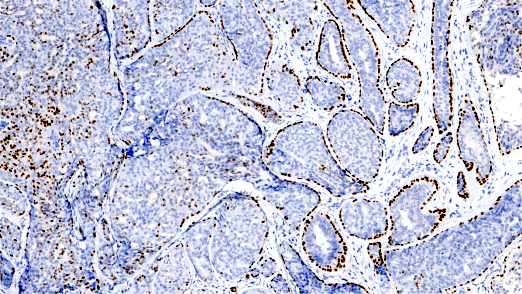
P63,肌上皮阳性
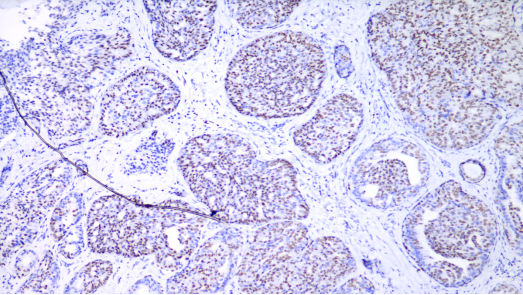
SOX-10,肿瘤细胞阳性
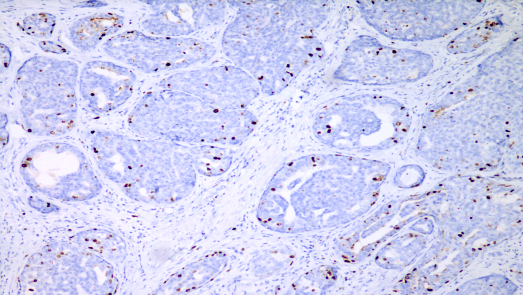
Ki-67,约5%
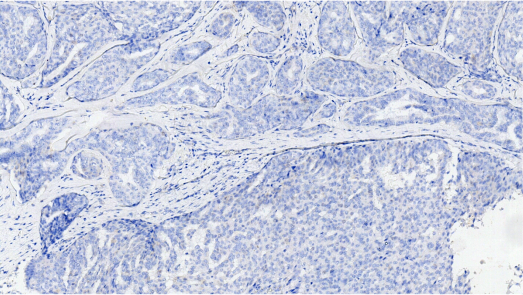
SYN,肿瘤细胞阴性
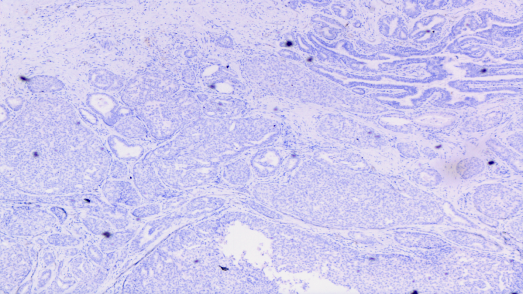
CgA,肿瘤细胞阴性
免疫组化结果汇总:
阳性标记:
ER(部分+),PR(部分+),HER2(1+),Ki67(约5%+),GATA-3(+),E-Cadherin(+),P120(胞膜+),CK5/6(斑驳+) ,SOX-10(部分+) ,P63(肌上皮+),Calponin (肌上皮+)
阴性标记:
CgA(-),SYN(-)
最终诊断
“左乳头后方肿块”:结合肿瘤发生部位及免疫表型,符合乳头腺瘤,导管上皮增生较旺盛。
乳头部疾病概述
乳头是乳房顶端、乳晕中央的小突起,输乳管由此开口于皮肤。乳头位于乳晕的中央,周边有一圈薄层、有色素的皮肤,这些结构一般总体称为乳头-乳晕复合体(nopple-areola complex,NAC)。乳头-乳晕复合体处富于皮脂腺,无毛囊。乳头-乳晕复合体处的复层鳞状上皮延伸至乳头大导管的终末部分、达1-4mm。乳头表皮内可见散在形态温和的腺细胞,即Toker细胞,皮下由一层平滑肌构成,无皮下组织。
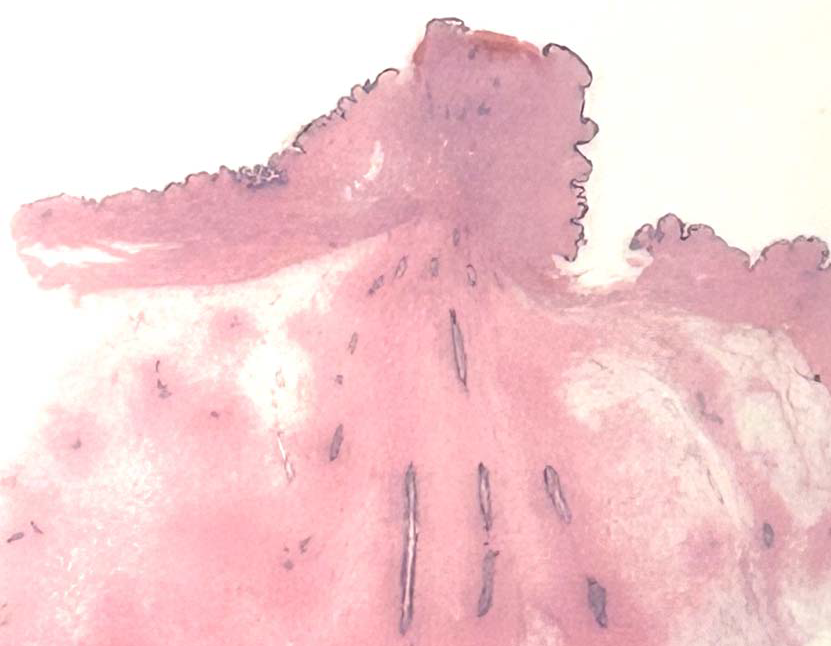
乳头-乳晕复合体镜下形态
绝大多数的乳头疾病是非肿瘤性的,也可以发生良性和恶性肿瘤。第5版乳腺肿瘤WHO分类当中,乳头上皮性肿瘤包括汗管瘤样肿瘤、乳头腺瘤以及乳腺Paget病。
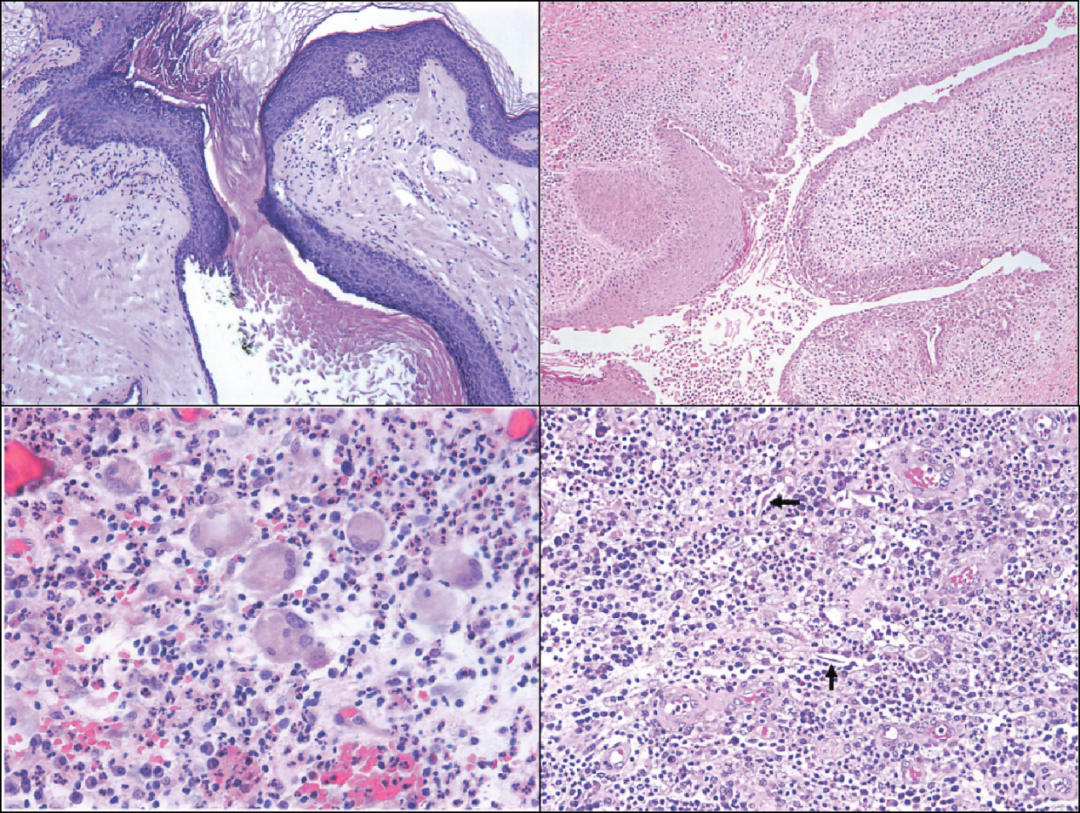
输乳管鳞状上皮化生,管腔内见角蛋白剥脱物(左上图所示),周围间质可见异物巨细胞、淋巴细胞、中性粒细胞浸润(右上及左下图所示),混杂角蛋白碎屑(右下图箭头所指)
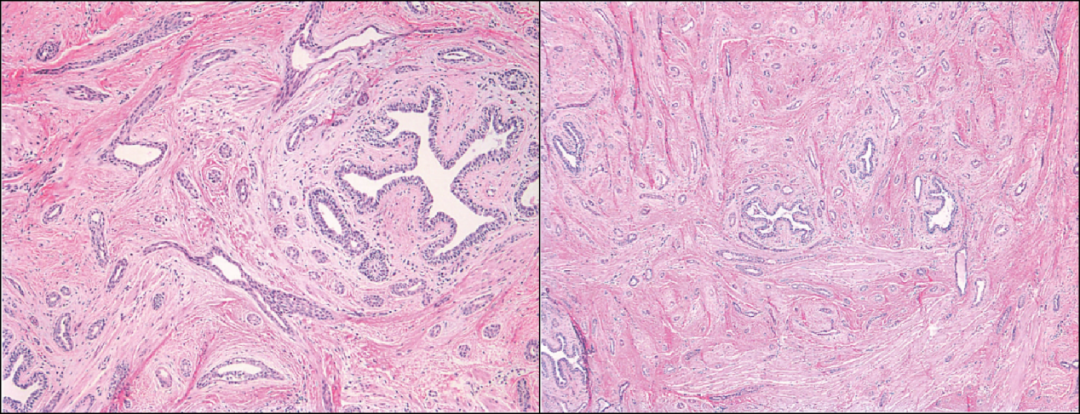
汗管瘤样肿瘤,增生小腺体呈浸润性生长,腺体常成角呈泪滴状或延伸的逗点状;无促纤维结缔组织反应;细胞核未见非典型,常无核分裂象
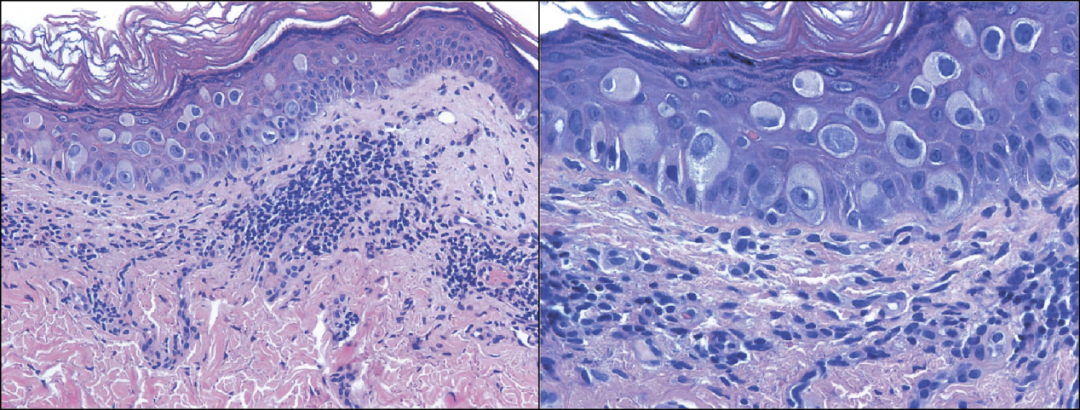
乳头Paget病,以腺上皮出现于乳头为特征,可扩展至乳晕及周围皮肤(左图);表皮单个或成簇分布的Paget细胞,细胞胞浆丰富,核大,核仁明显,可有黑色素(右图)
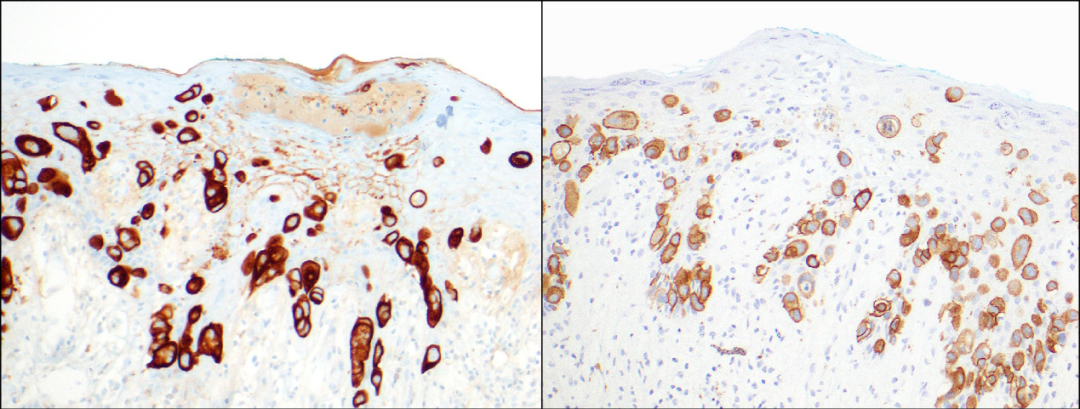
乳头Paget病,肿瘤细胞CK7(左图)、HER-2(右图)染色阳性
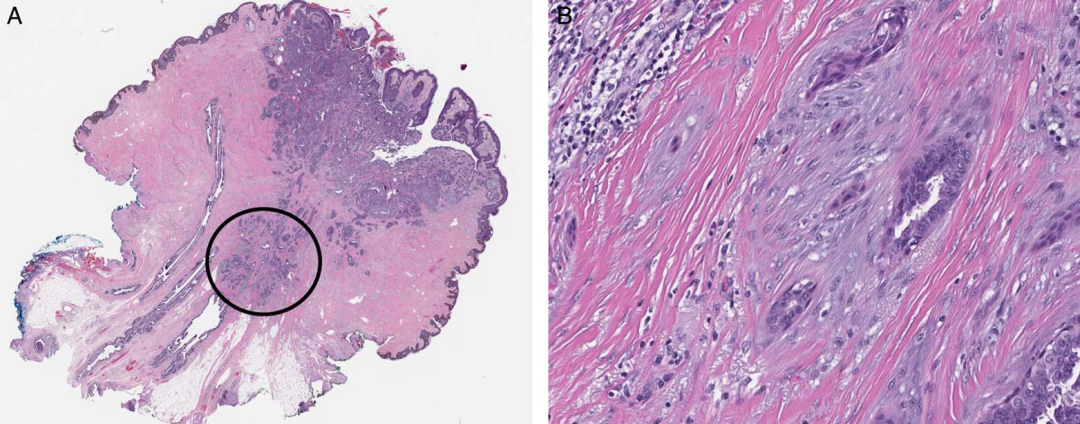
低级别腺鳞癌,可伴有乳头腺瘤(左图中黑圈所示);镜下可见鳞状细胞和腺上皮呈管状及逗点样巢状,并伴间质促纤维组织增生;可侵及乳头-乳晕复合体

乳头浸润性原发癌,非常罕见,要求肿瘤完全位于乳晕平滑肌之上、或侵犯平滑肌下方深度不足1cm,且大小小于上方的癌组织;图示病变位于乳头中央,仅轻度侵犯表浅的导管周围乳腺实质
乳头腺瘤诊断
定义
乳头腺瘤是一种具有乳腺导管样结构的良性上皮性病变,累及乳头导管开口及其周围间质和邻近的被覆表皮。
临床特点
流行病学:乳头腺瘤很少见,男性和女性均可发生,年龄范围很广,5个月至89岁均有发生,其中50岁女性最常见;
主要症状:大多数乳头腺瘤在临床检查时发现,皮肤表现不明显。若不及时发现切除,可持续多年而发展成大的肿块;可有乳头溢液、乳头表面红色糜烂;
影像表现:B超示乳头内或乳头后方圆/椭圆形低回声结节,境界清楚;
治疗及预后:手术切除即可;完全切除后预后好,如果不完全切除则可能会复发。目前尚不能排除乳头腺瘤与乳腺恶性肿瘤之间是否存在因果关系,但其发展为乳腺癌的风险不会超过与其他乳腺增生性病变。
大体形态
乳头部腺瘤形成结节状肿块,位于乳头浅表部位,通常与浅表皮肤相连续,多为单发类圆形肿瘤,直径一般小于2cm;切面呈灰白色或棕黄色,与周围组织分界清楚。
镜下形态
镜下肿物境界清楚,延伸至乳头表面代替鳞状上皮,可分为以下3种类型:
a.腺病型:腺体增生,周围间质内可见粗大胶原束,呈腺病、硬化性腺病样表现;
b.上皮增生型:腺上皮旺炽性增生,可呈实性、复杂乳头状形态;
c.硬化假浸润型:周围间质广泛纤维化、硬化,腺体扭曲变形,呈假浸润性生长模式;
上述三种类型的组织学形态常混合存在,另外可见鳞状上皮化、大汗腺化生、囊肿形成等病理改变。
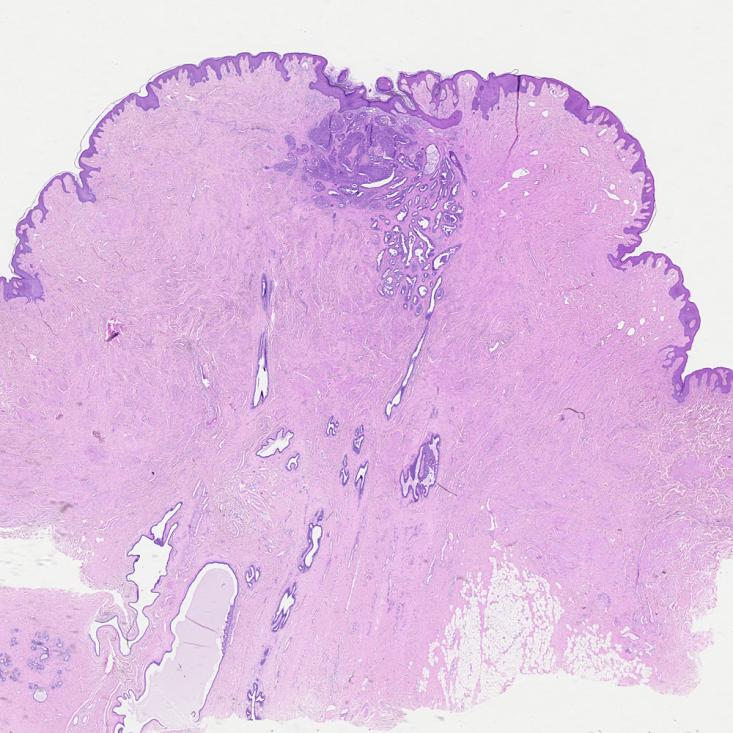
乳头腺瘤,肿物境界清楚,累及乳头皮肤
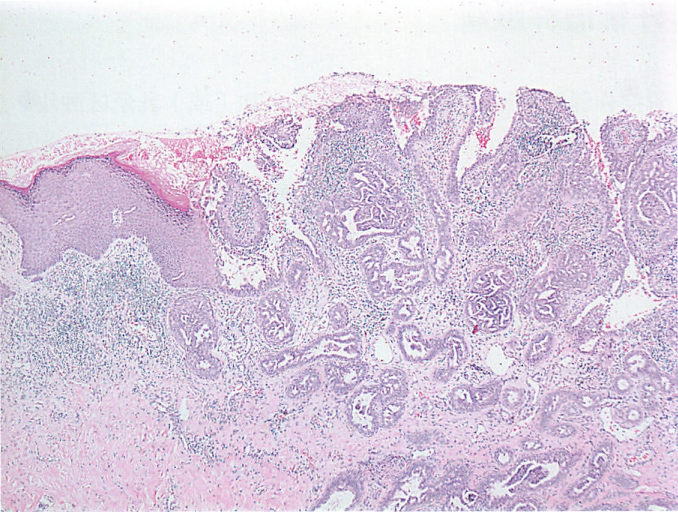
乳头腺瘤,腺上皮延伸至乳头表面代替鳞状上皮,大体可表现为红斑、糜烂
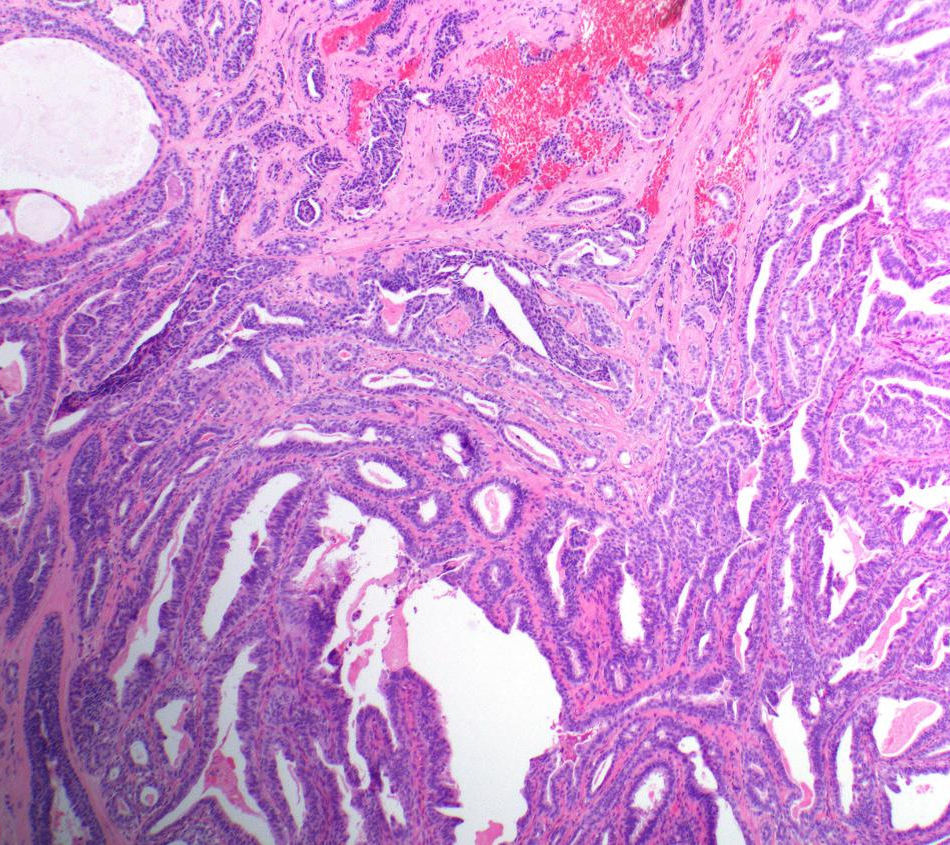
乳头腺瘤,肿瘤可在纤维化间质呈假浸润形态生长,也可呈乳头状瘤样生长
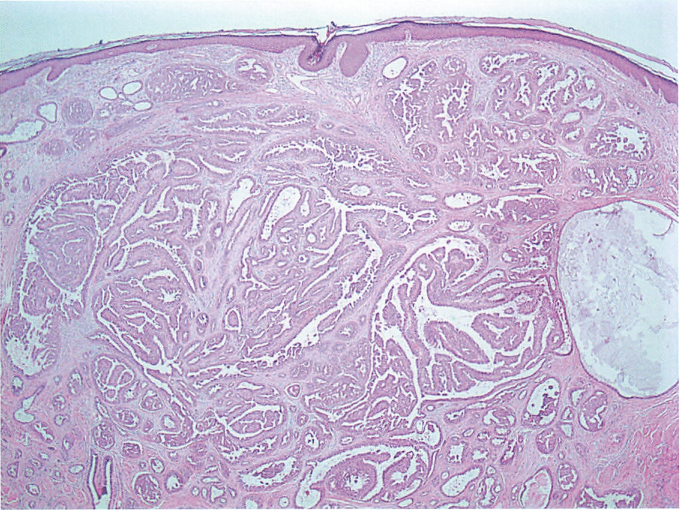
乳头腺瘤,肿瘤呈乳头状瘤样生长
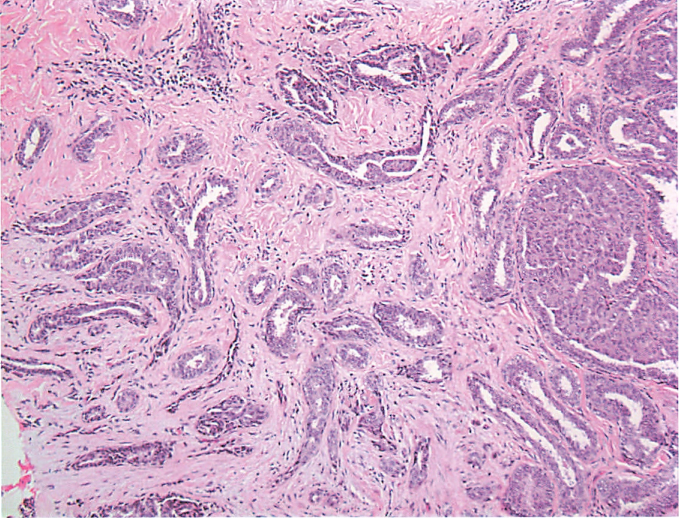
乳头腺瘤,肿瘤在纤维化间质背景中呈假浸润性生长
免疫组化
肌上皮标记物阳性,CK5/14及ER、PR呈异质性表达;
有研究发现5-羟甲基胞嘧啶(5-hmC)在乳腺癌中低表达,而在乳头腺瘤中高表达,认为其可作为乳头腺瘤的重要标志物。
分子及发病机制
目前发现PIK3CA 基因突变,包括KRAS 和BRAF 基因突变。
诊断标准
基本标准:
具有腺样结构的上皮增生性病变,累及乳头浅层导管开口、周围间质,通常与表皮相邻;低倍镜呈境界清楚的结节样结构;免疫组化肌上皮标记物阳性、ER增生的细胞异质性表达。
鉴别诊断
1.乳头Paget病
镜下Paget细胞异型性明显,细胞核大、不规则、呈单个或簇状分布于表皮内;免疫组化标记Paget细胞CK7、CAM5.2、HER-2、EMA均阳性,S-100阴性;
乳头腺瘤为良性增生的腺上皮向上伸入乳头并取代鳞状上皮,腺上皮细胞无异型性。
2.浸润性癌
浸润性癌呈弥漫浸润性生长;肿瘤异型性大,核分裂象易见;肿瘤性腺体周围无肌上皮围绕;
乳头腺瘤呈假浸润生长,但范围较局限,无深部组织的浸润;细胞无明显异型性,核分裂象罕见;免疫组化显示腺体周围均有肌上皮围绕。
3.导管原位癌
导管原位癌的癌细胞形态单一且分布均匀,有极向;其坏死范围广、程度重,坏死周围是癌细胞;免疫组化标记CK5/6多为阴性,ER、PR为弥漫一致的阳性;
乳头腺瘤增生的细胞为多克隆性,杂乱,缺乏极向;免疫组化CK5/6为阳性,ER、PR为强弱不等的阳性。
4.汗管瘤样肿瘤
汗管瘤样肿瘤的腺腔更小,拉长的小腺管常呈蝌蚪样、逗点状;缺乏腺病样腺管增生及上皮炽旺型增生等特点;无肌上皮,免疫组化染色SMA、Calponin均阴性。
5.小管癌
小管癌的腺管周围缺乏肌上皮;在极少数情况,乳头腺瘤可伴发小管癌,但乳头腺瘤的腺管为双层上皮,并且其缺乏深部组织浸润。
参考文献:
1.乳腺病理活检解读.(第3版) 2019 李国霞译.
2.乳腺病理诊断和鉴别诊断. 2014 丁华野.
3.乳腺病理学. 2021年 梅开勇,郭双平主译.
4.Brogi E, Scatena C. Nipple Lesions of the Breast: An Update on Morphologic Features, Immunohistochemical Findings and Differential Diagnosis.Adv Anat Pathol. 2023;30(6):397-414. doi:10.1097/PAP.0000000000000413.
5.WHO Classification of Breast Tumours. 5th Edition.
6.齐蕾, 赵振亚, 姚冬颖等. 乳腺乳头腺瘤6例临床病理分析[J]. 临床与实验病理学杂志, 2022, 第38卷(8):998-1000.
7.颜娇, 肖秀丽. 乳头腺瘤6例临床病理分析[J]. 临床与实验病理学杂志, 2022, 第38卷(2):208-210.
8.王成刚,马榕.乳头腺瘤的诊断与手术治疗[J].国际外科学杂志,2013,40(3):148-149.
刘彤华,陈杰,丁华野,等.刘彤华诊断病理学[M].4版.北京:人民卫生出版社,2019:723-724.
9.许伟伟,陈世荣,周晓军,吕京澴.乳腺乳头腺瘤4例并文献复习[J].临床与实验病理学杂志,2019,35(9):1082-1085.


