经导管主动脉瓣置换术的35个核心观点!新版临床路径专家共识
时间:2024-11-19 06:00:17 热度:37.1℃ 作者:网络
经导管主动脉瓣置换术(TAVR)已经日臻成熟,2017~2023 年期间我国开展中心数量由不到 10 家增加至 600 余家,每年置入量由数百例增加至超过 10 000 例,TAVR 在我国已进入持续稳定发展阶段。
《中国经导管主动脉瓣置换术临床路径专家共识 》2018 版及 2021 版在我国 TAVR 快速发展的黄金时期发挥了重要指导作用。随着 TAVR 领域在循证证据、应用经验、指南更新、器械研发、术式改良等方面的进展,尤其是中国原创技术及治疗方案优化等方面陆续取得重要突破,中国医师协会心血管内科医师分会结构性心脏病学组联合亚太结构性心脏病俱乐部于近日发布了新版临床路径专家共识。
新版共识提出了35个核心观点。
核心观点 1
TAVR 团队是一个由多学科组成的综合管理团队,负责术前评估、手术策略制定、手术实施及术后全病程管理。
核心观点 2
临床评估是以患者主动脉瓣疾病干预指征为核心的临床综合评估,其重点包括 TAVR 的适应证、手术方式选择及禁忌证三大步骤。内容包括主动脉瓣疾病症状及严重程度评估、临床基线数据的采集、心血管相关合并症的评估、非心血管相关合并症的评估、老年综合评估、神经系统功能评估和无效性评估。
核心观点 3
近年来 TAVR 指南更新的重点是适应证的拓展和干预方式的转变,强调干预方式选择依赖于临床评估团队和根据患者个体化的临床和解剖特点共同决策。
TAVR 的绝对适应证
主动脉根部及入路解剖结构符合 TAVR(特别是经股动脉 TAVR)要求且预期寿命> 1 年。
(1)年龄 70 岁及以上,有下列情况之一:①重度主动脉瓣狭窄患者有主动脉瓣狭窄导致的如下临床症状:运动性呼吸困难、心力衰竭、心绞痛、晕厥、既往或运动试验时晕厥先兆。②运动试验可以诱发症状或血压下降的无症状的重度 主动脉瓣狭窄患者。③无症状的重度 主动脉瓣狭窄,左心室射血分数(LVEF)<55%(无其他诱因导致的左心室收缩功能不全 )。④无症状的重度 主动脉瓣狭窄,LVEF>55%,运动试验结果正常,干预风险低且具备以下条件之一:极重度主动脉瓣狭窄[平均压差≥60 mmHg或最大峰值流速>5m/s];重度瓣膜钙化(经CT评估)且最大峰值流速进展≥0.3m/(s·y);经重复检测确认无其他诱因的B型利钠肽显著升高(大于经性别、年龄校正的正常值的3倍)。
(2)年龄小于70岁的重度主动脉瓣狭窄患者,存在外科手术禁忌或高危或存在其他危险因素,如胸部放射治疗后、肝功能衰竭、主动脉弥漫性严重钙化、极度虚弱等。
(3)外科主动脉生物瓣膜毁损。
TAVR的相对适应证
(1)年龄60~69岁的患者,满足TAVR的绝对适应证(1)中的条件之一,经过临床团队综合评估认为更适合行TAVR。
(2)二叶式重度主动脉瓣狭窄患者满足上述条件之一,可在有经验的中心(年手术量≥50例)或术者(年手术量≥25例)中开展。
(3)有症状的重度单纯主动脉瓣反流(PAR)患者,外科手术禁忌或高危,预期治疗后能够临床获益,解剖特点经过充分评估适合TAVR,可在有经验的中心(年手术量≥50例)或术者(年手术量≥25例)中开展。
(4)无症状的重度PAR患者,外科手术禁忌或高危,预期治疗后能够临床获益,解剖特点经过充分评估适合TAVR,需满足下述条件之一:左心室舒张末期内径>70mm;左心室收缩末期内径>50mm;左心室收缩末期内径指数>25mm/m2;
LVEF≤55%,可在有经验的中心(年手术量≥50例)或术者(年手术量≥25例)中开展。
TAVR的禁忌证
(1)左心室内新鲜血栓;(2)无纠正措施的左心室流出道严重梗阻;(3)急性心肌梗死不稳定期;(4)主动脉根部解剖形态不适合行TAVR治疗;(5)存在其他严重合并症,即使纠正了主动脉瓣疾病仍预期寿命不足1年。
核心观点 4
TAVR 围术期影像学评估中术前评估最为关键。CT 是评估主动脉根部及入路解剖结构和钙化的最重要手段,特定情况下超声心动图、心脏磁共振成像(CMR)、造影等检查方式可以达到协同或替代评估作用。人工智能分析、数值仿真及三维打印等新技术未来可能成为TAVR围术期评估的重要补充(表1)。
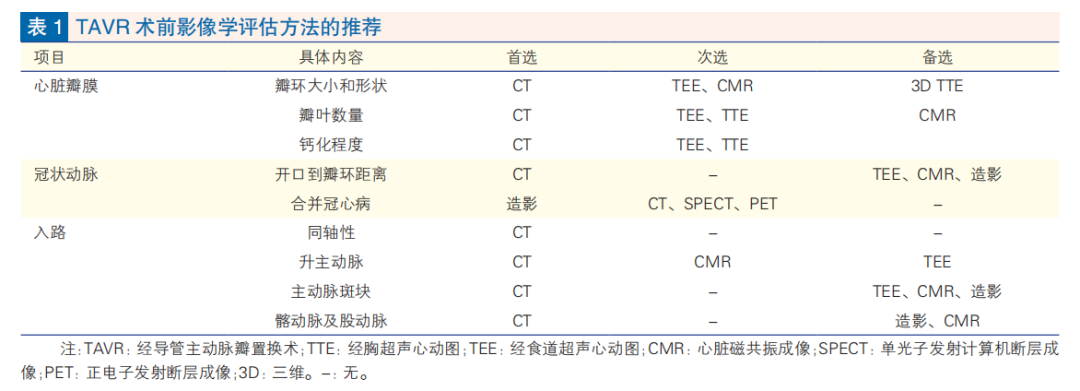
核心观点5
CT在TAVR术前评估、术中指导以及术后随访中处于核心地位,是术前人工瓣膜及入路选择的影像“金标准”,推荐心电门控全时相CT血管造影(CTA)扫描作为主动脉根部解剖评估的重要手段。
TAVR术前CT检查图像采集需评估患者心肾功能以及相关用药,尽量采用64排及以上CT扫描设备。
检查应包括3个方面内容:(1)心电门控非增强CT扫描;(2)心电门控全时相CTA扫描;(3)大范围非心电门控螺旋CTA扫描,扫描范围及重建参数需特别关注(表2)。

核心观点6
术者需要熟练掌握CT影像评估方法并对结果进行充分解读及个体化分析,可根据图像结果识别解剖难度、评估风险并制定正确的手术策略。
核心观点7
建议TAVR术后半年内常规行全时相CT扫描,评价瓣膜置换效果、位置、冠状动脉再介入可行性及血栓情况,制定合理抗栓方案。
核心观点8
超声心动图主要评价主动脉瓣病变的严重程度、其他瓣膜及心脏功能及围术期并发症是围术期影像评价的重要手段。
基于目前TAVR适应证向外科低危患者拓展,人工生物瓣膜耐久性成为术后评价的重要指标。瓣膜学术联盟-3标准所提出的生物瓣膜功能障碍分为结构性瓣膜退化、非结构性瓣膜功能障碍、临床瓣膜血栓形成或心内膜炎。其中结构性瓣膜退化被定义为人工瓣膜发生的内在性永久性变化,包括磨损、瓣叶破损、瓣叶连枷、瓣叶纤维化和(或)钙化,支架断裂或变形,非结构性瓣膜功能障碍被定义为人工瓣膜本身以外任何因素导致的瓣膜功能障碍。
核心观点9
生物瓣膜功能障碍的严重程度主要衡量指标为跨瓣压差绝对值升高,跨瓣压差较前进展,有效瓣口面积减少以及多普勒速度指数减少等,作为术后超声心动图随访评价瓣膜耐久性的重要指标,需特别关注。生物瓣膜退化分为三个阶段,具体见表3。

核心观点10
人工智能及3D打印等影像学新技术应用于TAVR患者影像学分析,可辅助提升评估的精准性和效率、缩短术者的学习曲线,有望进一步降低手术并发症风险,成为TAVR术前评估的重要手段。
TAVR手术数值模拟仿真及3D打印技术:TAVR数值模拟仿真可以根据患者解剖特点,通过计算机数值模拟不同尺寸和类型支架的置入效果,选择最优瓣膜型号和释放位置,分析并发症风险。3D打印技术通过CT构建3D模型进行仿真与体外模拟,优化手术策略与效果。
核心观点11
在TAVR术前评估中,CMR可在特定条件下作为CT的合理替代方案。
核心观点12
完整的多学科团队和完善的杂交手术室是TAVR的最好保障,但随着技术的发展和熟练程度的增加,各中心根据医院条件、团队配备情况在保障手术安全顺利的情况下,因地制宜地在导管室采用简化TAVR是可以推荐的。需根据术前评估方案及患者个体化需求充分准备好手术器械。
核心观点13
充分的麻醉术前准备非常必要,应根据患者的状况采用不同的麻醉方式。决定TAVR麻醉方式的选择主要包含三大方面的因素,分别来自患者本身、术者和麻醉医师、TAVR的入路,其中最主要的因素是入路。
经股动脉入路TAVR建议优选镇静或监护麻醉方式,对于特殊入路、危重患者及各中心早期开展阶段可选择全身麻醉。
核心观点14
股动脉入路是TAVR最主要的入路,90%以上患者可以选择股动脉入路。对于股动脉,如无钙化,一般置入鞘管外面积可以超过血管面积20%~30%。在我国,颈动脉、锁骨下动脉(腋动脉)途径已成为仅次于股动脉途径之外的常用外周血管入路。
核心观点15
进行瓣膜选择时应结合术前CT综合评估结果,如瓣膜的分型、瓣膜钙化分布、冠状动脉堵塞风险、永久起搏器植入可能性、瓣环破裂风险、生物瓣膜不匹配等,并根据患者血管入路情况和人工瓣膜特性,做到个体化选择,必要时结合术中球囊扩张的结果。
目前中国大陆共有8款经股动脉入路的TAVR瓣膜、1款经心尖入路的TAVR瓣膜上市,包括球囊扩张式瓣膜、自膨胀式瓣膜两大类,其中已有4款升级为可回收系统。数款针对PAR的经股动脉途径瓣膜已经完成临床试验,即将应用于临床。
核心观点16
TAVR术前完善脑血管和神经系统功能评估,对于高危栓塞风险的患者与神经内、外科及血管外科专家共同制定治疗策略,并推荐使用脑保护装置。
核心观点17
瓣膜置换前应基于临床和影像评估结果合理制定手术方案。包括临时起搏电极植入,跨瓣角度的选择以及跨瓣导丝的操作,瓣膜释放角度的判定,球囊预扩张方案,瓣膜类型及型号选择和可能出现的并发症以及处理预案。
核心观点18
瓣膜输送时,应特别关注跨越主动脉弓和主动脉瓣这两个位置的过程。不同类型的瓣叶结构,不同型号的瓣膜,对起始定位的高度要求有所不同。应从术前CT分析中确定TAVR瓣膜的锚定区和封堵区,决定起始位置及优选释放位置。
核心观点19
术后应观察血液动力学情况,通过超声心动图和主动脉根部造影来评估瓣膜的位置及反流情况,同时观察二尖瓣、左心室功能以及术中并发症。
核心观点20
TAVR术中常见并发症包括循环崩溃、瓣周漏、瓣膜移位、冠状动脉闭塞及心肌梗死、脑卒中、血管并发症、传导阻滞,需特别关注。
核心观点21
TAVR术中其他并发症包括:(1)心包积液及心包填塞;(2)左心室左心房漏;(3)主动脉瓣环撕裂;(4)主动脉夹层、撕裂;(5)二尖瓣功能损伤;(6)感染性心内膜炎;(7)瓣膜血栓;(8)急性肾功能损伤;(9)出血。
核心观点22
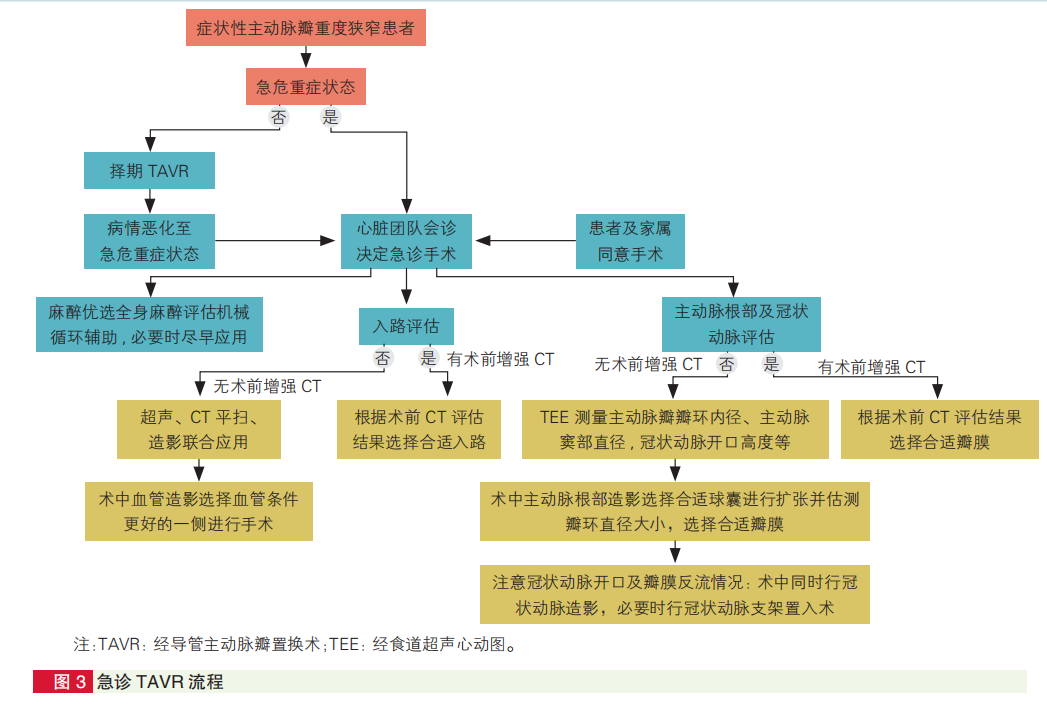
对药物治疗反应性差的难治性症状性重度主动脉瓣狭窄患者,伴或不伴有血液动力学不稳定,需要最短时间内完成的紧急经导管主动脉瓣球囊扩张或主动脉瓣置换术,定义为急诊主动脉瓣球囊扩张术/TAVR。
核心观点23
急诊主动脉瓣球囊扩张术/TAVR适应证包括:(1)心原性休克;(2)合并有持续性室性心动过速或发生心室颤动;(3)药物难以改善需要机械循环辅助装置的不稳定性心绞痛或慢性心力衰竭;(4)在TAVR评估及手术阶段出现血液动力学崩溃接受心肺复苏的患者。
核心观点24
如果决定使用机械循环辅助装置,建议在TAVR术前预防性植入,优选体外膜氧合装置,如不具备条件,可选择主动脉内球囊反搏装置。
核心观点25
因病情严重无法完善增强CT时,平扫CT、术中3D-TEE及血管造影的联合应用对于入路及根部评价有一定的作用。
核心观点26
简化TAVR的安全性和有效性不逊于传统TAVR,能够促进患者早期恢复,缩短住院时间,降低医疗费用。各中心可因地制宜,制定适合本中心的简化手术方案(表5)。
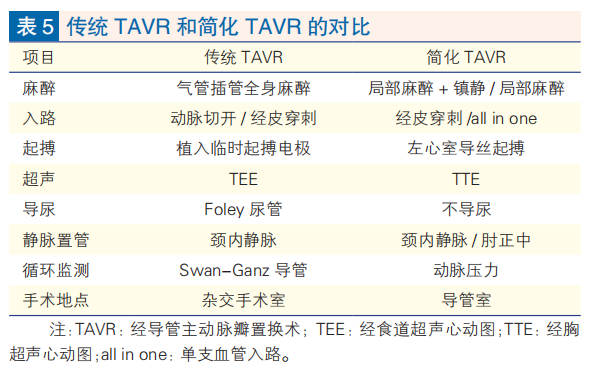
简化TAVR倾向于选择血管解剖条件合适的低危患者,应遵从个体化的原则,筛选标准包括:(1)具备合适的血管入路;(2)冠状动脉闭塞风险较低;(3)无慢性疼痛;(4)TTE声窗条件好;(5)可紧急插管;(6)可以平卧。不适宜行简化TAVR的标准包括:(1)入路血管条件较差;(2)冠状动脉闭塞风险较高;(3)瓣环破裂风险较高;(4)患者焦虑、术中不能配合;(5)瓣膜大小不确定;(6)患者无法平卧;(7)TTE声窗差。
核心观点27
我国目前尚无确切主动脉瓣反流患病率的流行病学数据,但现有证据显示其流行病学规律不同于西方,我国的主动脉瓣反流可能更常见。
核心观点28
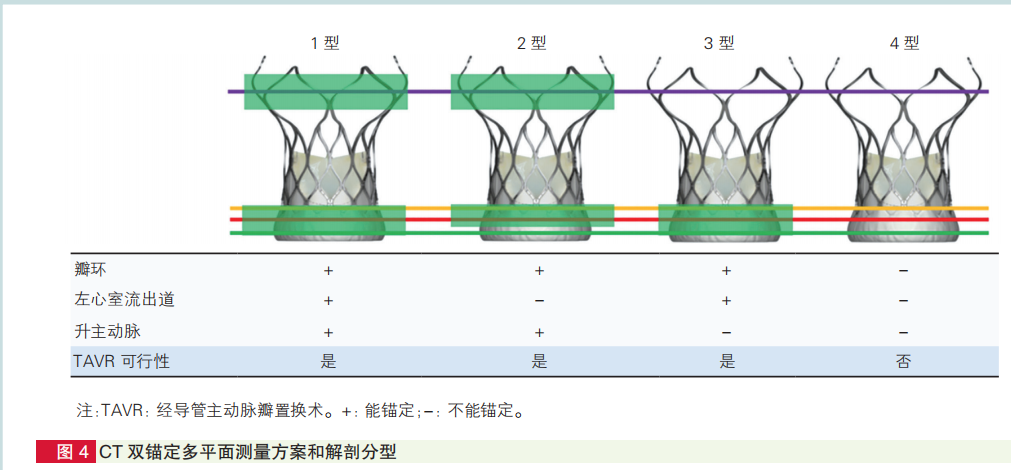
CT双锚定多平面测量方案和解剖分型对PAR的TAVR有指导意义。建议人工瓣膜在锚定平面的直径(周长)超尺寸比率应在10%以上。
CT双锚定多平面测量方案和解剖分型对TAVR有指导意义:1型:瓣环、左心室流出道、升主动脉均能锚定;2型:左心室流出道不能锚定,瓣环、升主动脉可锚定;3型:瓣环、左心室流出道可锚定、升主动脉不能锚定;4型:瓣环、左心室流出道、升主动脉均不能锚定(图4)。
核心观点29
重度主动脉瓣狭窄合并冠心病发病率为30%~50%,但是目前关于冠心病是否影响TAVR患者预后的临床研究结果并不完全一致,而且这些冠心病患者是否均需要血运重建仍存在争议。
核心观点30
一站式TAVR+经皮冠状动脉介入治疗(PCI)应在有经验的中心开展,早期应选择简单组合进行处理,建议进行预先跨瓣置入猪尾导管。对于合并左主干病变、多个靶病变、需要旋磨以及二叶式主动脉瓣的复杂TAVR+PCI一站式治疗的患者,应特别注意基础心功能及肾功能,避免多个难点进行组合导致手术难度过大、时间过长、对比剂用量过多从而增加风险。
手术过程中对于冠状动脉病变复杂及基础心功能状态不佳患者,应充分评估其麻醉方式及是否需要左心辅助装置。
核心观点31
左心耳封堵术(LAAC)是TAVR合并心房颤动患者重要的脑卒中二级预防手段,对于出血高危患者或术后无法坚持长期抗凝患者可考虑行同期手术。
核心观点32
盘式封堵器患者可口服氯吡格雷75 mg qd+阿司匹林100 mg qd,半年后改为口服阿司匹林100mgqd;塞式封堵器患者可口服抗凝+阿司匹林100 mg qd 45d,45 d后改为阿司匹林100 mg qd+氯吡格雷 75 mg qd至术后6个月,6个月后阿司匹林100 mg qd持续服用。若患者不能耐受高强度抗栓治疗,抗栓方案可根据患者耐受程度降级。术后第45天、6个月时通过TEE或CTA观察封堵器是否完全封闭左心耳,有无器械表面血栓。
核心观点33
生物瓣损毁是即将面对的重要问题,包括在外科毁损瓣中行TAVR治疗(TAVR-in-SAVR)及在TAVR毁损瓣中行TAVR治疗(TAVR-inTAVR)的瓣中瓣技术是解决生物瓣毁损的重要方式。
核心观点34
TAVR患者病情复杂并发症病情变化快,围术期管理尤为重要。
核心观点35
术后随访和康复对TAVR患者术后远期预后和生活质量具有重要作用。
随着TAVR适应证的拓宽、手术器械的多样化、操作流程优化,TAVR在我国必将有着更为广泛的应用。通过十余年的不懈探索,中国数据和方案在TAVR领域已经开始在国际舞台绽放,并具有越来越大的影响力。
来源:中国医师协会心血管内科医师分会结构性心脏病学组,亚太结构性心脏病俱乐部.中国经导管主动脉瓣置换术临床路径专家共识(2024版).中国循环杂志,2024,38(11):1041-1057 DOI: 10.3969/j.issn.1000-3614.2024.11.001.


