J Autoimmun:联合治疗在免疫介导炎症性疾病中的疗效与安全性
时间:2024-11-20 20:01:16 热度:37.1℃ 作者:网络
免疫介导的炎症性疾病(IMID)包括类风湿关节炎(RA)、炎症性肠病(IBD)等,常因多重炎症通路的复杂性而导致单药治疗效果有限。高级联合治疗(ACT),即至少两种生物制剂、生物制剂与小分子药物或两种小分子药物的联合应用,已在其他医疗领域显示出潜在优势。然而,IMID中ACT的疗效和安全性尚未得到全面评估。本研究旨在通过系统综述和荟萃分析,比较ACT与单药治疗在IMID中的临床缓解率及安全性,以期为临床治疗提供循证依据。

本研究遵循PRISMA指南,系统检索了截至2023年7月的文献,纳入符合标准的10项随机对照试验(RCTs),共包含1154例患者。研究对象覆盖RA(7项RCTs)、系统性红斑狼疮(SLE)(1项RCT)及IBD(2项RCT)。ACT包括抗肿瘤坏死因子(TNF)药物与抗IL-23、抗IL-1或小分子药物的联合治疗,或其他机制不同的药物组合。主要终点为临床缓解率,次要终点为不良事件(AE)、严重不良事件(SAE)、感染及严重感染。通过随机效应模型进行荟萃分析,采用GRADE评估证据质量,并分析异质性来源。
本研究通过对10项RCT的荟萃分析,对ACT与单药治疗在IMID中的疗效和安全性进行了系统评估,结果显示不同疾病类型的疗效和安全性存在显著差异。在类风湿关节炎(RA)患者中,ACT未显示出比单药治疗更高的临床缓解率(ACR70标准:RR=1.75, 95% CI: 0.60–5.13, I²=33%)。即使使用更宽松的ACR50和ACR20标准,ACT组与单药组在缓解率上亦无显著差异(ACR50: RR=1.39, 95% CI: 0.74–2.63, I²=46%;ACR20: RR=1.33, 95% CI: 0.85–2.10, I²=73%)。此外,ACT组不良事件的发生率高于单药组(RR=1.07, 95% CI: 1.01–1.12, I²=0%),但在严重不良事件、感染和严重感染的发生率方面,两组差异不显著(RR=1.96, 95% CI: 0.83–4.59, I²=36%)。对于系统性红斑狼疮(SLE),ACT的临床缓解率与单药治疗相当(RR=1.20, 95% CI: 0.53–2.72),且未增加不良事件风险。
在炎症性肠病(IBD)患者中,ACT表现出显著优势,显著提高了临床缓解率(RR=1.68, 95% CI: 1.15–2.46, I²=15%)。分疾病类型分析显示,ACT在溃疡性结肠炎(UC)中表现尤为突出(RR=1.90, 95% CI: 1.30–2.78),而在克罗恩病(CD)中的缓解率则未达到统计学显著性(RR=1.23, 95% CI: 0.62–2.44)。在安全性方面,ACT并未显著增加IBD患者的不良事件(RR=0.92, 95% CI: 0.80–1.05, I²=18%)、感染(RR=0.84, 95% CI: 0.47–1.49, I²=0%)或严重感染(RR=6.00, 95% CI: 0.25–145.45)的风险。
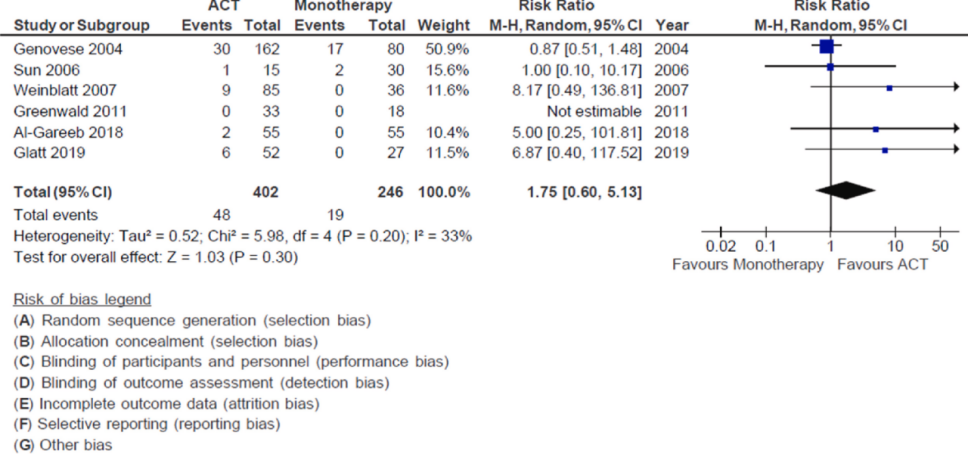
比较ACT与单药治疗在RA患者中实现临床缓解(定义为ACR 70)的森林图
本研究表明,ACT在RA和SLE患者中未表现出显著的临床优势,且增加了不良事件风险。但在IBD患者中,ACT可能提供更高的临床缓解率,且安全性与单药治疗相当。未来研究应聚焦于ACT的机制优化、患者分层以及长期疗效和安全性评估,以探索更适合不同IMID的个体化治疗策略。
原始出处:
Efficacy and safety of Advanced Combination Treatment in immune-mediated inflammatory disease: A systematic review and meta-analysis of randomized controlled trials. J Autoimmun. 2024 Nov 6;149:103331. doi: 10.1016/j.jaut.2024.103331. Epub ahead of print. PMID: 39509741.


