STTT:突破实体瘤治疗困境,曹雪涛院士团队发表论文揭示CAR-NK细胞疗法新机制
时间:2025-03-06 12:11:20 热度:37.1℃ 作者:网络
编者按:2025年3月3日,海军医科大学曹雪涛院士团队联合刘秋燕、郭猛团队在国际知名期刊《Signal Transduction and Targeted Therapy》上发表题为“Neoleukin-2/15-armored CAR-NK cells sustain superior therapeutic efficacy in solid tumors via c-Myc/NRF1 activation”的研究论文。

该研究揭示,通过Neo-2/15优化CAR-NK细胞的代谢功能,能够显著增强其在代谢不良的肿瘤微环境(TME)中的活性。这一发现为利用代谢修饰策略提升NK细胞活性、对抗实体瘤免疫抑制提供了潜在的通用解决方案,有望为实体瘤治疗开辟新的路径。
1 摘要
嵌合抗原受体(CAR)修饰的自然杀伤(NK)细胞过继转移为恶性血液病患者带来了显著的临床改善,堪称一种革命性的治疗策略。然而,在实体瘤治疗中,CAR-NK细胞的疗效受到免疫抑制性肿瘤微环境(TME)的显著限制,主要表现为细胞耗竭、浸润能力受损以及持久性不足。鉴于NK细胞的功能状态与IL-2信号通路密切相关,我们设计了一种新型的间皮素特异性CAR-NK细胞,使其能够分泌新型白细胞介素-2/15(Neo-2/15)。Neo-2/15作为一种IL-2Rβγ激动剂,能够有效抵抗TME内的免疫抑制极化。经过改造的Neo-2/15增强型CAR-NK细胞在TME中展现出更强的细胞毒性、更低的耗竭水平以及更长的持久性,从而在胰腺癌和卵巢癌治疗中表现出更优越的抗肿瘤活性。
从机制上来看,Neo-2/15为CAR-NK细胞提供了持续增强的IL-2受体下游信号传导,促进c-Myc和核呼吸因子1(NRF1)的表达。这种上调对于维持CAR-NK细胞的线粒体适应性和代谢韧性至关重要,最终导致细胞毒性增加和在TME内的显著持久性。NRF1的上调是Neo-2/15诱导的增强效应的关键,也是抵抗TME免疫抑制极化的重要机制。实验表明,NRF1的过表达显著增强了CAR-NK细胞的抗肿瘤效果,无论是在体外还是体内实验中,均表现为ATP产量的增加。总体而言,表达Neo-2/15的CAR-NK细胞通过抵抗耗竭和在实体瘤中更长的存活时间,展现出更优越的抗肿瘤效果,为实体瘤治疗提供了新的思路和策略。
2 研究背景
嵌合抗原受体(CAR)改造的免疫细胞过继转移是癌症免疫治疗的前沿应用。CAR-T细胞虽在某些癌症治疗中取得成功,但细胞因子释放综合征(CRS)和免疫毒性限制了其广泛应用。自然杀伤(NK)细胞因低CRS风险和独特的细胞因子谱成为替代方案,且在异体移植中表现出低移植物抗宿主病(GvHD)风险,为过继细胞治疗提供了更安全的选择。
CAR-NK细胞疗法在血液系统恶性肿瘤中疗效显著,但在实体瘤(如胰腺导管腺癌,PDAC)治疗中证据有限。PDAC的免疫抑制性肿瘤微环境(TME)限制了CAR-NK细胞的疗效,表现为代谢环境恶劣、免疫细胞功能失调和耗竭。TME的免疫抑制特性削弱了CAR-NK细胞的细胞毒性和持久性。
为克服TME的免疫抑制,研究者采用多种策略增强CAR改造免疫细胞的疗效,包括上调趋化因子受体、破坏癌症相关成纤维细胞和耗竭转录因子。然而,这些方法尚未解决免疫细胞在TME中的能量供应和存活问题。NK细胞的代谢韧性与效应功能密切相关,可通过细胞因子信号传导调节。白细胞介素(IL)-2或IL-15激活相关信号通路,增强NK细胞的代谢和功能。
本研究探讨自分泌超级细胞因子(如Neo-2/15)在实体瘤CAR-NK细胞疗法中的潜力。Neo-2/15通过激活IL-2Rβγ信号通路,增强CAR-NK细胞的抗肿瘤效果。研究发现,Neo-2/15激活STAT5/Akt通路,增强NK细胞对TME免疫抑制的抵抗力,并通过NRF1过表达提高ATP生成和抗肿瘤效果。
3 研究结果
1.Neo-2/15显著增强NK细胞的激活,同时防止其耗竭
IL-2和IL-15共享IL-2Rβγ受体亚基。为了为促进NK细胞增殖和活性提供有力基础,我们对这些天然细胞因子及其类似物超级细胞因子H9、H9T、N72D和Neo-2/15进行了筛选,以确定增强NK细胞功能的最佳IL-2R刺激物(图1a)。我们首先分析了它们对来自年轻和老年健康个体、接受化疗的癌症患者以及接受免疫抑制剂的器官移植受者的外周血中NK细胞增殖的影响。在这些激动剂中,Neo-2/15显著增强了来自多位供体的原代NK细胞的扩增(图1b-f和补充图1a-e)。此外,Neo-2/15也显著增强了人NK细胞系NK-92的增殖,其半数有效浓度(EC₅₀)值为0.018 nM,与IL-2的0.087 nM或H9T的0.043 nM相比(图1)。
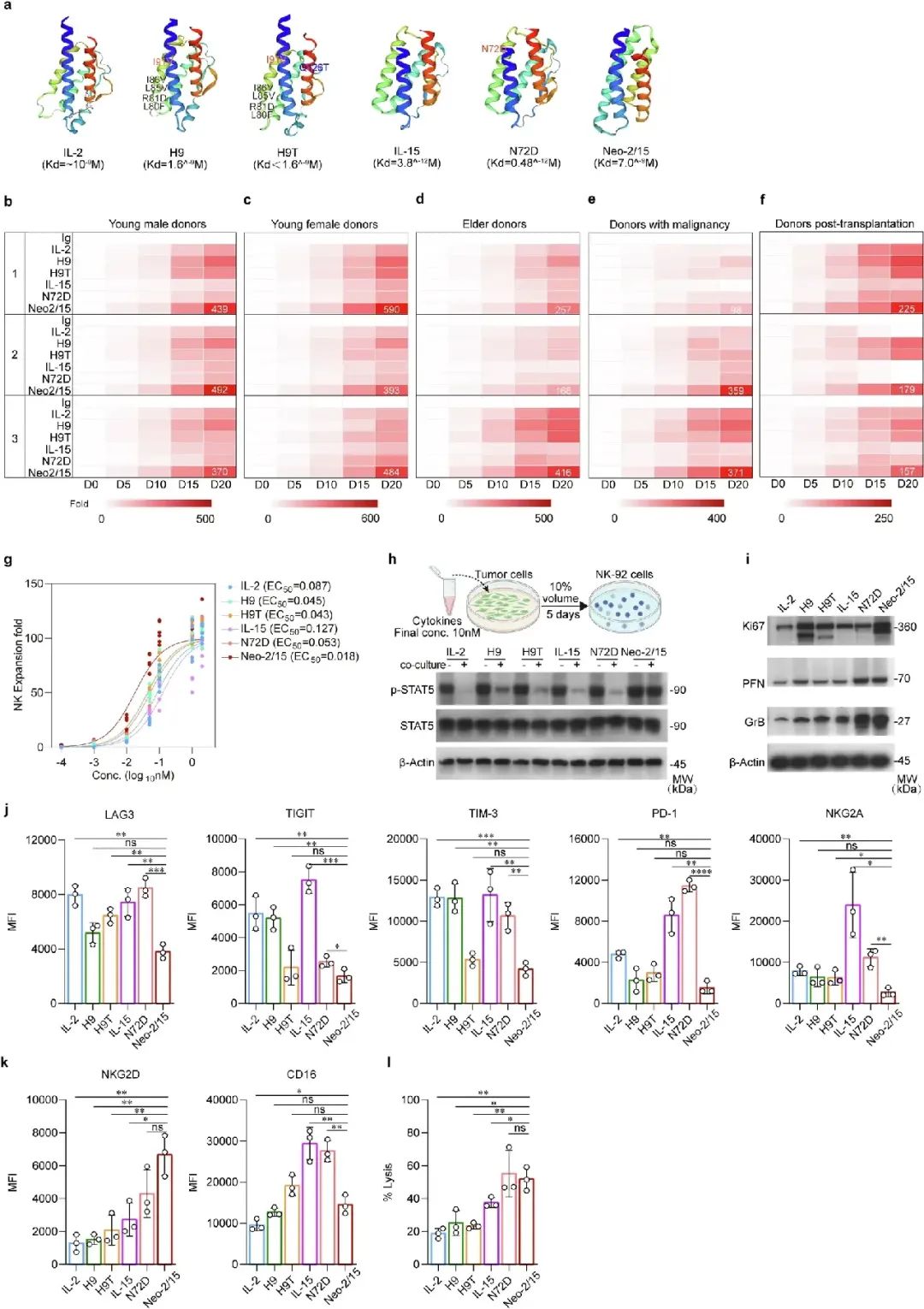
为了评估这些激动剂的稳定性,我们将它们加入到人胰腺癌细胞系AsPC-1的培养基中,并在5天后收集上清液,用于处理NK-92细胞(图1h,上)。这些激动剂的培养基均能诱导STAT5的磷酸化,然而,当在肿瘤细胞上清液中培养时,只有Neo-2/15能够在NK-92细胞中维持STAT5的磷酸化,与其他激动剂相比表现出更少的降解(图1h,下;补充图1f),这表明Neo-2/15在上清液中具有较高的稳定性。鉴于AsPC-1是一种高表达HMGB1的细胞系,而HMGB1可以激活NK细胞,我们使用HMGB1中和抗体中和培养上清液中的潜在HMGB1。值得注意的是,即使在中和HMGB1后,Neo-2/15仍能在NK-92细胞中维持STAT5的磷酸化(补充图1g)。同样,Neo-2/15处理显著增加了NK-92细胞中增殖标志物Ki67以及效应分子PFN和GrB的表达,与其他激动剂相比(图1i和补充图2a)。此外,Neo-2/15处理的NK细胞表现出更低水平的抑制性受体(图1j和补充图2b),以及更高的NKG2D和CD16表达(图1k和补充图2c),这与对K562细胞的第二高细胞毒性相对应(图1l和补充图2d,e)。综上所述,Neo-2/15有效地促进了NK细胞的增殖,增强了其细胞毒性能力,并减轻了NK细胞的耗竭,从而有助于实现良好的抗肿瘤反应。因此,我们继续测试Neo-2/15作为CAR-NK细胞的“装甲”,以延长免疫激活并抵抗TME诱导的功能障碍。
2.Neo-2/15增强CAR-NK细胞的抗肿瘤效果
我们通过将编码抗间皮素(MSLN)单链抗体(scFv)与4-1BB和CD3ζ细胞内信号域融合的慢病毒载体转导到NK-92细胞中,生成了MSLN特异性的CAR-NK细胞(以下简称为BBζ)。随后,BBζ细胞被进一步转导以表达Neo-2/15(以下简称为BBζ-Neo)(图2a和补充图3a、b)。通过将BBζ和BBζ-Neo与MSLN阳性的肿瘤细胞(AsPC-1、MSLNOE PANC-1或MSLNOE BxPC-3,补充图3c)在1:1或5:1的效应细胞与靶细胞比例(E:T)下共培养4小时,测量其细胞毒性。与未转导的NK-92或BBζ相比,BBζ-Neo表现出最强的细胞毒性(图2b)。此外,在与AsPC-1细胞共培养后,BBζ-Neo或BBζ的颗粒酶B(GrB)表达水平高于NK-92(图2c和补充图3d),而穿孔素(PFN)或CD107a的表达在BBζ-Neo中显著高于BBζ或NK-92(图2c、d和补充图3d、e)。此外,BBζ-Neo表达的免疫抑制分子水平低于BBζ或NK-92(补充图3f)。此外,在与肿瘤细胞共培养时,BBζ-Neo分泌的IFNγ、IL-1β、IL-6、MCP-1、TNF-α和IL-8水平显著高于BBζ(图2e、f)。除了使用细胞系进行实验外,我们还利用来自胰腺导管腺癌(PDAC)的患者来源类器官(PDO)进行实验,这些PDO经验证表达MSLN(补充图3g、h)。与BBζ相比,BBζ-Neo处理的PDO显示出显著的形态崩溃,表明细胞死亡(图2g)。
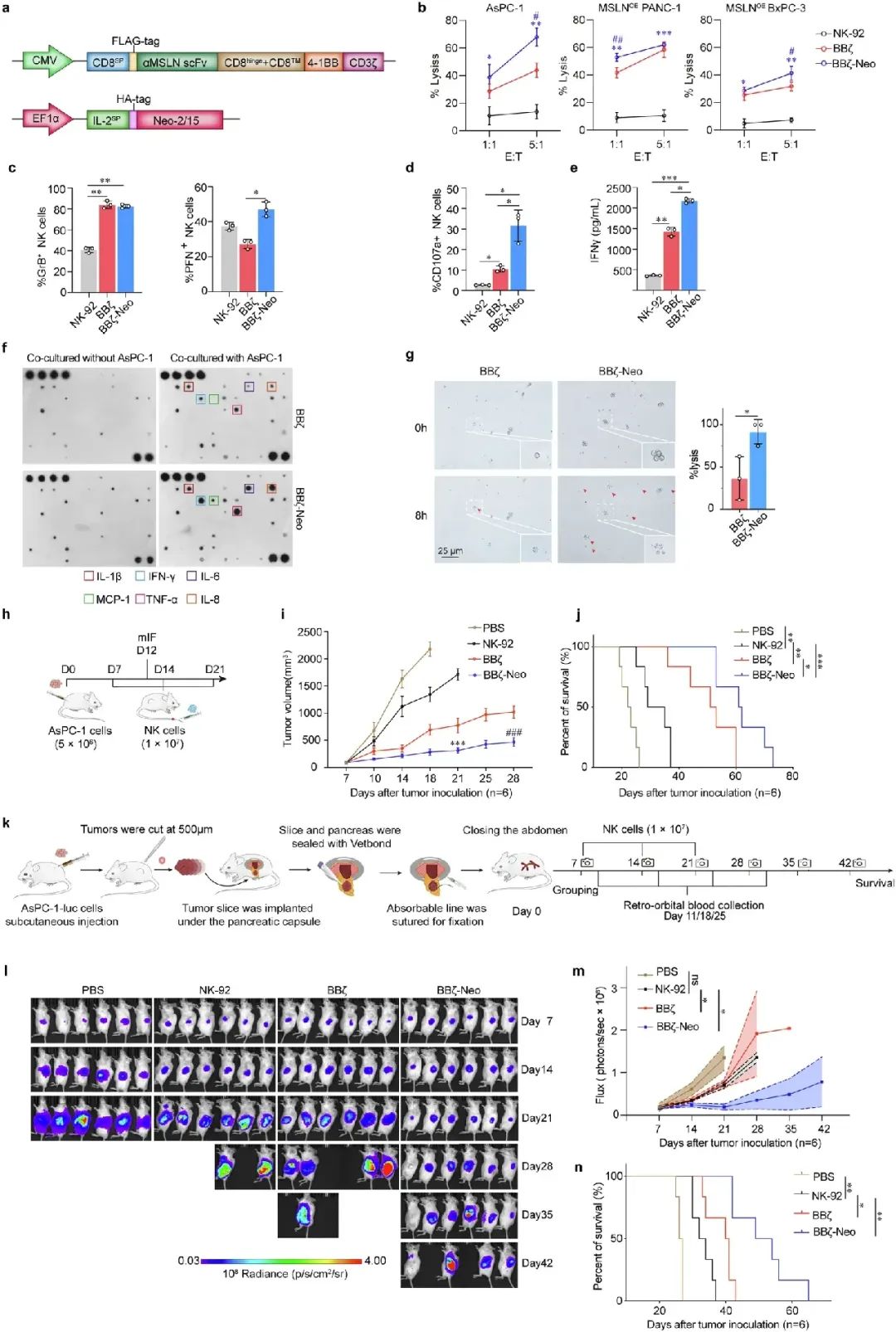
为了评估BBζ-Neo的体内抗肿瘤活性,我们将NCG小鼠皮下植入AsPC-1人胰腺导管腺癌(PDAC)细胞,随后在7天后向这些荷瘤小鼠分别注射PBS(对照组)、NK-92、BBζ或BBζ-Neo(图2h)。与BBζ或NK-92注射相比,BBζ-Neo治疗导致肿瘤负荷最低(图2i)和生存期最长(图2j),并且在肿瘤中检测到更多的NK细胞浸润(补充图4a、b)。如预期所示,浸润的NK细胞表现出更高的激活标志物CD107a水平和更低的耗竭标志物TIGIT表达(补充图4a-d)。为了更好地模拟PDAC的肿瘤微环境,我们进一步利用原位模型评估这些NK细胞的疗效(图2k)。结果一致显示,BBζ-Neo治疗在控制肿瘤生长和延长荷瘤小鼠生存期方面优于对照组和其他NK细胞注射(图2l-n)。此外,BBζ-Neo还有效抑制了MSLN阳性的人卵巢癌细胞Caov-3来源的异种移植瘤的生长,并提高了小鼠的生存率(补充图4e-g)。这些发现表明,Neo-2/15在体内显著增强了CAR-NK细胞对MSLN阳性实体瘤的疗效。
3.Neo-2/15通过STAT5/Akt/c-Myc信号通路增强CAR-NK细胞的细胞毒性
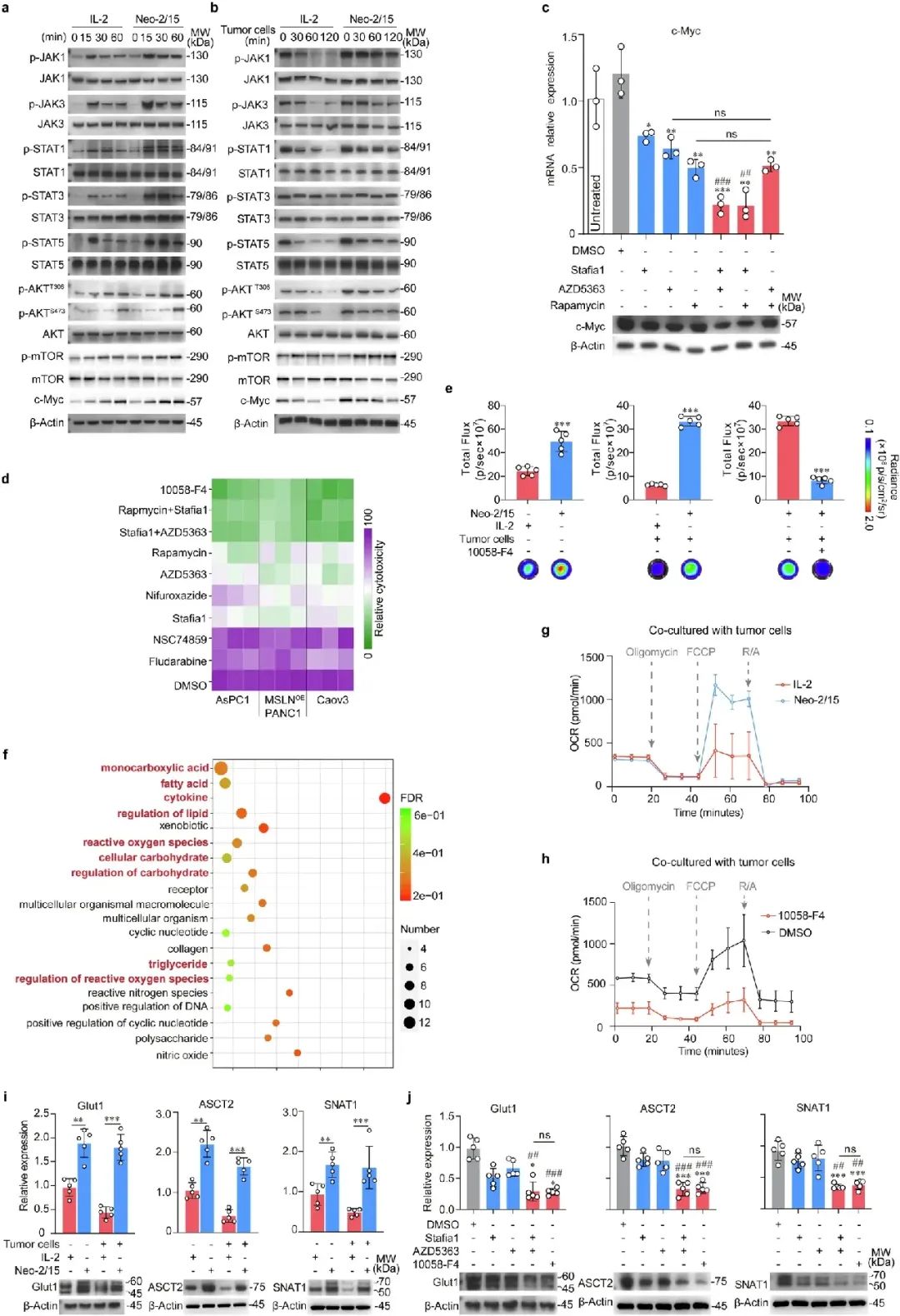
本研究进一步探讨了Neo-2/15和IL-2激活IL-2R下游信号通路的能力。结果显示,Neo-2/15和IL-2均能有效激活JAK1/3-STAT1/3/5和Akt-mTOR信号通路,并适度上调c-Myc在BBζ细胞中的表达(图3a)。然而,在与AsPC-1细胞共培养(模拟肿瘤微环境,TME)时,Neo-2/15刺激的BBζ细胞中c-Myc表达和IL-2R下游信号的衰减速度明显慢于IL-2刺激的BBζ细胞(图3b和补充图5a)。此外,在Neo-2/15刺激的BBζ细胞中,同时抑制STAT5和Akt或STAT5和mTOR显著降低了c-Myc的表达(图3c)。随后,我们对Neo-2/15刺激的BBζ细胞分别使用针对STAT1(Fludarabine)、STAT3(NSC74859)、STAT5(Stafia1)、STAT1/3/5(Nifuroxazide)、Akt(AZD5363)、mTOR(Rapamycin)或c-Myc(10058-F4)的抑制剂处理后,再与三种MSLN阳性肿瘤细胞系共培养。结果显示,c-Myc抑制剂或STAT5与Akt或STAT5与mTOR的双重抑制几乎完全消除了Neo-2/15刺激的BBζ细胞的细胞毒性(图3d)。综上所述,Neo-2/15通过增强STAT5和Akt的激活来增强CAR-NK细胞的细胞毒性,其中c-Myc作为该信号级联中的主要下游效应因子发挥了关键作用。
c-Myc在Neo-2/15刺激的BBζ细胞中的作用机制
接下来,我们探讨了c-Myc在TME中对Neo-2/15刺激的BBζ细胞细胞毒性的作用机制。c-Myc是淋巴细胞和肿瘤细胞代谢的关键调节因子,其在代谢中的作用已被广泛研究。我们进一步分析了IL-2和Neo-2/15刺激的BBζ细胞的代谢特征。结果显示,Neo-2/15刺激组的ATP生成显著高于IL-2刺激组,即使在与AsPC-1细胞共培养时也是如此(图3e)。值得注意的是,抑制c-Myc显著降低了Neo-2/15刺激的BBζ细胞在与AsPC-1细胞共培养时的ATP水平(图3e)。这些结果表明,c-Myc在TME中通过CAR-NK细胞介导的ATP生成中发挥了关键作用。
Neo-2/15刺激的BBζ细胞的代谢特征
我们进一步对Neo-2/15与IL-2刺激的BBζ细胞进行了转录组分析,并在与AsPC-1细胞共培养后比较了两者的差异。基因本体富集分析(GO分析)显示,差异表达基因在代谢通路中存在显著差异,尤其是碳水化合物代谢、碳水化合物调节以及细胞因子和活性氧(ROS)通路(图3f)。此外,非靶向代谢组学分析显示,与IL-2刺激的BBζ细胞相比,Neo-2/15扩增的BBζ细胞中泛酸和CoA生物合成、AMPK信号通路、丙酮酸代谢和三羧酸循环(TCA cycle)是主要改变的通路(补充图5c)。此外,Neo-2/15扩增的BBζ细胞中与糖酵解和TCA循环相关的酶(如HK2、ALDOA、PGK1、ENO1、PKM、ACLY和SUCLG1)表达增加(补充图5d),并且代谢中间产物(如延胡索酸和F6P)以及线粒体呼吸链复合体(尤其是复合体I)的水平也显著升高(补充图5e、f)。
c-Myc在维持OXPHOS中的关键作用
TCA循环通过产生大量的NADH来促进线粒体氧化磷酸化(OXPHOS)从而生成ATP。我们通过测量细胞耗氧率(OCR)来评估OXPHOS水平。结果显示,与AsPC-1细胞共培养时,IL-2刺激的BBζ细胞的线粒体最大呼吸能力受损,而Neo-2/15刺激的BBζ细胞则未受影响(图3g和补充图5g)。此外,c-Myc抑制剂显著降低了Neo-2/15刺激的BBζ细胞的OXPHOS水平,伴随基础呼吸能力的显著下降(图3h和补充图5h)。这些数据表明,c-Myc在维持Neo-2/15刺激的BBζ细胞的OXPHOS以生成ATP中发挥了关键作用。
Neo-2/15对营养摄取和能量生成的影响
葡萄糖和谷氨酰胺是激活NK细胞中维持线粒体OXPHOS的关键燃料来源。我们进一步检测了葡萄糖和谷氨酰胺转运蛋白的表达。结果显示,Neo-2/15刺激的BBζ细胞中Glut1、ASCT2和SNAT1的表达增加,即使在与AsPC-1细胞共培养时也高于IL-2刺激的BBζ细胞(图3i和补充图6a)。一致地,抑制c-Myc或双重阻断STAT5和Akt显著降低了Neo-2/15刺激的BBζ细胞中这些转运蛋白的上调(图3j)。通过流式细胞术进一步确认了BBζ细胞中Glut1的表达变化(补充图6b、c)。综上所述,这些结果表明,Neo-2/15通过STAT5/Akt/c-Myc通路增强营养摄取和能量生成,从而在TME中增强BBζ细胞的细胞毒性(总结见补充图6d)。
Neo-2/15通过c-Myc维持CAR-NK细胞的线粒体功能
在肿瘤微环境(TME)中,Neo-2/15增强的CAR-NK细胞的线粒体功能如何维持是一个重要问题。我们首先通过MitoTracker染色检测了在肿瘤细胞存在的情况下NK细胞的线粒体质量。结果显示,与Neo-2/15处理的BBζ细胞相比,IL-2处理的BBζ细胞在与肿瘤细胞共培养时线粒体质量显著减少(图4a)。共聚焦激光扫描显微镜也观察到了类似的结果,显示Neo-2/15刺激的BBζ细胞的细胞质中存在大量线粒体(补充图7a)。
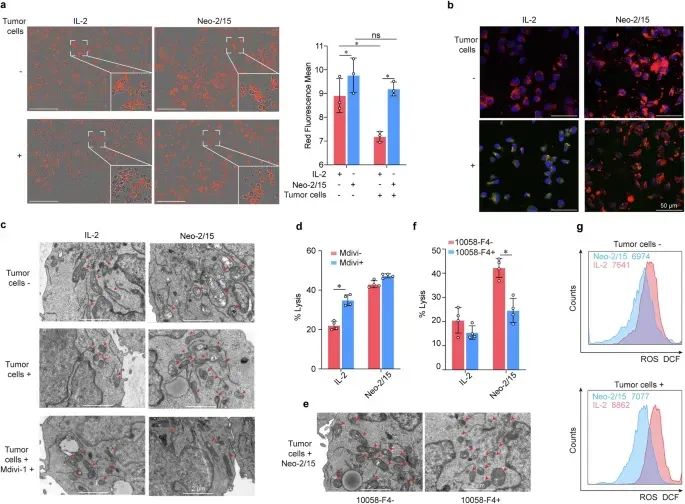
接下来,我们通过JC-1染色评估了线粒体膜电位的去极化情况。结果表明,在与肿瘤细胞共培养时,Neo-2/15而非IL-2能够维持BBζ细胞的线粒体膜电位(图4b和补充图7b)。此外,我们还通过透射电子显微镜(TEM)观察了线粒体形态。结果显示,Neo-2/15刺激的BBζ细胞的细胞质中线粒体保持完整,而IL-2刺激的BBζ细胞在与肿瘤细胞共培养时线粒体则呈现小而碎片化的形态(图4c)。线粒体分裂抑制剂Mdivi-1改善了IL-2刺激的BBζ细胞的线粒体形态,并增强了其杀伤肿瘤细胞的能力(图4c、d)。此外,c-Myc抑制剂预处理显著增加了Neo-2/15刺激的BBζ细胞的线粒体分裂,并降低了其细胞毒性活性(图4e、f)。相应地,在与肿瘤细胞共培养时,Neo-2/15刺激的BBζ细胞的线粒体活性氧(ROS)水平适度变化,而IL-2刺激的BBζ细胞的线粒体ROS水平显著增加(图4g)。这些结果表明,Neo-2/15能够在肿瘤细胞存在的情况下维持CAR-NK细胞的线粒体功能,而c-Myc在这一过程中发挥了重要作用。
eo-2/15通过c-Myc抵抗内质网应激诱导的凋亡,从而促进CAR-NK细胞在肿瘤内的持久性
肿瘤微环境(TME)引起的免疫抑制极化限制了CAR-NK细胞在体内的持久性。为了研究Neo-2/15对CAR-NK细胞持久性的影响,我们检测了来自荷瘤小鼠肿瘤组织中的BBζ和BBζ-Neo细胞的动力学变化(补充图8a)。结果显示,在AsPC-1异种移植瘤中,BBζ-Neo的数量显著高于BBζ(图5a和补充图8b),并且在外周血中BBζ-Neo的比例也高于BBζ(图5b)。此外,在卵巢癌异种移植模型的腹水中,BBζ-Neo的比例也高于BBζ(图5c和补充图8c)。
接下来,我们用丝裂霉素C处理Neo-2/15或IL-2刺激的BBζ细胞以诱导增殖停滞,然后将这些细胞注射到AsPC-1异种移植瘤中(图5d左)。免疫荧光(IF)分析显示,与IL-2相比,Neo-2/15显著提高了BBζ细胞在肿瘤组织中的持久性,尤其是在肿瘤内注射后72小时(图5d右和补充图8d)。这些数据表明,Neo-2/15能够促进CAR-NK细胞在TME中的持久性。
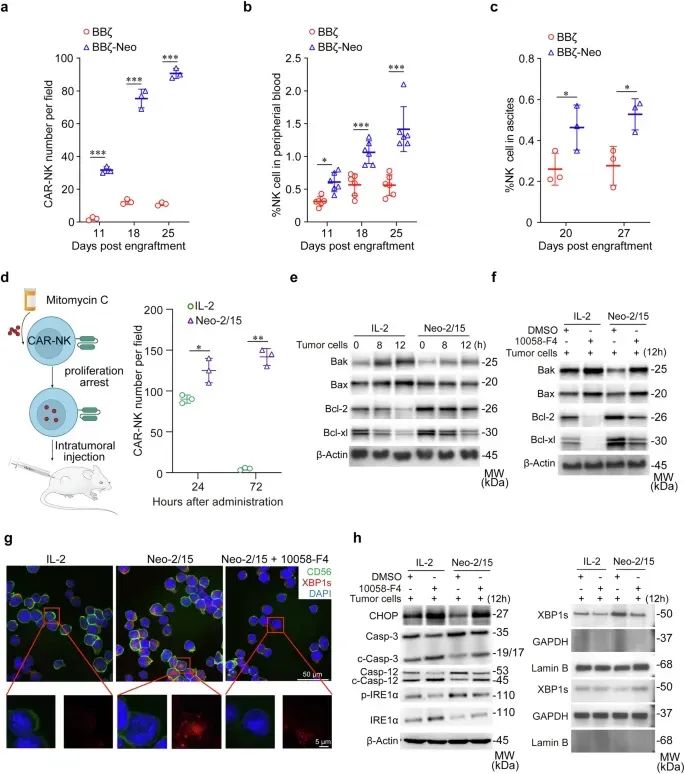
机制研究
从机制上讲,与IL-2处理相比,Neo-2/15刺激显著降低了与肿瘤细胞共培养的BBζ细胞中促凋亡蛋白Bax和Bak的水平,并增加了抗凋亡分子Bcl-2和Bcl-xl的水平(图5e)。正如预期的那样,c-Myc抑制剂消除了这种效应(图5f),表明Neo-2/15通过c-Myc在TME中维持BBζ细胞的抗凋亡表型。
此外,Neo-2/15显著促进了剪接型X盒结合蛋白1(XBP1s)向BBζ细胞核的转移,尤其是在与AsPC-1细胞共培养时(图5g)。Neo-2/15还下调了BBζ细胞中CHOP的表达以及caspase-3/12的裂解,但这些效应被c-Myc抑制剂阻断(图5h)。此外,c-Myc抑制剂消除了Neo-2/15诱导的肌醇需求酶1α(IRE1α)的磷酸化,并减少了XBP1s的核转移和表达,这与免疫荧光的结果一致(图5g、h)。
Neo-2/15通过c-Myc/NRF1增强CAR-NK细胞的ATP生成和抗肿瘤效果
为了进一步阐明XBP1s的核转移如何改善Neo-2/15刺激的BBζ细胞的功能,我们首先使用针对XBP1s的抗体进行了CUT&Tag实验。结果显示,在与AsPC-1细胞共培养时,XBP1s能够结合到Neo-2/15刺激的BBζ细胞中NRF1的开放染色质区域(图6a、b)。我们还发现,与IL-2处理的BBζ细胞相比,Neo-2/15处理的BBζ细胞中XBP1s和NRF1的表达显著上调,这一结果通过多色免疫荧光(IF)染色得到了证实(图6c)。此外,通过西方印迹和IF染色检测从异种移植瘤中浸润24小时后的BBζ细胞,结果显示Neo-2/15能够在TME中维持BBζ细胞中XBP1s和NRF1的表达,而IL-2则不能(图6d和补充图9a)。
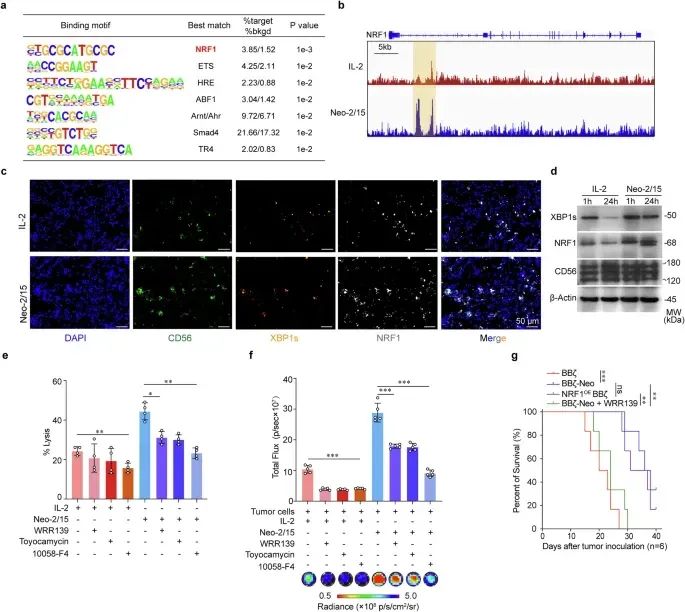
为了验证NRF1在BBζ细胞中的功能作用,我们在BBζ细胞中稳定过表达NRF1(NRF1OE BBζ)。结果显示,NRF1过表达增强了IL-2刺激的BBζ细胞的抗肿瘤效果,甚至超过了Neo-2/15刺激的BBζ细胞,这在体外(补充图9b)和体内(补充图9c)实验中均得到了证实,并伴随着ATP生成的增加(补充图9d)。相比之下,NRF1抑制剂WRR139、XBP1剪切抑制剂(Toyocamycin)和c-Myc抑制剂均削弱了BBζ-Neo细胞的细胞毒性(图6e)和ATP生成能力(图6f)。此外,NRF1抑制剂进一步增加了接受BBζ-Neo治疗的荷瘤小鼠的肿瘤负荷,并降低了其生存率(图6g和补充图9c)。
综上所述,这些结果表明Neo-2/15能够通过c-Myc/NRF1通路维持ATP生成,从而增强CAR-NK细胞的功能,提高其在实体瘤治疗中的疗效(补充图10)。
3 总结
CAR-NK细胞在肿瘤微环境(TME)中的浸润、活性和细胞毒性与实体瘤的清除密切相关。为了增强CAR-NK细胞在肿瘤组织中的积累,研究者通过基因改造宿主细胞使其分泌趋化因子,从而实现对实体瘤的消退。此外,CAR-NK细胞与表达细胞因子的溶瘤病毒联合使用已在胶质母细胞瘤中显示出强大的抗肿瘤效果。然而,维持CAR-NK细胞在TME中的功能仍然是一个重大挑战。研究表明,代谢状态的受损会导致CAR-NK细胞在肿瘤进展过程中抗肿瘤能力的下降。TME中营养物质的匮乏主要是由于髓系来源的抑制细胞(MDSC)和肿瘤细胞的存在导致供应不足,从而削弱了CAR-NK细胞的抗肿瘤能力和持久性。此外,TME中必需氨基酸的耗竭会诱导免疫细胞的无能,使其无法发挥细胞毒性作用。因此,建立能够在维持代谢健康的同时发挥效应功能的CAR-NK细胞对于实现对实体瘤的有效治疗至关重要。
本研究中,我们发现通过Neo-2/15增强的CAR-NK细胞在TME中具有更强的营养竞争力、更高的能量生成能力、更高的存活率和持久性。这些发现为代谢修饰在过继性细胞治疗中的有效性提供了有力证据。
细胞因子增强的CAR-NK细胞
细胞因子增强的CAR-NK细胞已被证明可以通过增强对免疫抑制极化的抵抗力来改善对实体瘤的治疗效果,从而促进抗肿瘤免疫反应。例如,IL-2、IL-15、IL-12、IL-21和IL-18等细胞因子已被用于增强NK细胞的增殖和活化,并被用于扩增原代NK细胞或增强记忆样NK细胞对血液系统恶性肿瘤的细胞毒性。然而,这些天然细胞因子诱导的NK细胞增殖通常受到限制。例如,IL-15虽然常用于支持NK细胞活化,但会导致人类NK细胞的功能耗竭。相比之下,Neo-2/15在诱导免疫治疗效果方面表现出较低的毒性,并且与天然IL-2R激动剂相比,其对IL-2Rβγ的亲和力更高,能够独立于IL-2Rα和IL-15Rα激活下游信号。我们之前的研究表明,经过改造以分泌Neo-2/15的饲养细胞在增强NK细胞增殖和功能方面具有显著潜力。
Neo-2/15对CAR-NK细胞代谢的影响
我们的研究揭示了Neo-2/15能够维持NK细胞在TME中的STAT5/Akt信号通路,并保持下游c-Myc的表达。Neo-2/15扩增的CAR-NK细胞增加了营养转运蛋白的表达、线粒体OXPHOS速率和ATP生成,从而抵抗TME免疫抑制诱导的功能障碍,展现出更强的细胞毒性、更少的耗竭和在TME中更长的持久性,从而提高了胰腺癌和卵巢癌的治疗效果。
线粒体健康与能量代谢
线粒体质量的维持对于OXPHOS、最大呼吸能力和线粒体融合至关重要,无论细胞类型如何,线粒体融合都能增加能量生成以应对压力。线粒体质量调节CD8+ T细胞的命运决定、抗肿瘤免疫、记忆形成和代谢健康。从肝癌肿瘤浸润性淋巴细胞中分离的耗竭NK细胞主要具有碎片化和明显的线粒体,伴随细胞毒性降低。OXPHOS在淋巴细胞中增加了线粒体健康,从而在TME中实现抗凋亡和细胞持久性。此外,线粒体碎片化会导致细胞功能障碍,敲除与线粒体融合相关的基因可以不可逆地阻断癌干细胞的永生化并抑制肿瘤形成。因此,线粒体健康和能量生成与免疫细胞和癌细胞的命运密切相关。目前,关于NK细胞线粒体状态、动态调节和NK细胞介导的免疫监视之间关系的研究较少。目前,使用线粒体分裂抑制剂(如Mdivi-1)或敲除线粒体分裂基因的方法被用于恢复NK细胞的线粒体形态和杀伤功能。我们的研究结果表明,Neo-2/15可以在TME中维持线粒体健康,从而增加能量生成和抗凋亡能力。我们证实,Neo-2/15维持线粒体健康的机制部分依赖于c-Myc的上调。当c-Myc被化学抑制时,Neo-2/15增强的CAR-NK细胞表现出线粒体分裂、OXPHOS降低和ATP生成减少,导致抗凋亡表型减弱和抗肿瘤效果失败。这些结果为优化工程化NK细胞的代谢以增强其在荷瘤宿主中的抗肿瘤效果提供了证据。
c-Myc和NRF1在调节线粒体功能中的作用
c-Myc已被证明对线粒体基因表达和生物合成至关重要。此外,IRE1α-XBP1通路在体内驱动NK细胞对肿瘤的反应。我们发现,在Neo-2/15刺激的CAR-NK细胞中,IRE1α和XBP1s上调,且XBP1s转移到细胞核中,而这些效应在c-Myc被抑制时减弱。我们进一步证实,NRF1是Neo-2/15处理的CAR-NK细胞中XBP1s介导的基因表达的主要转录靶点,通过增强细胞毒性在体内和体外发挥作用。NRF1通过诱导与线粒体功能相关的多种基因的转录来影响细胞代谢,尤其是在细胞呼吸、ATP合成和抗氧化防御方面,这些基因在肝细胞等多种细胞类型中至关重要。我们的结果还表明,NRF1过表达增强了IL-2刺激的BBζ细胞的抗肿瘤效果和ATP生成,而NRF1和c-Myc抑制剂则削弱了BBζ-Neo的细胞毒性。NRF1的抑制导致CAR-NK细胞中ATP生成显著减少,以及接受BBζ-Neo治疗的荷瘤小鼠的存活率下降。因此,我们推测具有充足能量的效应细胞可以在TME中逃避凋亡,并最佳地发挥其细胞毒性功能。
结论
这些研究结果强调了通过Neo-2/15优化治疗性NK细胞代谢以改善其在代谢不利的TME中的功能,可能为对抗实体瘤免疫抑制极化的NK细胞活性代谢修饰提供一种潜在的通用策略。
原文链接:https://www.nature.com/articles/s41392-025-02158-2


