Cell子刊:南方医科大学龚神海/陈鹏/赵晓山/曾振华发现肠道细菌代谢物可缓解对乙酰氨基酚过量引起药物性肝损伤
时间:2023-04-27 08:22:52 热度:37.1℃ 作者:网络
对乙酰氨基酚(APAP)过量是药物性肝损伤(DILI)的主要原因。肠道菌群和相关代谢物对APAP和肝功能的影响尚不清楚。
2023年4月25日,南方医科大学龚神海、陈鹏、赵晓山和曾振华团队在Cell Host & Microbe在线发表了题为“Liberation of daidzein by gut microbial β-galactosidase suppresses acetaminophen-induced hepatotoxicity in mice”的研究论文,该研究发现APAP紊乱与一个独特的肠道微生物群落有关,阴道乳杆菌显著减少。研究结果显示由于阴道乳杆菌β-半乳糖苷酶能从日常食物中释放异黄酮黄豆苷元(Daidzein),接受阴道乳杆菌的小鼠表现出对APAP肝毒性的抗性,而β-半乳糖苷酶抑制剂可消除阴道乳杆菌对APAP暴露无菌小鼠的肝保护作用。
在APAP处理的小鼠中,缺乏β-半乳糖苷酶的阴道乳杆菌比野生型菌株产生更差的结果,但这些差异通过给药黄豆苷元被克服。从机制上讲,黄豆苷元可以防止铁死亡,这与降低Fdps的表达有关,Fdps激活了AKT-GSK3β-Nrf2的关键铁致死亡途径。该研究结果显示阴道乳杆菌β-半乳糖苷酶释放黄豆苷元能抑制Fdps介导的肝细胞铁死亡,该研究为DILI提供了潜在的治疗方法。

多种免疫和代谢性疾病可表现为急性肝衰竭(ALF),但ALF的主要触发因素是药物性肝损伤(DILI)。在美国,对乙酰氨基酚(APAP)过量服用是大约50%的临床ALF的原因。在治疗剂量下,APAP主要通过硫代转移酶和葡萄糖醛酸转移酶代谢成稳定的化合物,然后通过胆汁和尿液排出。如果这一代谢途径被阻断,APAP的一部分被细胞色素p450 2E1 (CYP2E1)转化为n -乙酰基-对苯醌亚胺(NAPQI),这是一种高活性和毒性的中间代谢物。一部分NAPQI通过与谷胱甘肽(GSH)结合迅速解毒,而过量未结合的NAPQI与线粒体蛋白共价结合产生APAP蛋白复合物,最终导致氧化应激增强和线粒体功能障碍,甚至并发肝细胞死亡。
肠-肝轴是肠道微生物群与宿主肝脏之间的相互作用。例如,微生物来源的格拉司琼有效地下调了败血症引起的肝损伤的易感性。微生物衍生的代谢物1-苯基-1,2-丙二酮通过消耗肝脏GSH介导APAP诱导产生节律性肝损伤。除了肠道细菌直接产生的代谢物外,微生物酶从饮食中释放的生物活性化合物在调节疾病易感性方面也起着重要作用。确定肠道微生物群从饮食中释放出类似的益生素有助于制定改善健康的策略。
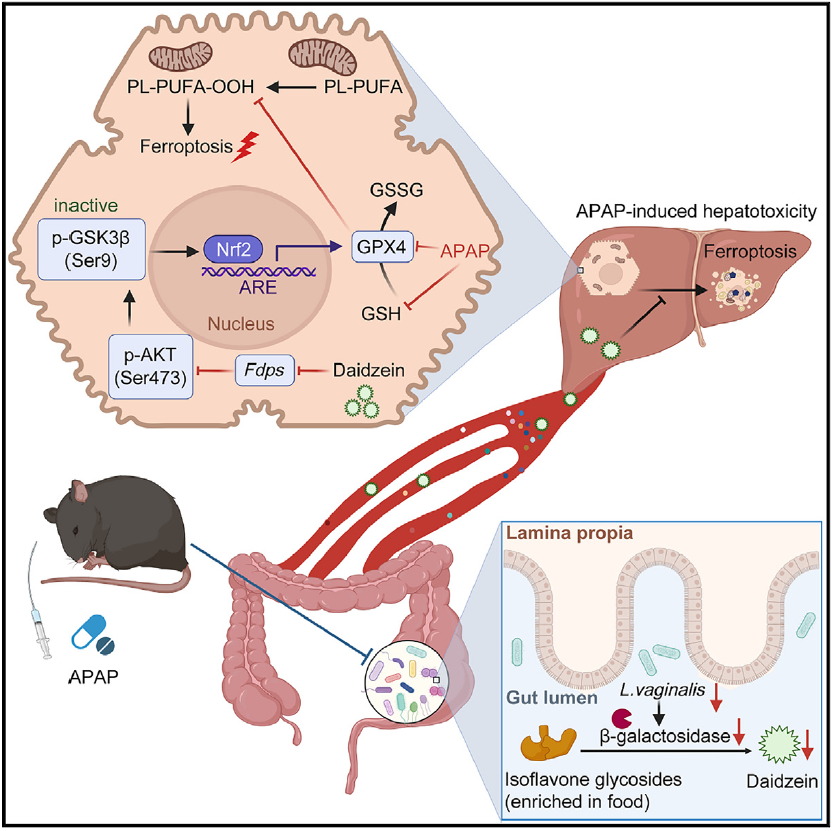
文章模式图(图源自Cell Host & Microbe )
一项流行病学研究发现,大豆食品的高摄入量与肝脏疾病的患病率呈负相关。大豆食品含有多种营养成分,包括异黄酮。天然形式的大豆异黄酮主要以糖苷的形式存在。因此,大豆异黄酮在小鼠体内的口服吸收和生物利用度是有限的。肠道菌群在膳食类黄酮的代谢中起着关键作用。在肠道异黄酮水解过程中,游离形式的苷元可由微生物的β-葡萄糖苷酶或β-半乳糖苷酶释放。苷元主要包括genistein(GEN)、黄豆苷元(DA)和glycitein (GLY),具有较高的生物利用度。因此,可认为大豆食品中释放的异黄酮苷元是潜在的益生素,其在DILI中的有效性有待进一步研究。
铁死亡是由铁依赖的脂质过氧化作用驱动的,被认为是DILI的中心细胞事件。核因子-红细胞2相关因子2 (Nrf2)被认为是抗氧化系统的主要调节因子,可防止脂质过氧化和铁死亡。作为Nrf2的上游组分,糖原合成酶激酶3β (GSK-3β)磷酸化(失活状态)受到AKT(蛋白激酶B)磷酸化的正调控,提示AKT- GSK3 β-Nrf2信号轴参与铁凋亡。Fdps通过破坏破骨细胞中的蛋白烯酰化被认为是治疗骨质疏松症的有效靶点;然而,对Fdps在调节肝细胞凋亡依赖性DILI中的作用缺乏深入的了解。
该研究旨在探讨肠道微生物来源的益生菌与宿主肝脏生理之间的相互作用。该研究证明了肠道菌群失调放大了APAP处理小鼠的肝毒性,通过Fdps介导的肝细胞铁死亡,这是由于通过阴道乳杆菌的β-半乳糖苷酶从饮食中释放的DA减少,从而揭示了DILI治疗的治疗方法。
原文链接:
https://www.cell.com/cell-host-microbe/fulltext/S1931-3128(23)00146-4#%20


