Alzheimer Dementia- 血液中特定蛋白组合,可有效预测大脑淀粉样蛋白
时间:2021-06-30 07:02:15 热度:37.1℃ 作者:网络

在阿尔茨海默病(AD)中,潜在的大脑淀粉样β(Aβ)和tau病变以及随之而来的神经退行性可以用脑脊液(CSF)和成像生物标志物进行可靠的检测和监测。CSF中Aβ42(单独或与Aβ40的比率)和磷酸化tau(p-tau)的浓度反映了AD相关的Aβ和tau在大脑中的代谢变化。Aβ和tau的正电子发射断层扫描(PET)被用来测量Aβ斑块负荷和不溶性配对螺旋丝(PHF)tau聚集物。
神经变性(由于AD或其他原因)的生物标志物包括氟脱氧葡萄糖(FDG)PET、磁共振成像(MRI)和CSF神经丝蛋白(NfL)。CSF和成像生物标志物已经被纳入ATN(淀粉样蛋白、tau、神经变性)分类系统,这是美国国家老龄化研究所为诊断AD提出的研究框架。然而,为了在临床试验中广泛适用,以及未来在常规临床护理中的实施,需要更容易获得和便宜的方法,如血液测试。血液中的AD生物标志物浓度很低,使得在其他高丰度蛋白质存在的情况下对其进行量化具有挑战性。然而,最近在质谱和免疫检测方面的技术进步导致了新方法的发展,使血液中的Aβ42/Aβ40、p-tau和NfL得到可靠的评估。
血液中的Aβ42/Aβ40与CSF Aβ42/Aβ40和Aβ-PET相关,可以相对准确地识别出脑部Aβ负担异常的人或那些未来转换为Aβ-PET阳性的高风险人群。当在血浆中测量时,在苏氨酸217和181处磷酸化的tau(p-tau217和p-tau181)可准确检测PET评估的淀粉样和tau病理学,区分AD与非AD神经变性疾病,并预测未来发展为AD痴呆。p-tau217的血浆水平已被证明在AD的早期临床前阶段增加,并随着时间的推移在临床前和前驱AD患者中继续增加。在散发性疾病的轻度认知障碍(MCI)和AD痴呆阶段,以及在家族性AD的无症状阶段,也有血液NfL水平升高的报道,并随着时间的推移与其他神经变性的迹象同步增加。然而,NfL不是AD神经变性的特异性指标,而是在许多其他中枢神经系统疾病中增加(在CSF和血液中),例如包括额颞叶痴呆、进行性核上性麻痹、皮质基质综合征、肌萎缩性侧索硬化症和克雅氏病。
血浆生物标志物有可能大大加快AD有效疾病修改疗法的发展,因为它有助于识别处于疾病早期阶段的人(即临床前或前驱AD的受试者),此时治疗最有可能成功。尽管血浆AD生物标志物在检测Aβ病理方面显示出相对公平的准确性,但将这些生物标志物结合在一起的血液测试是否能提供更好的性能仍有待确定。
例如,AD的血浆Aβ水平的下降是非常温和的(最多15%-20%),而血浆p-tau是一个更动态的生物标志物,可以更好地反映大脑Aβ负担的逐渐增加。同时,由于AD的生物标志物遵循不同的轨迹,Aβ42/Aβ40首先开始变化,其次是p-tau,然后是NfL,因此在疾病的早期阶段,血液Aβ42/Aβ40很可能是最准确的。
藉此,瑞典隆德大学的Shorena Janelidze等人,在两个独立的认知障碍(CU)参与者(n = 591)和MCI患者(n = 304)队列中测量了血浆Aβ42/Aβ40、血浆p-tau217和血浆NfL。
他们首先评估了单个生物标志物的准确性,然后评估了不同生物标志物组合的准确性,以分别检测CU受试者和MCI患者的大脑Aβ异常状态(使用CSF Aβ42/Aβ40或Aβ-PET定义)。最后,测试了包括受检者的脂蛋白E(APOE)ε4状态信息是否提高了准确性。
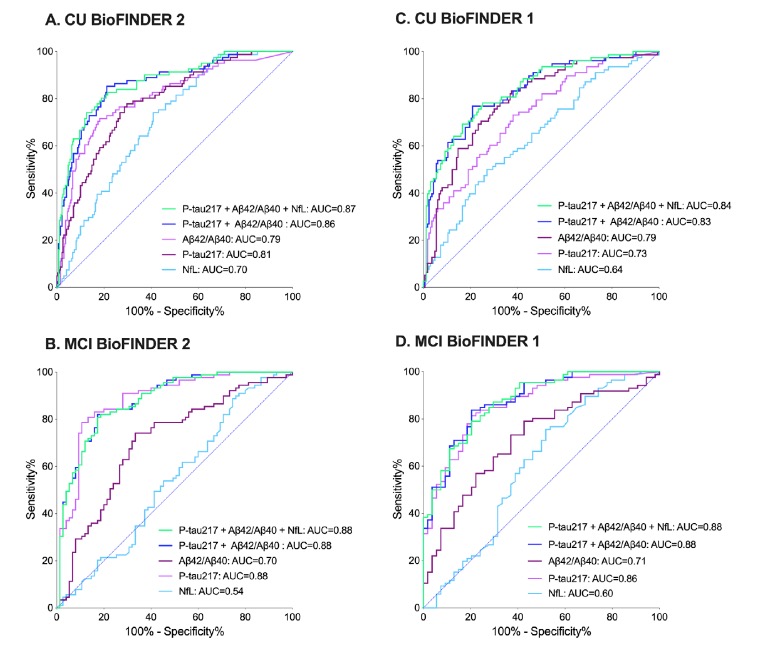
他们发现:在CU中,血浆Aβ42/Aβ40和p-tau217的组合可以检测到异常的脑Aβ状态,曲线下面积(AUC)为0.83至0.86。
在MCI中,包括p-tau217单独或Aβ42/Aβ40和p-tau217的模型具有相似的AUC(0.86-0.88);然而,后者显示出更好的模型拟合。目前他们已将这个预测模型,做成网页版预测工具:https://brainapps.shinyapps.io/PredictABplasma/。
这个研究的重要意义在于,发现了血浆Aβ42/Aβ40和p-tau217的组合能以相对较高的准确度区分Aβ状态,而p-tau217在MCI中显示出与Aβ病理的最强关联,但在CU中却不是。
原文出处:
Janelidze S, Palmqvist S, Leuzy A, Stomrud E, Verberk IMW, Zetterberg H, Ashton NJ, Pesini P, Sarasa L, Allué JA, Teunissen CE, Dage JL, Blennow K, Mattsson-Carlgren N, Hansson O. Detecting amyloid positivity in early Alzheimer's disease using combinations of plasma Aβ42/Aβ40 and p-tau. Alzheimers Dement. 2021 Jun 20. doi: 10.1002/alz.12395. Epub ahead of print. PMID: 34151519.


