Front Immunol:肥胖和2型糖尿病患者IL-36水平升高通过诱导脂肪细胞和巨噬细胞自身表达和释放促进脂肪组织炎症
时间:2022-03-11 11:22:59 热度:37.1℃ 作者:网络

肥胖被定义为功能失调的脂肪组织(AT)的过度堆积,是一种主要的全球流行病,导致重要的生理和代谢相关功能障碍,包括2型糖尿病(T2D)、心血管疾病和癌症。随着这一公共健康问题的日益普遍,人们现在认识到,脂肪组织(AT)质量增大,加上血管形成不足、缺氧、巨噬细胞浸润、低度炎症和/或纤维化,都会导致肥胖的许多并发症的发生。额外的复杂性是由于AT驻留免疫细胞的失调,这是通过调节炎症和新陈代谢来维持AT动态平衡的关键。肥胖的全身性和慢性炎症反应的特征是脂肪细胞或免疫细胞(主要是巨噬细胞)浸润的脂肪细胞或免疫细胞释放细胞因子、白细胞介素(IL)和脂肪因子的改变。
白细胞介素-36(IL-36)是近年来发现的一种细胞因子,在多种炎症性疾病的调节中具有重要作用。由于目前还没有关于这种细胞因子如何调节AT稳态的数据,我们的目标是探索一种特殊的亚型,IL-36g,一种激动剂,在人类肥胖和肥胖相关的2型糖尿病以及AT炎症和纤维化中的作用。
在一项病例对照研究中,对91名参与者的血浆IL-36g进行了测定,并对31例接受减肥手术的严重肥胖症患者的减肥效果进行了评估。分析IL36G及其受体在人体相关代谢组织中的基因表达水平。体外测定炎症因子和IL-36G对人脂肪细胞和巨噬细胞的影响。
首次发现肥胖患者经Roux-en-Y胃分流术减肥后,循环中升高的IL-36g水平降低(P<0.001),内脏AT和外周血单个核细胞IL-36G基因表达水平上调(P<0.05)。我们还发现饮食诱导的肥胖小鼠附睾AT中IL36g的表达水平增加(P<0.05)。脂多糖可显著增强人脂肪细胞和单核巨噬细胞的IL36G(P<0.001),而与抗炎细胞因子孵育后IL36G无明显变化。加入IL-36g 24h后,IL-36g自身表达增强(P<0.01),主要炎症和趋化因子表达增强(P<0.01),而肝纤维化相关基因无明显变化。此外,肥胖患者脂肪细胞条件培养液还能增加单核巨噬细胞IL-36g的释放(P<0.01)和组织蛋白酶G(CTSG)的表达(P<0.05)。

图1|肥胖及其相关的T2D对IL-36G水平的影响。手术减肥的效果。(A)正常体重(NW)志愿者(n=18)、肥胖(OB)患者(n=32)和糖耐量受损/2型糖尿病(IGTT2D)患者(n=41)的空腹血浆IL-36g浓度;(B)肥胖者(n=31)Roux-en-Y胃分流术减肥前后血浆IL-36g浓度的比较。(C,D)条形图显示NW志愿者(n=6)、OB-NG(n=23)和OB-T2D(n=15)患者内脏脂肪组织(VAT)中IL36G和IL36R的mRNA水平,以及T2D患者(n=6)和非T2D患者(n=8)的脂肪细胞(n=11-13)和间质血管部分细胞(SVFC)(n=8)中IL36G和IL36R的mRNA水平。(E)检测正常对照组(n=20)、OB-NG组(n=16)和OB-T2D组(n=18-25)外周血单个核细胞(PBMC)中IL-36G和IL-36R的基因表达水平,以及按IGT-T2D阳性和阴性分为33例和28例的OB患者肝组织中IL36G和IL36R的基因表达水平。条形代表平均值±扫描电镜。在适当的情况下,用单因素方差分析(One-way ANOVA)和图基检验(Tukey‘s test)以及未配对和配对的双尾学生t检验来分析各组之间的差异。*P<0.001,**P<0.01,*P<0.05。

图2|炎症相关因子对IL36G和IL36R基因表达水平的影响。条形图显示(A,B)LPS,(C,D)TNF-α,(E,F)IL-4和(G,H)IL-13孵育24小时对人分化内脏脂肪细胞和单核细胞来源的巨噬细胞IL 36G和IL 36R转录水平的影响。未刺激细胞的基因表达水平假设为1,取值为平均值±扫描电镜(n=4-7)。组间差异分析采用单因素方差分析和Dunnetts‘s检验。*P<0.001,**P<0.01,*P<0.05。
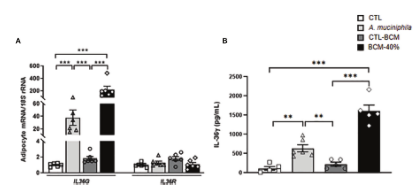
图3|(A)内脏脂肪细胞IL-36G和IL-36R的基因表达水平以及(B)与粘液阿克曼氏菌或细菌条件培养基(BCM)孵育后内脏脂肪细胞释放IL-36G的情况。条形图表示平均值±SEM。组间差异分析采用单因素方差分析,随后进行图基后检验。**P<0.01和*P<0.001,每组5~6例。

图4|脂肪细胞条件培养液(ACM)对单核细胞来源的巨噬细胞的影响。条形图显示孵育24小时的肥胖者ACM(20%和40%)对(A)IL36G、IL36R和CTSG转录水平的影响以及(B)ACM治疗后IL-36G分泌水平的影响。取值为平均±扫描电镜(n=5~6)。组间差异分析采用单因素方差分析,然后进行图基检验。*P<0.05和**P<0.01。(n=5~6个/组)。
这些发现首次为IL-36g在调节AT慢性炎症中的特性提供了证据,成为AT生物学和肥胖相关合并症之间的联系。
原文出处:Frühbeck G, Gómez-Ambrosi J, Ramírez B, et al.Increased Levels of Interleukin-36 in Obesity and Type 2 Diabetes Fuel Adipose Tissue Inflammation by Inducing Its Own Expression and Release by Adipocytes and Macrophages.Front Immunol 2022;13


