Molecular Neurodegeneration:油酰乙醇酰胺促进阿尔茨海默病小鼠模型中的 PPARα 和 TFEB 信号传导并减弱 Aβ 病理学
时间:2023-09-02 14:00:11 热度:37.1℃ 作者:网络
阿尔茨海默病(AD)是最常见的与年龄相关的神经退行性疾病,其特征是淀粉样β(Aβ)斑块和神经原纤维缠结的积累。这些病理特征伴随着大脑中神经胶质细胞的显著变化。全基因组关联研究表明小胶质细胞及其相关途径(例如内吞作用和吞噬作用、脂质代谢和免疫反应)在迟发性 AD 的病因学中发挥着重要作用。
除了遗传证据外,年龄也是最大的风险因素。年龄影响的潜在机制可能很复杂,因为已知衰老会引起细胞、细胞器和系统水平的多种变化。因此,延缓衰老和促进长寿的化合物可能被证明可以有效对抗AD。

油酰乙醇酰胺 (OEA) 是一种进化上保守的内源性脂质,已被证明可以通过溶酶体到细胞核的信号传导和代谢基因表达的激活来延长线虫的寿命和健康寿命。在哺乳动物系统中,OEA 在外周组织和中枢神经系统 (CNS) 中产生。有趣的是,最近的一项脂质组学分析发现,与非痴呆对照相比,OEA 和其他脂肪酸乙醇酰胺是 AD 患者脑脊髓液和血浆中下调的脂质类别,这提高了 OEA 和相关脂质可能影响 AD 进展的可能性它们的循环水平可以作为有用的生物标志物。
OEA 在摄食调节中的作用归因于它与过氧化物酶体增殖物激活受体 α (PPARα) 的结合,这是一种配体激活的核受体,在与类视黄醇 X 受体 (RXR) 二聚化后,充当有效的转录因子,可激活参与能量稳态、脂质代谢、自噬和炎症的下游靶标。除 PPARα 外,还有两种 PPAR 亚型:PPARβ/δ 和 PPARγ。它们在外周组织和中枢神经系统中表达。
通过类似的信号传导机制,PPAR 在细胞代谢中发挥着关键作用,其失调与多种疾病有关,如 2 型糖尿病、癌症和阿尔茨海默氏病。合成 PPARα 激动剂已被证明通过作用于 APP 加工和 Aβ 代谢、自噬和溶酶体途径、脂质过氧化 和神经炎症在 AD 小鼠模型中提供有益作用。PPARα 可能通过与 PPARβ/δ 和 PPARγ 的串扰发挥作用或与其他转录因子,其中包括转录因子 EB (TFEB)。
TFEB 是自噬和溶酶体生物合成的主要调节因子,可通过 mTOR 依赖性磷酸化和核信号传导协调溶酶体营养状态 。研究人员报道了 TFEB 通过自噬-溶酶体途径和吞噬作用在减轻 Aβ 和 tau病理学方面的有效作用,PPARα 和 TFEB 具有复杂的调控网络,其中它们共享上游诱导物和下游靶点。Raha 等人报道了星形细胞 PPARα-TFEB 通路调节 Aβ 清除。然而,人们对 OEA 在生理和疾病条件下大脑中可能发挥的作用知之甚少。
OEA 是一种脂质酰胺,可以被脂肪酸酰胺水解酶(FAAH)水解。为了提高 OEA 的稳定性,Astarita 等人。开发了一种类似物 KDS-5104,它是 OEA 的功能模拟物,并且能抵抗酶水解。使用当前研究中的类似物,2023年8月15日发表在Molecular Neurodegeneration的文章,证明 OEA/KDS-5104 激活 PPARα 下游靶点 CD36 以增强吞噬作用,并激活 TFEB 以促进溶酶体清除,后者是 mTOR 独立的。
这些协同活动导致小胶质细胞 Aβ 和脂质的有效吸收和清除,并抑制 LPS 诱导的炎症小体激活。对 AD 的 5xFAD 小鼠模型施用 KDS-5104 可逆转脂质谱的改变以及大脑中小胶质细胞和星形胶质细胞的反应性。这些变化伴随着 AD 模型中 Aβ 病理学的减弱、突触完整性和认知功能的改善。
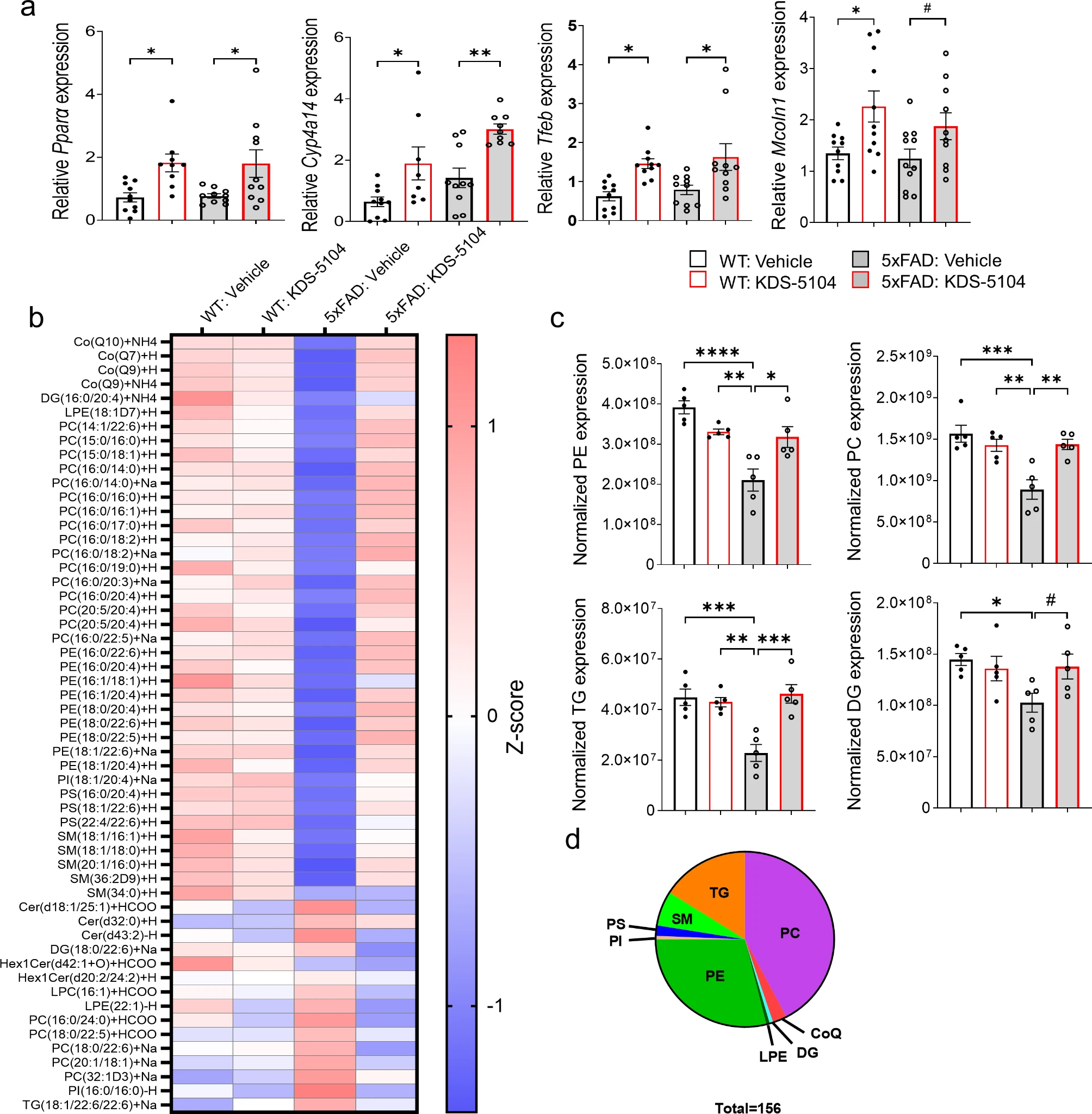
KDS-5104 治疗逆转了 5xFAD 小鼠的脂质失调
研究人员使用原代小胶质细胞培养物以及遗传和药理学方法来检查 OEA 在介导 Aβ 吞噬和清除、脂质代谢和炎性体形成中的信号传导机制和功能作用。此外,本文还通过对 5xFAD 小鼠进行长期治疗,测试了 OEA 在体内对急性 LPS 诱导的神经炎症的影响。
研究结果显示,OEA 激活 PPARα 信号传导及其下游细胞表面受体 CD36 活性。此外,OEA 以 PPARα 依赖性但 mTORC1 独立的方式促进 TFEB 溶酶体功能,两者的结合导致小胶质细胞 Aβ 的摄取和清除增强。这些与抑制 LPS 诱导的脂滴积累和炎症小体激活有关。用 KDS-5104 对 5xFAD 小鼠进行长期治疗,可恢复失调的脂质分布,减少反应性神经胶质增生和 Aβ 病理,并挽救认知障碍。

用 KDS-5104 治疗的 5xFAD 小鼠的反应性神经胶质增生和 Aβ 病理减少
衰老是 AD 的最大危险因素。因此,改善健康衰老的药物可能有助于预防或延缓 AD。本文提供的证据表明 OEA 可能代表这种化合物。它对 AD 患者血浆和脑脊液的减少提供了进一步的疾病相关性。OEA 增强作为一种治疗策略具有几个有吸引力的特点:首先,它增强了内源性脂质信号通路;其次,它针对两个具有治疗潜力的分子,PPARα和TFEB,而后者是mTORC1独立的;最后,OEA 相对安全,并且作为营养保健品进行销售。因此,本研究呼吁进一步开发 OEA 类似物作为衰老和 AD 的潜在疗法。
原文出处
Comerota, M.M., Gedam, M., Xiong, W. et al. Oleoylethanolamide facilitates PPARα and TFEB signaling and attenuates Aβ pathology in a mouse model of Alzheimer’s disease. Mol Neurodegeneration 18, 56 (2023). https://doi.org/10.1186/s13024-023-00648-x


