国际会议 | 2023 ESMO:乳腺癌LBA重点研究盘点!
时间:2023-10-31 14:42:34 热度:37.1℃ 作者:网络
前言
2023年欧洲肿瘤内科学会(ESMO)年会将于欧洲中部夏令时间10月20日-24日在西班牙马德里召开,届时将公布众多领域前沿进展和重磅研究成果。
目前ESMO官网在线发布了入选研究的常规摘要和LBA,而LBA研究作为所有研究的重中之重,可能对临床实践产生重大影响。e路新干线小编第一时间整理乳腺癌药物治疗LBA重点研究,供各位医学同道参考。
1 早期乳腺癌
摘要号:LBA 17
monarchE研究预计划的OS期中分析结果进一步支持阿贝西利联合内分泌疗法治疗HR阳性、HER2阴性高危早期乳腺癌患者
题目:阿贝西利联合内分泌疗法辅助治疗HR阳性、HER2阴性高危早期乳腺癌:monarchE研究预先计划的OS期中分析结果,包括5年疗效结果
报告人:Nadia Harbeck
背景
2年阿贝西利联合内分泌治疗(ET)辅助治疗HR阳性、HER2阴性、淋巴结阳性、高危早期乳腺癌患者的无侵袭性疾病生存期(IDFS)和无远端复发生存期(DRFS)持续显著改善。在此,我们报告了预先设定的OS期中分析的5年疗效结果。
方法
患者随机(1:1)接受至少5年ET+/-2年阿贝西利治疗。高危早期乳腺癌被定义为≥4枚腋窝淋巴结(ALN)阳性或1-3枚ALN阳性并伴有3期疾病和/或肿瘤≥5 cm(队列1)。纳入更少的患者人群为1-3枚 ALN阳性和中心测定的Ki-67≥20%(队列2)。意向治疗(ITT)人群包括队列1(5120例患者)和队列2(517例患者)。测定ITT人群的OS是否具有统计学意义。采用Cox比例风险模型估计风险比(HR)。
结果
在ITT人群中,中位随访时间为54个月,阿贝西利持续获益,IDFS的HR为0.680(95% CI:0.599,0.772),DRFS的HR为0.675(95% CI:0.588,0.774)。阿贝西利的持续获益意味着KM曲线的持续分离,5年IDFS和DRFS率绝对改善分别为7.6%和6.7%,而4年IDFS和DRFS率绝对改善分别为6.0%和5.3%,3年IDFS和DRFS率绝对改善分别为4.8%和4.1%。队列1治疗期间的获益与ITT人群一致。没有观察到新的安全信号。阿贝西利联合ET组的死亡人数相比于ET组持续更少(208 vs. 234;HR,0.903;p=0.284),未达到显著性。
结论
在预先计划的期中分析中,阿贝西利联合ET在治疗完成后继续降低侵袭性和远端疾病复发的风险,5年的绝对改善增加与延滞效应一致,该数据进一步支持在高危早期乳腺癌患者中使用阿贝西利。OS数据正在朝着有利于阿贝西利的方向发展,随访仍在继续。
摘要号:LBA 23
NATALEE研究的关键亚组分析结果进一步支持瑞波西利联合NSAI治疗HR阳性、HER2阴性早期乳腺癌患者
题目:Ⅲ期NATALEE研究的关键亚组分析:瑞波西利+NSAI治疗HR阳性、HER2阴性早期乳腺癌患者的IDFS
报告人:Aditya Bardia
背景
NATALEE研究表明,在Ⅱ或Ⅲ期HR阳性、HER2阴性早期乳腺癌复发风险人群中,瑞波西利(RIB)+NSAI相比于单独NSAI的IDFS获益具有统计学意义(Slamon D, et al. ASCO 2023. Oral LBA500)。评估临床相关亚组的IDFS预后对于了解特定患者的治疗获益非常重要。在此,我们报告了一个NATALEE研究预先设定的探索性亚组分析患者的iDFS。
方法
HR阳性、HER2阴性早期乳腺癌患者随机1:1接受RIB 3年(400 mg/d 用3周停1周)+NSAI≥5年(来曲唑2.5 mg/d或阿那曲唑1 mg/d)或NSAI。绝经前女性和男性每28天接受戈舍瑞林治疗。根据AJCC的癌症分期手册(第8版),NATALEE研究包括ⅡA期患者(有额外危险因素的N0或N1 [1-3枚腋窝淋巴结])和所有ⅡB期及Ⅲ期患者。采用Kaplan-Meier法评估iDFS。根据解剖分期、绝经状态、淋巴结状态、年龄、Ki-67评分(当地检测)进行IDFS分析。这种预先确定的分析没有统计学意义。
结果
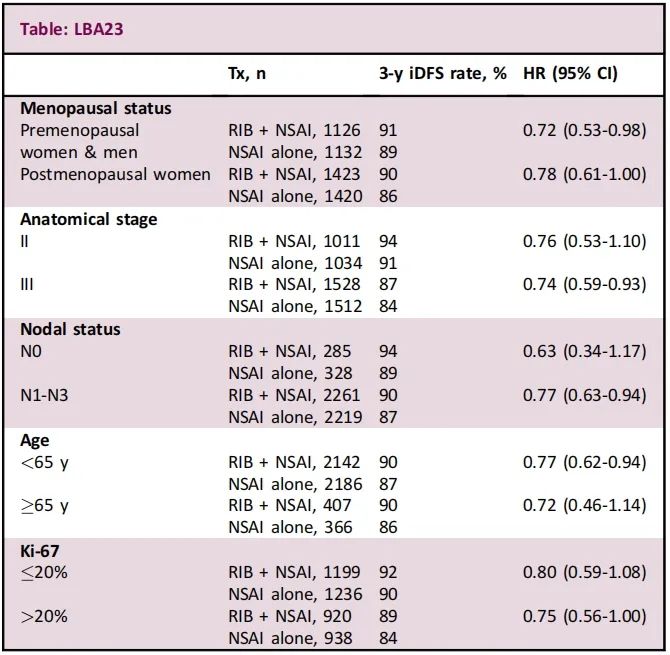
共纳入5101例患者(数据截止日期:2023年1月11日;IDFS的中位随访时间:27.7个月)。总的来说,与单独使用NSAI相比,RIB + NSAI的IDFS获益在所有临床相关亚组中都是一致的(表1),同时与总体试验人群中观察到的结果一致。
表1:NATALEE研究中各亚组3年IDFS率
结论
RIB + NSAI的IDFS获益与NATALEE研究的意向治疗人群基本一致,而不是由任何特定的亚组驱动的。该结果进一步支持了RIB + NSAI作为HR阳性、HER2阴性早期乳腺癌患者的一种新的治疗选择。
摘要号:LBA 20
CheckMate 7FL研究达到主要终点:纳武利尤单抗+NACT/ET+纳武利尤单抗治疗高危、ER阳性、HER2阴性原发乳腺癌患者pCR率显著改善
题目:一项随机、双盲研究:纳武利尤单抗 vs. 安慰剂联合新辅助化疗序贯内分泌治疗±纳武利尤单抗辅助治疗高危、ER阳性、HER2阴性原发乳腺癌
报告人:Sherene Loi
背景
高危、早期ER阳性、HER2阴性乳腺癌治疗包括新辅助化疗(NACT)和辅助内分泌治疗(ET)。CheckMate 7FL(CM-7FL;NCT04109066)是第一个前瞻性、Ⅲ期随机试验,研究纳武利尤单抗(NIVO) vs. 安慰剂(PBO)联合NACT序贯ET±NIVO辅助治疗高危、ER阳性、HER2阴性原发乳腺癌。
方法
本研究纳入了新诊断的ER阳性、HER2阴性乳腺癌患者,分期为:T1c-2 N1-2或T3-4 N0-2的2级(ER 1-10%)或3级(ER≥1%)疾病。患者随机按1:1分为NACT + NIVO 360 mg Q3W/NIVO 240 mg Q2W(A组)或NACT+PBO(B组)。2022年4月,根据外部数据,试验停止新入组;主要终点被修正为调整的ITT人群(mITTP;数据库锁定2023年4月14日)中病理完全缓解(pCR;ypT0/is ypN0)率。次要终点包括程序性死亡配体1(PD-L1)阳性(PD-L1+)患者(SP142≥1%)的pCR率、残留癌症负担(RCB)0-1率(所有患者和PD-L1+)、不良事件(AE)发生率和死亡发生率。
结果
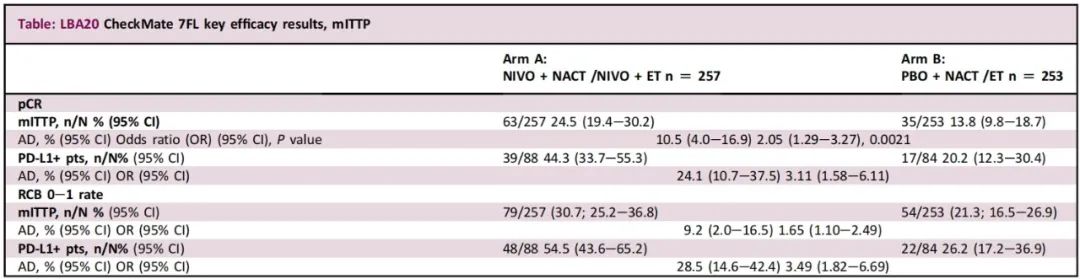
筛选830例患者,521例随机分组(A/B组,n=263/258),510例纳入mITTP。两组间的基线特征是平衡的。pCR率:A组(24.5%)总体上显著高于B组(13.8%;P=0.0021)和Ⅲ期亚组(A/B组,30.7%/8.1%)。NIVO使PD-L1+患者pCR的获益更高(调整后的差异[AD],24.1%;A组为44.3%,B组为20.2%)。RCB 0-1率总体改善,PD-L1+患者更明显。在NACT阶段,3/4级治疗相关的AE发生率在各组间相似(A/B组,n=92[35%]/82 [32%])。A组中有2例死亡(肺炎、肝炎)与研究药物相关。A组中免疫介导的AE(IMAE)发生率高于B组。
表2:CheckMate 7FL研究的关键疗效结果,mITTP
结论
CM-7FL研究达到其主要终点,显著改善了pCR和RCB 0-1率(PD-L1+患者增强),IMAE发生率增加,总体安全性与NIVO和CT一致。
摘要号:LBA 21
KEYNOTE-756研究pCR结果:在化疗中加入帕博利珠单抗显著提高了早期高危ER阳性、HER2阴性乳腺癌患者的pCR率
题目:Ⅲ期KEYNOTE-756研究:帕博利珠单抗/安慰剂+化疗新辅助治疗序贯帕博利珠单抗/安慰剂+内分泌治疗(ET)早期、高危、ER阳性、HER2阴性乳腺癌
报告人:Fatima Cardoso
背景
KEYNOTE-756(NCT03725059)是一项全球Ⅲ期研究,帕博利珠单抗/安慰剂+化疗新辅助治疗序贯帕博利珠单抗/安慰剂+内分泌疗法(ET)治疗高危、ER阳性、HER2阴性早期乳腺癌。在此,我们报告了主要的pCR结果。
方法
符合条件的患者为中心确认的T1c-2(≥2 cm)cN1-2或T3-4 cN0-2、Ⅲ期、侵入性导管ER阳性、HER2阴性乳腺癌患者,1:1随机分组接受帕博利珠单抗200 mg Q3W或安慰剂新辅助治疗,然后是紫杉醇QW 12周,然后4周期的多柔比星或表柔比星+环磷酰胺(新辅助治疗)。根治性手术(±放疗)后,患者接受9周期帕博利珠单抗或安慰剂+标准ET。分层因素包括区域(东欧 vs. 中国 vs. 其他)、肿瘤PD-L1状态(CPS≥1 [+] vs. CPS<1 [-])、淋巴结受累(+ vs. -)、ER阳性表达率(≥10% vs. <10%)和蒽环类药物治疗方案(Q3W vs. Q2W)。双主要终点是pCR(ypT0/Tis ypN0)和EFS。次要终点包括OS、pCR定义为ypT0、ypN0和ypT0/Tis和安全性。
结果
1278例患者随机接受帕博利珠单抗+化疗(n=635)或安慰剂+化疗(n=643)。在最终的pCR分析中(2023年5月25日,第一次期中分析数据截止),中位随访时间为33.2个月,ITT人群中,帕博利珠单抗+化疗 vs. 安慰剂+化疗显示pCR(ypT0/Tis ypN0)有统计学显著改善:24.3%(95% CI,21.0-27.8) vs. 15.6%(95% CI,12.8-18.6);估计差异为8.5%(95% CI,4.2-12.8);P=0.00005;与次要终点定义的pCR结果一致,ypT0 ypN0(21.3% vs. 12.8%)和ypT0/Tis(29.4% vs. 18.2%)。在预先指定的亚组中,帕博利珠单抗+化疗对pCR的获益一致。在新辅助治疗阶段,帕博利珠单抗+化疗组≥3级治疗相关的AE发生率为52.5%,安慰剂+化疗组为46.4%,其中帕博利珠单抗+化疗组有1例死于急性心肌梗死。EFS结果尚不成熟,随访仍在继续。
结论
在化疗中加入帕博利珠单抗显著提高了早期高危ER阳性、HER2阴性乳腺癌患者的pCR率,安全性与每种方案的已知情况相一致。
摘要号:LBA 18
Ⅲ期KEYNOTE-522研究更新结果:无论pCR结果如何,帕博利珠单抗联合化疗治疗早期TNBC患者的EFS有临床意义的改善
题目:Ⅲ期KEYNOTE-522研究更新的EFS结果:帕博利珠单抗/安慰剂+化疗序贯帕博利珠单抗/安慰剂治疗早期三阴性乳腺癌患者
报告人:Peter Schmid
背景
KEYNOTE-522(NCT03036488)研究显示,在早期三阴性乳腺癌(TNBC)患者的化疗中加入帕博利珠单抗后,pCR和EFS具有统计学意义和临床意义的改善。在此,我们展示了中位随访大约5年后更新的EFS结果。
方法
符合条件的患者为既往未经治疗、非转移性、中心确认的TNBC(AJCC评估的T1c N1-2或T2-4 N0-2),2:1随机分组接受帕博利珠单抗200 mg Q3W或安慰剂新辅助治疗,两组均接受4周期紫杉醇+卡铂治疗,然后给予4周期多柔比星或表柔比星+环磷酰胺。根治性手术后,患者接受帕博利珠单抗或安慰剂辅助治疗9周期或直到复发或出现不可耐受的毒性。双主要终点是pCR(ypT0/Tis ypN0)和EFS(从随机分组到疾病进展的时间,排除了根治性手术、局部/远处复发、第二原发癌症或任何原因导致的死亡)。
结果
1174例患者被随机分为帕博利珠单抗组(n=784)或安慰剂组(n=390)。在数据截止日期(2023年3月23日),中位随访时间为63.1个月。帕博利珠单抗组有145例(18.5%)且安慰剂组有108例(27.7%)发生EFS事件(HR 0.63 [95% CI,0.49-0.81]),60个月的EFS率(95% CI)分别为81.3%(78.4-83.9)和72.3%(67.5-76.5);两组均未达到中位数。最常见的首次EFS事件是远处复发,帕博利珠单抗组有72例(9.2%),而安慰剂组有55例(14.1%)。在210例远处复发事件中,帕博利珠单抗组患者在60个月时的远处疾病进展或无远处复发生存率为84.4%,而安慰剂组患者为76.8%(HR 0.64[95% CI,0.49-0.84])。帕博利珠单抗的EFS获益在预先指定的亚组中是一致的,包括PD-L1表达和淋巴结状态。在一项预先指定的、非随机、探索性分析中,帕博利珠单抗组和安慰剂组的5年EFS率在达pCR的患者中为92.2% vs. 88.2%,在未达pCR的患者中为62.6% vs. 52.3%。OS随访仍在继续。
结论
无论pCR结果如何,帕博利珠单抗联合化疗新辅助治疗序贯帕博利珠单抗继续辅助治疗 vs. 单独化疗新辅助治疗早期TNBC患者的EFS有临床意义的改善。
2 转移性乳腺癌
摘要号:LBA 11
TROPION-Breast01研究结果支持Dato-DXd作为一种新的治疗方案,用于既往接受过1-2线化疗的不可手术或转移性HR阳性、HER2阴性乳腺癌患者
题目:随机、Ⅲ期TROPION-Breast01研究的主要结果:datopotamab deruxtecan (Dato-DXd) vs. 化疗治疗既往不可手术或转移性HR阳性、HER2阴性乳腺癌
报告人:Aditya Bardia
背景
在Ⅰ期TROPION-PanTumor01试验(NCT03401385)中,靶向Trop-2的抗体-药物偶联结合物Dato-DXd在既往经过多重治疗的不可手术或转移性HR阳性、HER2阴性乳腺癌患者中显示出良好的活性。在此,我们报告了来自全球Ⅲ期TROPION-Breast01试验(NCT05104866)的主要PFS结果。
方法
经内分泌治疗(ET)后进展或不适合ET或既往接受过1-2线全身化疗(CT)的不可手术或转移性HR阳性、HER2阴性乳腺癌成人患者1:1随机分组至Dato-DXd(6 mg/kg Q3W)或研究者选择CT(ICC;艾立布林、长春瑞滨、卡培他滨或吉西他滨),直至进展或不可耐受的毒性。双主要终点是盲法独立中心审查(BICR)根据RECIST 1.1评估的PFS和OS。
结果
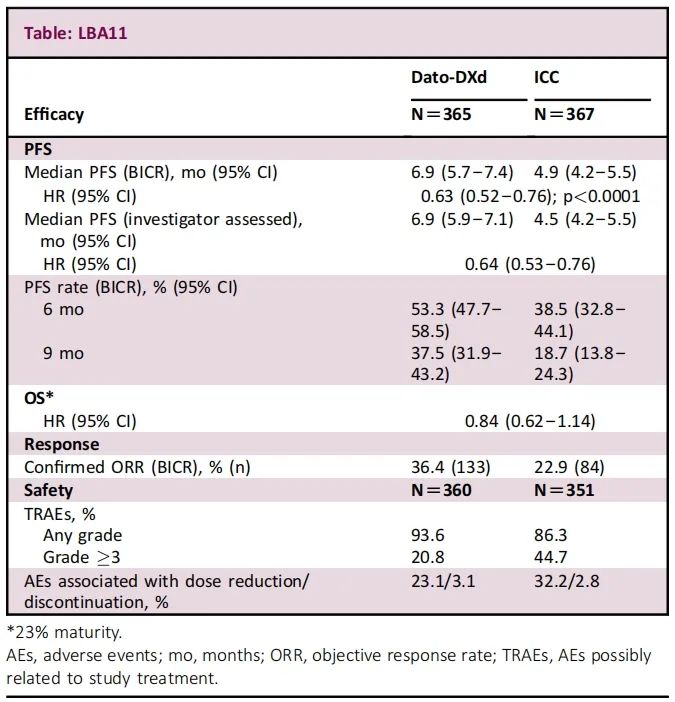
732例患者被随机分组(Dato-DXd:365;ICC:367)。Dato-DXd/ICC组的中位年龄(范围)为56岁(29-86)/54岁(28-86)。在数据截止时(2023年7月17日),Dato-DXd/ICC组中有93/39例患者正在进行治疗,结果如表3所示。与ICC相比,接受Dato-DXd治疗的患者PFS显著改善(HR 0.63[95% CI 0.52-0.76];p<0.0001),OS数据尚不成熟。与ICC相比,接受Dato-DXd治疗的患者的3级TRAE发生率和剂量减少发生率更低(表3)。
表3:TROPION-Breast01研究PFS、OS及安全性结果
结论
TROPION-Breast01研究达到PFS的主要终点;研究尚不成熟,OS随访仍在继续。与ICC相比,接受Dato-DXd治疗的患者PFS有统计学意义和临床意义的改善,以及良好和可控的安全性。结果支持Dato-DXd作为一种新的治疗方案,用于既往接受过1-2线化疗的不可手术或转移性HR阳性、HER2阴性乳腺癌患者。

