Lancet Rheumatol:类风湿关节炎患者病理生物学生物疗法分层
时间:2023-12-05 21:38:36 热度:37.1℃ 作者:网络
生物疾病修饰抗风湿药物(DMARDs)改变了类风湿关节炎患者的前景。然而,大约40%的患者缺乏有意义的治疗反应,特别是在使用低疾病活动或缓解等严格反应标准时,以及潜在的副作用和接触潜在无效的高成本药物,突出表明需要确定反应的预测标志物,以确保个人目标治疗的最佳治疗结果,并促进患者在治疗前分层。
与众所周知的类风湿关节炎异质性一致,对生物DMARD的可变反应可能与单个患者治疗靶点的可变表达和致病相关性有关。几项研究试图定义与生物DMARD反应相关的血液和滑膜生物标志物,包括基因(DNA、RNA和miRNA)和蛋白质。然而,大多数证据来自临床试验的小型观察研究或事后分析,其预测价值不大,临床实践中患者分层的临床适用性有限。
2021年的一项随机对照试验(R4RA)报告称,与白细胞介素-6受体抑制(tocilizumab)相比,对至少一种肿瘤坏死因子(TNF)抑制剂没有反应的患者中,低或不存在的滑膜B细胞分子特征与B细胞耗竭(利妥昔单抗)的反应较低有关。对同一试验的进一步分析确定了对单个疗法治疗反应的分子预测因子,以及与多药耐药性相关的特征。

2023年10月23日发表在Lancet Rheumatol的文章,报告了通过病理生物学(STRAP)试验分层类风湿性关节炎生物疗法的结果,其主要目的是测试分析滑膜B细胞浸润作为潜在生物标志物的实用性,以指导对传统合成DMARD没有反应的患者做出治疗决策的实用性。主要假设是,与依那西和托西珠单抗组合在一起评估,通过组织形态学和B细胞特异性分子评分评估的低B细胞浸润的患者对利妥昔单抗的B细胞消耗反应更差。
STRAP和STRAP-EU是在英国和欧洲26个大学中心进行的两项平行、开放标签、活检驱动、分层、随机的第三阶段试验。包括基于美国风湿病学会(ACR)-欧洲抗风湿联盟分类标准和对常规合成抗风湿药物(DMARD)反应不足的18岁或以上的生物质类风湿关节炎患者。
超声引导的超声活检后,根据滑膜B细胞特征将患者分为B细胞贫乏或富含B细胞,并随机(1:1:1)分配到静脉注射利妥昔单抗(0周和第2周1000毫克)、皮下托西利单抗(每周162毫克)或皮下依那西诺西(每周50毫克)(每周50毫克)。
主要结果是B细胞贫乏、有意治疗的人群(定义为所有随机分配的患者)的16周ACR20反应,汇集了两项试验的数据,比较了依那西塞和托西利珠单抗(分组)与利妥昔单抗。对所有接受至少一剂研究药物的患者的安全性进行了评估。
研究结果显示,2015年6月8日至2019年7月4日期间,226名患者被随机分配到依那西普(n=73)、tocilizumab(n=74)和利妥昔单抗(n=79)。三名患者(每组一名)在随机化后被排除在外,因为他们在招募前的4周内接受了肠外类固醇。在有意治疗的223名患者中,168名患者中,168名(75%)是女性,170名(76%)是白人。
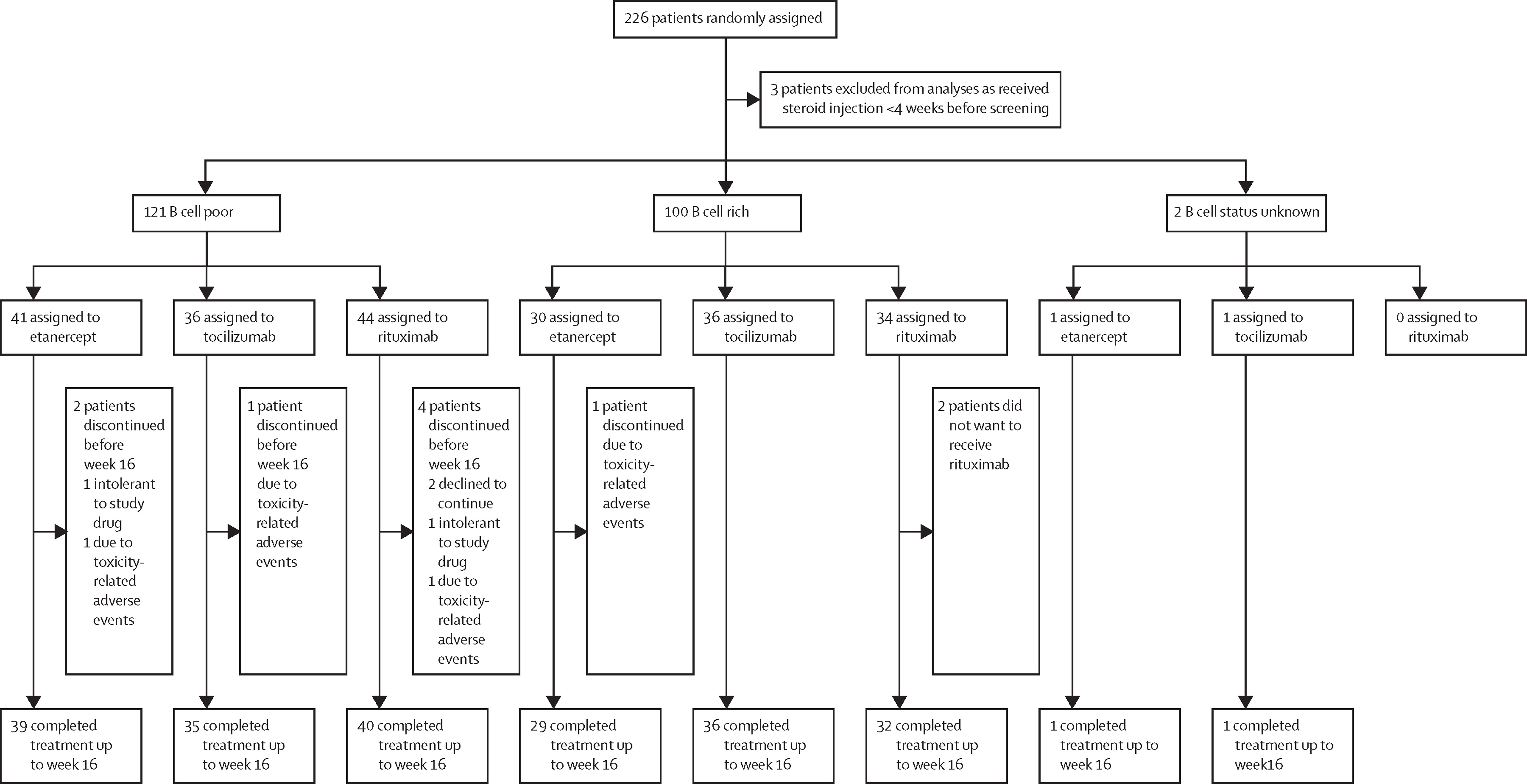
审判简介
在B细胞贫乏人群中,16周(主要终点)的ACR20反应显示依那西嗪和托西单抗与利妥昔单抗之间没有显著差异(77名患者中有46[60%],44名患者中有26[59%];赔率为1.02[95%CI 0.47–2.17],p=0.97)。不良事件没有观察到差异,包括严重不良事件,利妥昔单抗组102名患者中有6人(6%)、依那西单抗组108名患者中有9名(6%)和tocilizumab组73名患者中的3名患者中有3名(4%)(p=0.53)。
综上所述,STRAP试验表明,与依那赛普或托西利珠单抗相比,舒单抗治疗利妥昔单抗的二分体分类无法预测治疗患者的治疗反应,因为对于滑膜B细胞特征低或缺失的患者,主要终点(ACR20反应)没有显著差异。然而,研究表明,滑膜组织分析可能与临床实践具有潜在相关性。
特别是,具有pouci免疫病理类型的患者对利妥昔单抗的反应较低,加上利妥昔单抗的作用缓慢,富含B细胞的患者放射学进展风险较高,表明利妥昔单抗不太适合早期疾病,因为抑制结构损伤的机会之窗需要能够快速控制关节炎的药物。
至于类风湿性关节炎精密医学的未来,预计响应与非响应的预测算法将从正在进行的后期深层分子分析中出现。此外,鉴于风湿关节炎众所周知的异质性,而不是二元患者分层,应使用更全面的生物标志物驱动方法,其中将颗粒分子和组织学反应特征结合起来,以定义对单个药物治疗反应的预测算法。
原始出处
Rivellese, F., Nerviani, A., Giorli, G., Warren, L., Jaworska, E., Bombardieri, M., ... & Romão, V. (2023). Stratification of biological therapies by pathobiology in biologic-naive patients with rheumatoid arthritis (STRAP and STRAP-EU): two parallel, open-label, biopsy-driven, randomised trials. The Lancet Rheumatology, 5(11), e648-e659.


