关于停止肾脏替代治疗的时机,我们知道些什么?
时间:2023-12-10 23:41:01 热度:37.1℃ 作者:网络
目的 急性肾损伤在重症患者中很常见,支持治疗包括使用肾脏替代疗法作为器官支持。在过去的几年中,肾脏替代治疗的启动时机一直是备受关注的话题,有几项随机对照研究探讨了开始RRT的最佳时间。与此相反,关于停止RRT时机的证据却很少。鉴于这种治疗复杂、价格昂贵且有一定风险,我们似乎应该及时花费精力来解决这个棘手的问题。
近期发现 尽管有几项研究报告了肾脏替代治疗的成功终止,但迄今为止的所有研究都是观察性的,大多使用了常规的生化指标以及包括尿量在内的生理参数。近年来,更多新的肾功能生物标志物被纳入研究,但到目前为止并没有确定出最佳变量或终止阈值。
总结 目前已知有几个变量可能在确定哪些患者可以成功撤离肾脏替代治疗中发挥着作用。尽管尿量是最常用的指标,但却很少有人接受过有力的检查,任何可疑指标的支持证据都十分稀少。最近,一些新的生物标志物也被纳入研究,但同样受到研究设计和异质性的限制。很明显,我们需要进一步的研究来更好地关注多变量模型中的优选变量,以提高预测能力并成功终止治疗。
引言
急性肾损伤( AKI )在危重症中很常见,据报道其发生率高达60 %,当然这取决于AKI的定义和标准。AKI的发展与短期和长期死亡率增加均有关,其中病情严重到需要应用肾脏支持治疗的患者死亡率高达50 %。因此,肾脏替代治疗(RRT )仍然是约4 - 10 %危重症患者的常用干预措施,在ICU患者中更是高达23.5 %。
迄今为止,大多数研究都集中在何时启动RRT这一棘手问题上,更是通过多个大型随机对照试验(RCT )以及大量的回顾性队列和临床研究对此进行了调查。这些研究包括审查RRT的"经典指征"(如难治性高钾血症和/或酸中毒)以及侧重于RRT最佳启动时机的研究。相比之下,RRT的终止相对被我们忽视,事实上,最近的一项系统评价也并未能确定出任何研究该问题的RCT。这与机械通气的撤机过程形成了鲜明对比,例如,在撤机过程中,有多个基于RCT的指南和已发表的协议,以帮助临床医生就撤出这种形式的器官支持做出决策。
相关证据表明,尝试停止RRT的失败与较差的临床结果相关,包括ICU住院时间延长和死亡率增加。然而,目前尚不清楚撤机失败是否代表着整体临床情况更差——即疾病的严重程度,而不是与RRT的过早停止直接相关。结合证据表明,RRT治疗的非必要延长可能损害肾脏功能恢复,特别是当对治疗产生不利影响时,因此RRT的成功撤离似乎是一个与启动RRT同样值得关注的领域。目前,减少RRT治疗剂量、改变治疗模式甚至完全停止都是基于一系列生化参数(血清尿素、肌酐、肌酐清除率)、患者特征(如血流动力学稳定性、液体平衡、电解质紊乱和临床决策)以及管理工作(如管路凝血、人员可用性和管路并发症)的决定。
有效停止的定义
简单来说,这意味着脱离器官支持——不再需要进一步的体外肾脏支持,但目前尚无公认的RRT有效停止的定义。KDIGO指南建议在“不再需要RRT的情况下”停止RRT ——要么是因为固有肾功能已经恢复到足以满足患者需求的程度,要么是因为RRT不再符合护理的目标。这也符合机械通气撤机的原则,即肾损伤的根本原因已经解决,支持治疗可以撤离并最终使患者解放出来。由于缺乏共识,已发表的研究对成功停止RRT的定义存在显著差异。大多数研究将其定义为患者未接受进一步RRT的特定时期,但这一"无RRT期"的确切时间跨度在为期3 ~ 60天的研究中存在显著差异,这使得比较工作变得困难。
最近,关于RRT时机的研究也包括了对停止治疗的指导。例如,在AKIKI试验中,根据预定义的尿量标准或在利尿足以使血肌酐浓度自发下降的情况下,可以考虑停止RRT。在STARRT AKI试验中,RRT一旦启动,将持续进行,除非遇到下列情况之一:①死亡;②患者的护理目标发生改变的情况下撤销生命支持干预措施;③临床医生判断患者肾功能恢复无需继续RRT。如果停用RRT一段时间后再次出现肾功能不全,则由治疗医师酌情重新启动RRT。
模式改变
CRRT的撤机过程可能是一个逐步过渡到完全停止RRT的过程,这可能包括减少处方剂量、过渡到混合模式(如持续低效率透析或使用间歇性血液透析)。这种从连续性治疗到间歇性治疗的过渡并没有显示出连续性肾脏替代治疗( CRRT )和混合模式在死亡率、血流动力学稳定性、溶质清除或透析依赖方面的差异,因此它是一种可行的从CRRT中脱机的实用方法。
成功停止肾脏替代治疗的预测因素
一些探讨成功停止RRT预测因素的研究在确定停止阈值的生化和生理值方面再次表现出显著的差异性。此外,这些变量的测量时机(即RRT停止前或停止后)往往没有统一要求。其中涵盖了尿量、传统生物标志物(如血清肌酐)、更新颖的指标和多变量预测模型等。
(1) 尿量
近年来,作为AKI分级的标准,尿量也常被临床医生认为是在ICU环境下成功停用或脱离RRT的最重要的预测因素。2013年一项关于英国重症监护病房AKI管理的当代实践调查显示,停止RRT最常见的原因是尿量增加( 74 % )、pH值正常化( 70 % )和容量状态目标得到满足( 55 % )。有趣的是,39 %的患者也使用了血清尿素和肌酐的正常化作为撤机指标。尿量仍是迄今为止关于预测RRT成功终止的变量中被研究得最多的。然而,相关研究中预测可能成功停止RRT治疗的尿量差异十分显著(范围从191 ml / 24 h到超过1700 ml / 24 h),这使得研究之间的可推广性和比较变得困难。Best Kidney研究纳入了529例患者的数据,其发现自发尿量达436 ml/天和使用利尿剂后2330 ml/天的尿量对成功撤机具有最高的敏感性、特异性和阳性预测值( 80.9 %和87.9 %)。而另有研究认为尿量增加100ml/天是成功预测因素。实际上,这一标准也被用于关于RRT启动策略的AKIKI试验——①如果自发尿量≥500 ml/24 h,则考虑停止RRT;②对于需接受利尿剂治疗的患者,其自主排尿量> 1 000 ml/24 h或使用利尿剂情况下> 2000 ml/24 h,建议停用RRT;③在试验期间,如果利尿足以使血清肌酐浓度自发下降,则必须停止肾脏替代治疗。如果利尿不足以导致肌酐水平自发下降,或在没有利尿治疗的情况下,尿量每24小时低于1000毫升(或接受利尿治疗的患者每24小时低于2000毫升),则恢复RRT。同样,在RRT时机的ELAIN研究中,肾脏恢复定义为在没有利尿剂治疗的情况下尿量>400 ml / 24 h,而在使用利尿剂治疗的情况下尿量为>2100 ml / 24 h。
然而到目前为止,用来指导停止RRT的尿量或产生率还没有统一标准。关于尿液排出的时间,不管是停止前还是停止后的一小时内的尿量,对于预测成功都没有体现出更高的价值。一项纳入86例患者的回顾性研究中有78 %的患者成功撤机,研究指出停止RRT后的6小时尿量是最成功的预测因素,当尿量<0.3 ml/kg/h时,超过70 %的患者撤机失败。考虑到这反映了无法排出足够的溶质负荷,这些发现并不令人意外,也符合尿量作为最广泛研究的变量的优势。如前所述,利尿剂的使用和反应也被考虑在内。在预测AKI方面,呋塞米的肾小管反应性已经通过呋塞米负荷试验进行了广泛的评估。然而,利尿剂在停用RRT中的作用尚不清楚。有趣的是,本研究建立了多变量模型,确定了CRRT撤机成功的危险因素是性别和停止CRRT后6 h尿量。在接受呋塞米治疗的患者中,停止治疗后6 h尿量预测CRRT成功撤机的受试者工作曲线下面积( AUC-ROC )为0.94 ( 0.88 ~ 1.0 ),在肾小管功能未恢复的患者中为0.85 ( 0.72 ~ 0.99 )。然而,来自BEST肾脏研究的数据发现,尿量对成功停止RRT的预测能力受到包括利尿剂的负面影响。这似乎表明,增加利尿在RRT停止时可能作为一种管理液体正平衡和液体超负荷的方法,降低了RRT的再启动率。然而,一项探讨RRT后给予呋塞米的RCT研究并未显示出对肌酐清除率高于30 ml/min或肌酐清除率低于30 ml/min且血肌酐水平稳定至少3天的AKI恢复的显著影响。与安慰剂相比,尽管呋塞米的使用并没有改善肾功能,但那些尿生成率显著升高的患者并不需要再继续进行肾脏替代治疗。
(2) 传统生物标志物
尽管所使用的血肌酐值之间也存在显著的异质性,但在个别研究和多变量模型中,血肌酐已被确定为有助于预测RRT脱机的因素。血肌酐倾向于与一系列其他临床和生化值结合使用,以帮助有关RRT的决策。例如,在ICU患者中,每日24 h尿肌酐排泄量可预测RRT的撤机——当尿肌酐> 5.2 mmol/24 h时,受试者曲线下面积为0.76。值得注意的是,利尿剂的使用并不影响结果。在进一步的前瞻性研究中发现,2 h肌酐清除率可用于指导CRRT的停止,且优于血肌酐值或尿量。同样,在ATN试验中,也使用了2 h肌酐清除率值来决定是否停止RRT。在因AKI接受间歇性血液透析( IHD )的患者中,尿量和尿尿素浓度也被发现可以预测撤机成功。IHD撤机的最佳诊断阈值为尿量>8.5 ml/kg/24 h,尿尿素浓度>148mmol/L,每日尿素排泄量>1.35 mmol / kg / 24 h。每日尿尿素排泄量的AUROC ( 0.96 )大于尿量的AUROC ( 0.86 )或尿尿素浓度的AUROC ( 0.83 ) ( P < 0.001)。
估算的肾小球滤过率是最常用的肾功能指标,但其在RRT停止决策中的价值尚不清楚。eGFR计算公式的准确性取决于稳态血清肌酐( SCr )浓度,但这在RRT停止后几乎是不可能实现的。SCr的一个潜在应用是通过使用动态eGFR,即一种在血清肌酐变化的情况下估计肾功能的措施,通过在不同时间点两次测量SCr计算的肌酐清除率,从理论上反映肾功能的动态变化。有2项小型的回顾性研究显示了良好的区分度,AUROC为0.87。值得注意的是,在ICU患者中,如果不直接测量,通常会出现肌肉消耗导致肌酐值下降,高估肾功能的情况。
(3) 新型标志物
与肾损伤相关的新型生物标志物也被用于预测肾脏恢复和转归。一些研究致力于使用这些生物标志物来区分短暂性和持续性AKI以及肾脏功能恢复,如果这些生物标志物的初始水平较低,或者浓度下降,那么肾脏恢复的可能性更大。这些生物标志物也是用于预测成功停止RRT或在RRT停止之前证明肾脏恢复的证据的焦点。中性粒细胞明胶酶相关脂质运载蛋白( NGAL )在远端肾单位产生,在肾损伤时其合成上调,因此被认为是预测和识别AKI的生物标志物,也是需要行RRT治疗的预测因子。保守治疗AKI时NGAL的降低可作为AKI恢复的良好预测指标。事实上,多位学者已经进行了关于NGAL对预测停用RRT时机相关的研究。
Chen等人的研究表明,停止RRT治疗时血清NAGL水平403ng /ml预测成功撤机的AUROC值为0.81,然而其他研究认为血浆NT-proBNP,(而不是血浆NGAL)是撤机相关预测因素。各项研究(尤其是综合性研究)往往没有报告使用的参考标准和阈值,因此使用NGAL作为预测因素的研究之间往往很难进行比较。也有研究表明,血清NGAL值的连续下降,而并非一个特定的阈值,也与预测肾脏恢复和成功停止RRT的能力有关。最近的一项多中心研究中,NGAL和白介素- 6 在严重AKI患者CRRT治疗中的应用价值得到了验证。研究共纳入133名患者,其中存活组105名。死亡组患者RRT开始时尿NGAL和血浆IL - 6水平均显著高于存活组,但RRT停止时尿NGAL水平显著低于治疗成功组(定义为7 d时脱离RRT ),血浆IL - 6水平在两组间差异无统计学意义。
胱抑素C 是肾功能的可靠生物标志物,在估算肾小球滤过率方面显示出替代肌酐的前景。胱抑素C是中等大小的分子( 13.3 k Da ),在近端肾小管中完全分解代谢,不被重吸收回血液,不受性别、年龄、种族、蛋白质摄入量或肌肉量的影响,当GFR相应下降时,胱抑素C升高,在AKI的早期检测中具有重要的应用前景。同样地,在已报道的研究中,使用的时间和阈值都存在显著的异质性,范围波动于从撤离CRRT时的1.85 mg /l到入住ICU时的2.98mg/l不等。一些学者提出将血清胱抑素C作为CVVH过程中残余肾功能的标志物。然而,这一发现受到了质疑,即基于不同模式胱抑素可以在启动RRT后显著下降,表明有显著的体外清除。
前脑啡肽A 119- 159(penKid)已被作为研究肾功能的生物标志物,在AKI患者中具有重要应用。即使在不稳定的环境中,其也可以反映实时肾小球滤过率,且不受系统危重症、炎症、年龄或性别的影响。在一项ELAIN试验的事后分析中,RRT开始前较低的penKid水平( 89pmol / l)与早期成功脱离RRT有关。然而,该分子的确切药代动力学和生物学调控在很大程度上仍然是未知的。
(4) 危险评分
为了预测患者如何成功撤离RRT治疗,一些研究采用了多变量分析。在一项单中心研究中,共有1158例患者成功撤机——定义为撤机后7天内不需要RRT。符合成功撤机标准的患者在撤机前一天( D-1 ) UO更大,多因素分析显示D-1尿量300 ml、平均动脉压50 ~ 78 mm Hg、血钾< 4.1mmol/l、BUN <35mg/dl ( 12.5 mmol / l )是CRRT成功撤机的预测因素。使用这四个变量开发评分系统时,其AUROC为0.731。在另一个单中心研究中,纳入1135例需要CRRT的患者,成功撤机被定义为在撤机后72 h内未接受任何RRT治疗并存活至出院。建立多变量logistic回归模型并进行内部验证,独立预测因素包括撤机前12 h内平均每小时尿量、撤机前24 h内平均血肌酐值、入ICU至撤机前累积液体平衡量、撤机前CRRT持续时间和撤机前24 h内血管活性药物需要量。该模型在验证集中表现出良好的区分度( AUROC分别为0.76和0.78;阳性预测值分别为36 %和48 %;阴性预测值分别为92 %和94 % )和校准度。
当前的建议
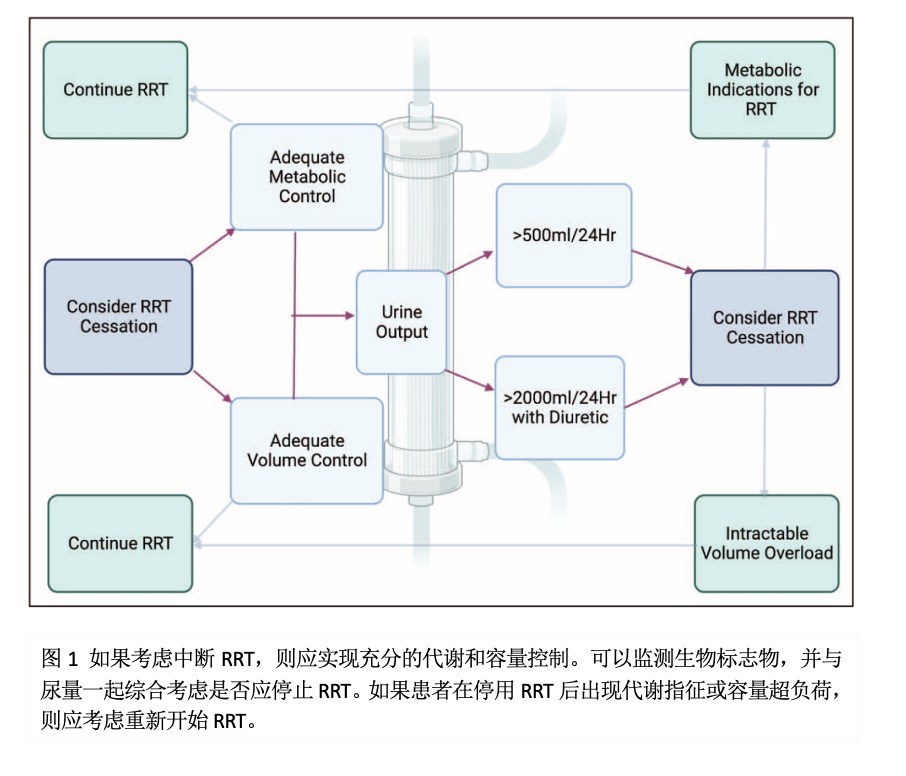
目前尚缺乏足够的证据来提出关于停止RRT的建议。专家们已经提出了几种成功撤机的预测因子,但由于所使用的标志物及参考值和时间的异质性使得各项研究难以进行相互比较。与单独的个体因素相比,综合评分可能会更好地预测RRT的成功撤机。图1展示了一种比较贴合临床实际的撤机路径。在患者血流动力学和代谢得以改善且实现理想的容量平衡的情况下,可以考虑停止RRT治疗,其中尿量被认为是合适的预测指标。目前文献建议,若患者停用利尿剂24 h内尿量≥500 ml或予利尿剂后≥2L/24h,方可考虑撤机。未来关于新型生物标志物研究的数据可能会提高尿量的单独预测能力。在考虑最佳的撤机和停止时机时需要考虑的其他因素包括开始治疗的根本原因:如果启动RRT是为了控制液体量、电解质紊乱或急性尿毒症的治疗,那么在撤机前必须充分控制这些变量,并评估呼吸和心血管血流动力学,否则很难成功撤机。急性RRT如果用于治疗中毒,则撤机关键将取决于毒素的清除。在一项回顾性观察性研究中显示,在有清除毒素相关指征的患者中,RRT的撤机成功率为100 %。
结论
迄今为止,尚无多中心随机对照研究探讨成功撤机的潜在预测因素。一些观察性研究表明,当患者自发尿量> 400 ml/24h且肌酐清除率为15~20 ml/min,或当尿量> 30 ml/h且24h尿肌酐排泄量> 5.2mmol/L时,可以尝试停止RRT。然而,最近的一项系统评价认为,目前文献的异质性较大,以至于无法得出最佳撤机阈值的建议。由于目前各项研究的异质性很大,未来需要制定一个含有记录的RRT自由时间框架,以使进一步的研究工作顺利进行,并让专家学者对成功中止肾脏替代治疗有更明确的定义。停止RRT的决定可能需要个体化,并考虑到行RRT的根本原因、患者目前的临床状态以及纳入临床和生化指标,未来我们还需开发并使用复合模型对此进行预测。


