【ASH继续教育】CLL的MRD驱动治疗:MRD的定义、检测方法及对长期生存的影响
时间:2024-01-12 20:59:35 热度:37.1℃ 作者:网络
CLL中的MRD
近年来,慢性淋巴细胞白血病 (CLL) 患者的治疗已从免疫化疗 (CIT) 转向使用新型靶向药物,包括BTK抑制剂和和 BCL2抑制剂,且通常与抗 CD20 单克隆抗体联合使用,现在已成为一线治疗和复发治疗的基石。随着 CLL 治疗格局的演变,也需要重新定义其治疗终点。在CIT、维奈克拉为基础方案和细胞治疗后,检测MRD是一种较为灵敏的评估肿瘤负荷手段,已证实其预后价值。
尽管最近取得了进展,但 MRD驱动治疗(MRD-directed therapy,个人更喜欢翻译成驱动治疗)的实用性以及在常规临床实践中根除MRD的尝试仍存在争议。临床试验中很少有关于检测MRD阴性(U-MRD) 的最佳方法,以及监测MRD是否可以改变治疗策略。
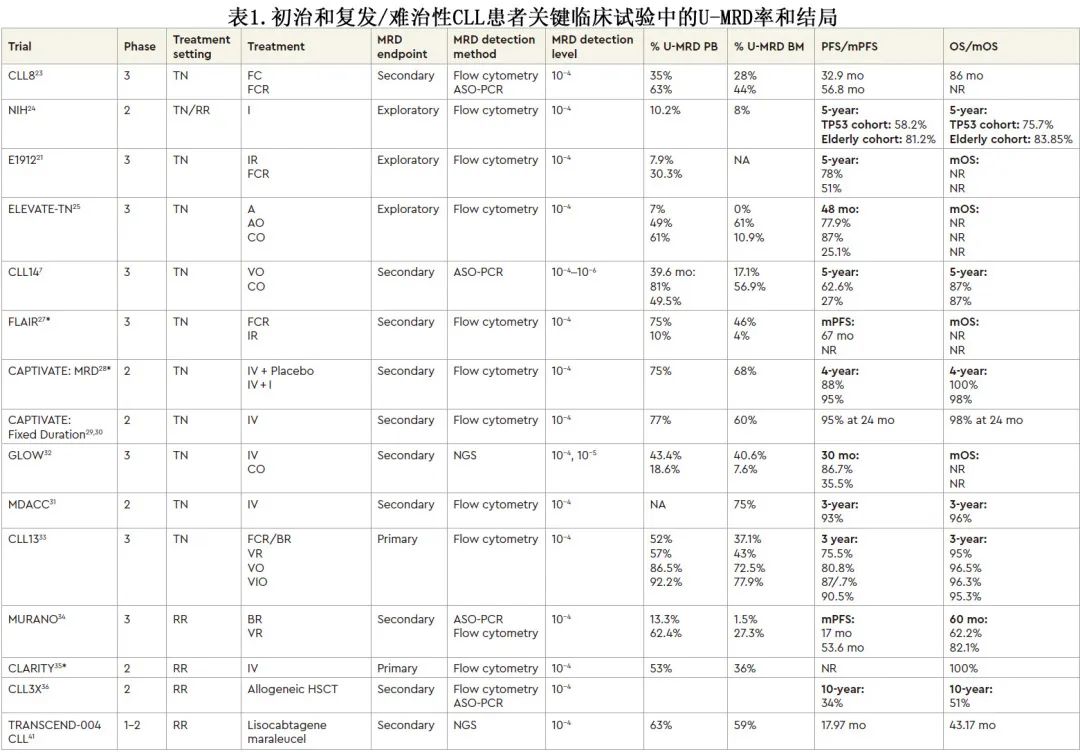
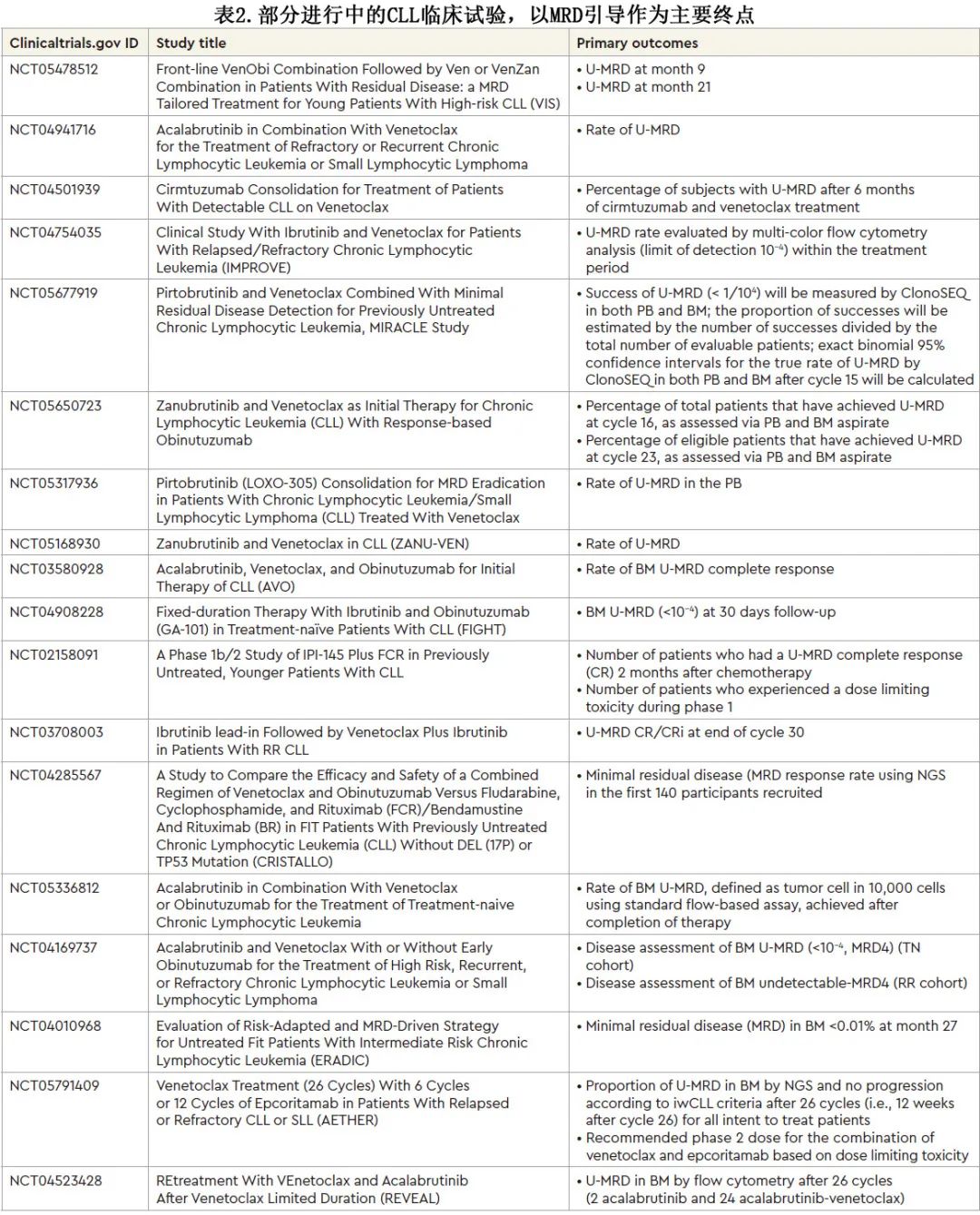
2023年ASH继续教育项目一篇文章中,作者综合讨论了 MRD 的定义、检测方法及其对 CLL 患者长期生存的影响,也包括新靶点治疗的结局(表1)和开发中的新型两药/三药联合方案(表2)。

学习目标
•审查 CLL 中MRD的定义、术语和检测方法
•审查当前使用“不可测量残留病灶”的数据及其对生存结局的预后作用
•讨论当前临床试验数据结果的潜在临床应用和进一步研究的领域
临床案例
JT 是一名73岁男性,既往有高血压和高脂血症病史,6年前诊断为CLL,当时在择期膝关节置换术的术前血液检查中发现孤立性淋巴细胞增多。本次就诊中自述疲劳恶化和新发早饱症状。血液检查显示白细胞计数为113000个细胞/μL,血红蛋白为9.3 g/dL,血小板计数为93000个细胞/μL。患者现在符合 iwCLL标准可开始治疗,与患者讨论开始连续 BTKi 或用 维奈克拉-奥妥珠单抗(VO) 治疗一年。在临床访视前患者了解了 MRD 检查的相关内容,询问哪种治疗最佳,可给出最深缓解。
如何定义MRD?
MRD 定义为样本中检测到的 CLL 细胞数量。最近召集了一个专家小组对 CLL 中 MRD 的命名和评估进行标准化。未检出 MRD(U-MRD) 是首选术语。MRD 水平定义为MRD4(10-4或1/10000白细胞)、MRD5(10-5或1/100000白细胞)和MRD6(10-6或1/1000000白细胞)。考虑到现有分析方法的异质性,在讨论 MRD 结果时需要报告所用方法、灵敏度阈值和供试样本(tested compartment)。在 MRD 结果中识别供试样本很重要,因为外周血 (PB) 和骨髓 (BM) 之间可能存在不一致。专家小组及 iwCLL 指南将 U-MRD 阈值定义为至少10-4(MRD4)。尽管尚无关于 MRD 检测和监测时间的具体指南,专家小组共识建议考虑在完成固定持续时间治疗后至少两个月进行检测。目前,在常规临床实践中如何使用 MRD 检测结果尚无共识指南。
如何检测MRD?
MRD 检测方法多种多样(图1),其中基于流式细胞术的检测是最广泛使用和最常用的方法。欧洲 CLL 研究倡议为通过流式细胞术协调 MRD 检测提供了共识指南。目前的建议是使用由CD5、CD19、CD20、CD43、CD79b和 CD81 组成的抗体组,其可以通过四色流检测到MRD4。6色和10色流式细胞术可以增加灵敏度,可检测到MRD5。还可以进行免疫球蛋白重链可变区 (IGHV) 基因的聚合酶链反应 (PCR),可以达到 MRD6 的灵敏度,但需要患者特异性引物,因此多在临床试验中使用,但在临床实践中不常用。二代测序 (NGS) 检测和 IGH VDJ 或DJ、IgK和 IgL 受体基因序列重排或易位 BCL1/IGH(J) 和 BCL2/IGH(J) 的检测更易得。基于 NGS 的检测方法与流式细胞术检测方法具有良好的一致性,对 MRD6 敏感,并已纳入前瞻性临床试验。这些检测要求基线样本在开始治疗前确定克隆性。新出现的 MRD 检测包括数字微滴 PCR(ddPCR) 和无细胞DNA(cfDNA),两者均显示出极好的灵敏度,但不常规使用。

MRD与靶向药物持续治疗
BTKi 单药治疗与 CIT 相比,可改善无进展生存期 (PFS) 和总生存期 (OS) 。多项研究已证实 MRD 在 CIT 治疗患者中的预后价值,对于接受氟达拉滨、环磷酰胺和利妥昔单抗 (FCR) 治疗的患者,U-MRD缓解可预测PFS,尤其是对于 IGHV 突变的 MRD6 缓解患者。鉴于 U-MRD 反应在预测 CIT 结局方面的预后价值,多项临床试验探索了 U-MRD 在BTKi连续治疗中的作用。
伊布替尼持续治疗的研究表明,完全缓解 (CR) 率和 U-MRD 率均较低,但仍有较好的 PFS 和OS,包括在具有高危遗传特征(例如del17p/TP53、IGHV未突变、复杂核型)的患者中。在 NIH 针对老年患者或 TP53 异常患者开展的 II 期 CLL 研究中,伊布替尼单药持续治疗的缓解随时间加深,CR 率从治疗6个月时的0%增加至治疗60个月时的28.4%,4年时 U-MRD 率较低:PB为10.2%(5/49),BM为8%(2/25)。尽管 U-MRD 率较低,但 TP53 异常患者的5年 PFS 极佳(58.2%),老年患者为81.2%。在<65岁 CLL 初治fit患者中比较伊布替尼-利妥昔单抗 (IR)(持续伊布替尼)与6个周期 FCR 的关键3期E1912 研究中也观察到类似结果。在5.8年随访时,IR组的中位 PFS 长于 FCR 组(风险比 [HR]=0.37),IGHV 未突变患者的 OS 有小幅但具有统计学意义的改善 (HR=0.35;p=0.01),但IGHV 突变患者无改善 (HR=0.72;p=0.68)。接受 FCR 治疗的患者在3、12、24和36个月时的 U-MRD4 率高于IR(3个月时为29.1%,12个月时为30.3% vs 7.9%,24个月时为23.4% vs 4.2%,36个月时为8.6% vs 3.7%)。比较阿可替尼、阿可替尼-奥妥珠单抗(AO) 和苯丁酸氮芥-奥妥珠单抗(CO) 的3期ELEVATE-TN研究更新4年随访结果也表明,尽管 U-MRD 发生率较低,但接受含阿可替尼治疗的患者的4年 PFS 有所改善。这些结果表明,即使在治疗多年后,BTKi的结局仍极佳。因此,目前的建议是持续治疗直至疾病进展或出现不可接受的毒性,因此不建议进行常规 MRD 检测。
FLAIR 研究在无 del(17p) 的初治fit CLL 患者中比较了 IR 与 FCR 治疗。伊布替尼治疗持续6年,直至U-MRD4、毒性或疾病进展;在随机化后9个月和12个月以及此后每6个月评估 PB 和 BM MRD,如果达到U-MRD,则停止伊布替尼治疗,治疗持续时间基于从随机化至 U-MRD 的时间。中位随访53个月时,IR组未达到中位PFS,FCR组为67个月。第9个月时,IR组的 U-MRD 率 (3.9%) 低于 FCR 组 (55.3%),再次证明 U-MRD 不一定与BTKi持续治疗的 PFS 相关。更新的结果(包括MRD 对 PFS 的影响和伊布替尼停药后的至下次治疗时间)将为利用 MRD 检测缩短 BTKi 治疗持续时间提供潜在作用。
MRD与靶向药物一线固定持续时间治疗
已在固定持续时间治疗的临床试验中研究了 MRD 终点。CLL14 是一项关键性随机3期研究,导致 VO 获批用于 CLL 的一线治疗。患者以1:1的比例随机接受 VO 治疗12个月 vs CO 治疗6个月。VO 组等位基因特异性寡核苷酸 (ASO)PCR 和四色流式细胞术测定的 U-MRD4 率高于 CO 组(治疗结束+3个月时为76% vs 35%)。与 CO 相比,接受 VO 治疗的患者可测量疾病的复发也更迟(21个月 vs 6 个月),不仅证明了治疗结束 (EOT) 时达到 U-MRD 的重要性,还突出了不同治疗的 U-MRD 缓解持续时间存在差异。
2期 CAPTIVATE 研究纳入≤65岁 CLL 患者接受一线伊布替尼和维奈克拉(IV) 治疗。患者接受3个月的伊布替尼导入治疗,随后接受12个月的 IV 治疗。研究包括固定持续时间 (FD) 队列和随机 MRD 队列。在 PB 和 BM 中通过八色流式细胞术测量MRD4,而U-MRD 定义为两次单独的 U-MRD 测量结果。EOT 时,PB组75%的患者和 BM 组68%的患者达到U-MRD。在高危亚组中观察到 U-MRD 的高发生率,包括 del17p 和IGHV 未突变患者。在 MRD 队列中,达到 U-MRD 的患者随机接受安慰剂或伊布替尼,未达到 U-MRD 的患者随机接受伊布替尼或 IV 给药。U-MRD队列中,伊布替尼组的4年 PFS 为95%,安慰剂组为88%;未达到U-MRD 队列中,伊布替尼组的30个月 PFS 为95%,IV组为97%。在 FD 队列中,EOT+3时 U-MRD 患者的4年 PFS 率高于可检测到 MRD 的患者 (90% vs 66%),但OS 没有差异。一项2期研究中纳入伴高危遗传特征(即del17p、TP53、del11q或IGHV未突变)的初治 CLL 患者 IV 治疗24个月,观察到相似的结果。EOT(18个联合治疗周期)时的完全缓解率为96%,61%的患者最初在 BM 中达到U-MRD,随着随访时间的延长,75%的患者在 BM 中达到 U-MRD 作为最佳缓解,相关的3年 PFS 为93%。
3期 GLOW研究纳入≥70岁或不适合CIT的CLL患者,对比固定持续时间 IV 与 CO 一线治疗,并通过NGS评估MRD4和 MRD5。在EOT+3时IV 组的 MRD5 率高于CO组,包括BM 和 PB 中(BM 40.6%和PB 43.4% vs 7.6%和18.1%),且EOT+12时PB 的 MRD5 率同样如此(36.8% vs 6.7%)。与 CO 组相比,IV组更有可能维持U-MRD,而CO的U-MRD持续时间更短。IV 组无论BM为 U-MRD4或MRD4可检测,其PFS 无显著差异 (96.3% vs 93.3%),表明无论是否达到 U-MRD 状态,PFS均极佳。
CLL13研究比较了维奈克拉联合方案与CIT,将fit患者以1:1:1:1的比例随机分配接受CIT(FCR 或苯达莫司汀-利妥昔单抗 [BR])治疗6个周期、维奈克拉-利妥昔单抗 [VR] 治疗12个周期、VO 治疗12个周期或维奈克拉-奥妥珠单抗-伊布替尼[VOI] 12个周期,共同主要终点为第15个月(即EOT+3)时的U-MRD4和PFS。结果VO和 VOI 组 PB 和 BM 中 U-MRD4 的发生率高于CIT(分别为72.5%、77.9%、37.1%)。在中位随访38.8个月时,VO、VOI和 CIT 的3年 PFS 分别为76.4%、82.9%和65.5%。在15个月时,与 CIT 相比,含维奈克拉方案的 U-MRD 与 PFS 改善相关,但双联和三联联合方案之间无显著差异。
上述 MRD 与 PFS 相关性差异的潜在原因是什么?GLOW 的随访时间短于CAPTIVATE,考虑到连续 BTKi 治疗的长期 PFS 获益,观察含 BTKi 方案的 PFS 差异可能需要更长时间。重要的是,GLOW入组了老年人群,研究中报告了几例死亡;表明在为老年患者人群选择治疗时需要考虑方案的毒性,并且在某些人群中由于方案相关毒性,达到 U-MRD 可能并非最佳。
临床案例(续)
JT 想开始阿可替尼单药治疗。在这种情况下不建议检查 MRD 检测,因为结果与 U-MRD 状态相关性不佳。接受阿可替尼治疗5年后,患者出现疾病进展,并开始接受 VR 治疗。患者询问 MRD 检测,是否应该现在进行检测。
MRD与靶向药物的复发/难治治疗
鉴于一线 CIT 治疗后 U-MRD 缓解患者的 PFS 和 OS 改善,在接受靶向药物治疗复发/难治性 CLL 的患者中探索了 MRD 作为终点。MURANO 是比较 VR 与 BR 治疗复发/难治性 CLL 患者的实用的3期临床试验,通过 ASO-PCR 和四色流式细胞术评估MRD。在最近的更新中,VR治疗患者的7年 PFS 为23%,而 BR 治疗患者为0%;7年 OS 率分别为69.6%和51%(HR=0.53)。对于 EOT 时未发生疾病进展的 U-MRD 患者,中位 PFS 为52.5个月,而MRD 可检测的患者为18个月,表明在 VR 治疗结束时达到 U-MRD 的患者 PFS 延长,在这种情况下U-MRD状态可能是预后因素。
CLARITY 研究是一项2期研究,使用 IV 联合方案治疗复发性 CLL 患者,并在联合治疗12个月后观察 PB 和 BM 中 MRD4 作为主要终点。与 CLL14 和 MURANO 不同(所有患者在12个月时停止治疗,无论 MRD 状态如何),如果 U-MRD 得到证实,患者可以在8-26个月的任何时间停止联合治疗;如果患者在26个月时未U-MRD4,则继续伊布替尼治疗。治疗14个月时,36%(19/53) 的患者 BM 达到U-MRD,53%(28/53) 的患者在14个月时 PB 达到U-MRD(12个月联合治疗)。到第26个月时,U-MRD缓解加深 (44%[11/25])。23例 U-MRD 患者已停止所有治疗,14/18例在38个月时仍为U-MRD4。这些数据表明,IV应答可随时间推移而加深;在停止治疗期间、至下次治疗期间进一步随访 PFS 有助于告知靶向U-MRD(尤其是 FD 治疗)是否可改善结局。
MRD与细胞治疗
异基因干细胞移植仍是fit高危 CLL 患者治疗模式的一部分,具有治愈潜力,尽管考虑到新型靶向治疗的疗效,异基因干细胞移植使用频率较低。关于移植后U-MRD的前瞻性数据有限。德国 CLL3X 研究观察了低危复发/难治性 CLL 患者的减低强度预处理异基因干细胞移植,发现存活患者(包括 del17p 患者)在12个月时的 U-MRD 率为52%。此外,12个月时的 U-MRD 是复发风险降低的预后因素,6年 OS 为58%,无论高危基因特征如何。
CAR-T 细胞最初是在 CLL 患者中研究的,早期研究具有持久缓解。几种产品目前正在研究中,并已证明能够实现U-MRD,即使是在高危患者中。一项在伊布替尼治疗期间疾病进展的患者中开展的 CD19 CAR-T 细胞治疗联合伊布替尼研究表明,4周总缓解率为83%,61%的患者达到U-MRD。一项在复发/难治性 CLL 患者中开展的1-2期lisocabtagene maraleucel研究表明,CR率为18%,总缓解率为43%。PB 和 BM 的 U-MRD 率分别为63%和59%。U-MRD 患者的中位 PFS 为26.2个月,而MRD可检测的患者为2.8个月。这些数据证明了细胞治疗对 U-MRD 的预后价值,但还需要对 CAR-T 细胞进行更长时间的随访以确定缓解的持久性。
临床案例(续)
VR 治疗两年后,在 EOT 时使用四色流式细胞仪检查U-MRD,并在0.02%的细胞中检测到克隆。
MRD是否准备好进入黄金时代?
EOT 时的 U-MRD 已证明了多种 CLL 治疗的重要预后价值,包括CIT、维奈托克联合治疗和细胞治疗。因此,如果检测随时可用,在这些有限治疗结束时评价 U-MRD 状态是合理的。目前,MRD检测对生存的价值需要在未来的联合治疗方案中进一步研究,因为尚不清楚 MRD 驱动的治疗方案是否会标准化。目前,没有证据表明 MRD驱动治疗应在临床试验之外使用。U-MRD 仍是临床试验的一个有吸引力的终点,因为许多关键临床试验尚未达到中位OS,因此需要替代终点。
虽然 U-MRD 是预后因素,但其他疾病特异性因素仍会影响结局。具有高危基因组特征(如 del17p 和IGHV未突变)的患者的 U-MRD 发生率与低危患者相似,但 PFS 持续缩短,表明基于疾病生物学的 MRD 动力学存在潜在差异。截至目前,尚无明确证据表明如何基于 MRD调适治疗。BOVen研究使用泽布替尼、维奈克拉、奥妥珠单抗三联治疗初治 CLL 患者,89%的患者在中位治疗10个周期后 PB 和 BM 达到 U-MRD 缓解。仍需要更长时间的随访,但 MRD 水平似乎与缓解的持久性相关,94%的患者在额外15.8个月随访后仍为U-MRD。CLARITY 研究进行修订以增加 IV 治疗的持续时间,几乎所有患者在两年结束时停止治疗。FLAIR 研究也采用个体化治疗持续时间,但需要更长时间的随访(特别是在伊布替尼停药后)来确定这是否是一种有效的方法。伊布替尼、IV或 VO 作为 CLL 一线治疗的 CLL17 研究,将有助于确定一线治疗的持续性时间限制性治疗是否最佳,但将该数据转化为二代 BTKi 的结局具有挑战性。
尽管最近有共识指南,但仍有关键的尚未回答的问题:MRD检测的目标水平应该是什么?应使用哪种检测方法?何时和多久进行一次检测,以及使用哪个样本?最后,MRD是否是所有 CLL 患者的正确终点?持续BTKi 治疗的结局极佳,可能无需 U-MRD 来改善所有患者的生存期。
总结
MRD 仍是某些固定持续时间治疗方案缓解评估的有力工具,有可能成为 PFS 的重要替代指标。尽管 MRD 具有预后效用,但仍需要进一步的研究和随访来确定其在常规临床实践中的作用,包括预测和指导常规临床实践中的治疗决策。最后,U-MRD可能并非一刀切的终点,需要考虑患者因素、治疗和所需终点的个体化治疗决策。目前正在进行临床试验以回答这些问题,热切期待这些结果。
参考文献
Rhodes JM,et al.MRD-directed therapy in CLL: ready for prime time ?Hematology Am Soc Hematol Educ Program . 2023 Dec 8;2023(1):413-420.


