【Hemasphere】CAR-T等新疗法显著改善了R/R侵袭性B细胞淋巴瘤生存:西班牙真实世界研究
时间:2024-05-28 19:01:29 热度:37.1℃ 作者:网络
B细胞淋巴瘤真实世界研究
对于复发/难治性(R/R)侵袭性B细胞淋巴瘤(ABCL),近年来很多新疗法逐渐纳入治疗库,如新的单克隆抗体(monoclonal antibodies,MA)、CAR-T细胞、双特异性抗体(BiMA)等。《Hemasphere》近日发表一项西班牙真实世界研究,旨在评估这些新疗法已在多大程度上纳入临床实践,以及如何影响患者生存。

研究结果
该多中心回顾性研究基于西班牙GELTAMO工作组的RELINF注册组平台,纳入2853例具有信息的侵袭性B细胞淋巴瘤患者。353例患者(47.8%)为原发性难治,而139例患者(19%)在诱导治疗完成后3个月至1年内复发;这492例患者合并为“早期复发组”(12个月内复发,占R/R患者的67%)。此外246例患者晚期复发(12个月后复发,33%);其中第二年132例(54%),第三年51例(21%),第四年24例(10%),第五年16例(6%),第六年以后23例(10%)。
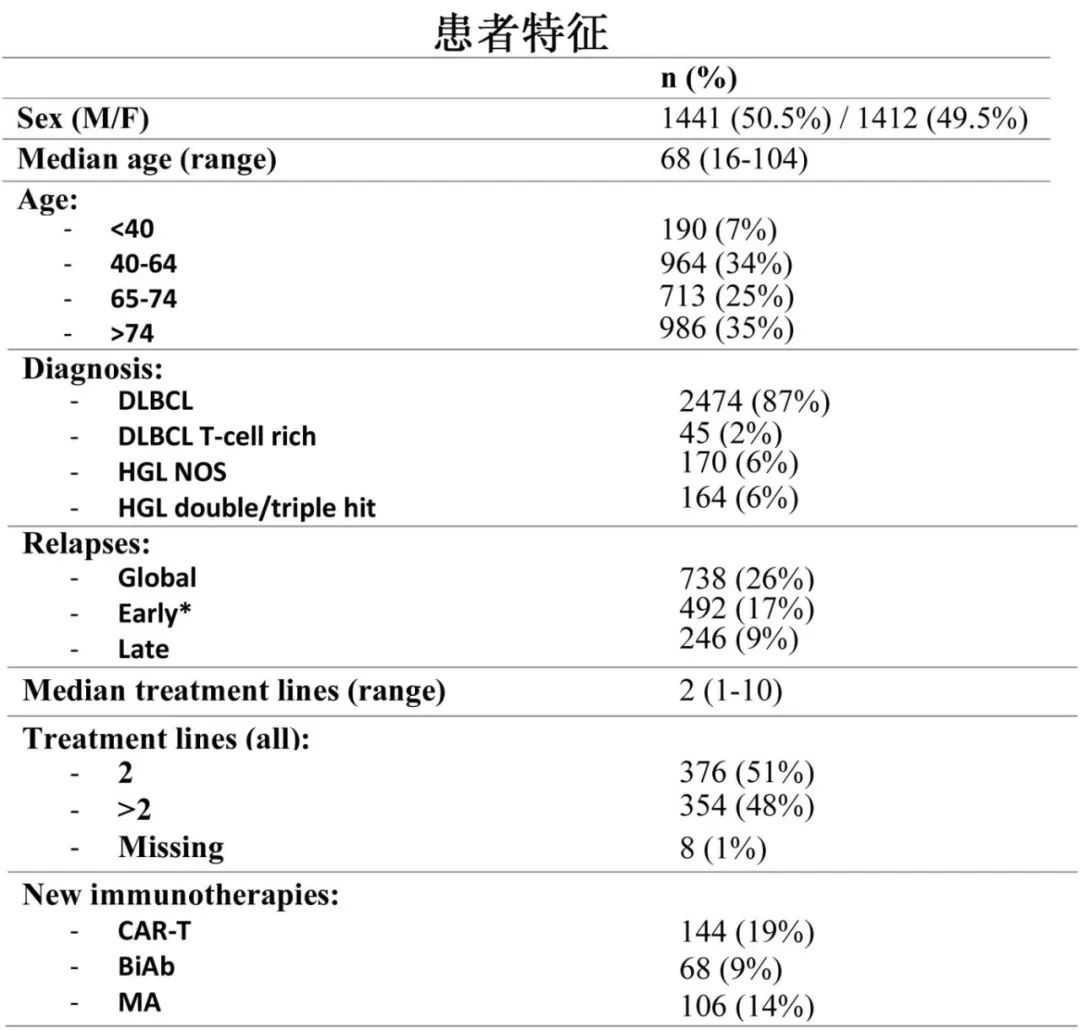
在组织学方面,与DLBCL或HGL NOS(16%)相比,早期复发在双打击/三打击HGL(34%)和富T细胞DLBCL(29%)中最常见(p<0.001)。
在738例有挽救治疗信息的患者中,236例接受新药治疗(NT): 144例接受CAR-T治疗(其中90例作为唯一NT),68例接受BiMA(其中27例作为唯一NT),92例接受维泊妥珠单抗为基础的治疗(46例作为唯一NT),14例接受tafasitamab-来那度胺治疗(12例作为唯一NT),61例接受多个NT治疗。在738例患者中,有730例获得治疗线数的具体信息。R/R患者的中位治疗线数为2线。在接受≥3线治疗的患者中,NT的使用要频繁得多。绝大多数只接受两线治疗的患者(n=376)接受常规治疗(90%),只有38例(10%)接受NT。相比之下,在354例接受≥2线治疗患者中,有194例(55%)接受了NT:130例(67%)接受CAR-T细胞治疗(80例为唯一NT),75例(21%)接受维泊妥珠单抗(35例为唯一NT), 9例(2%)接受tafasitamab-来那度胺(7例为唯一NT),55例(15%)接受BiMA(18例为唯一NT),54例(30%)接受多个NT,而160例(45%)患者没有接受任何NT。175例(74%)患者只接受一种NT, 50例(21%)接受两种联合NT, 11例(5%)接受三种NT。在接受常规治疗和NT治疗的患者之间,复发时间(早期和晚期)没有差异。
中位随访49个月,整个队列的中位PFS为54个月,中位OS为82个月。
在多因素分析中,早期复发(HR=2.91,p<0.001)、总治疗线数(HR=1.4,p=0.018)、年龄≥65岁(HR=1.83,p=0.008)、年龄≥75岁(HR=2.86,p<0.001)、使用CAR-T细胞治疗(HR=0.67,p=0.029)和BiMA治疗 (HR=0.5,p<0.001)对OS有显著影响。
仅考虑738例R/R患者,中位随访时间为40个月,中位OS (mOS2)为16.8个月。接受>2线药物治疗的患者的OS(19个月)长于仅接受两线药物治疗的患者(11个月)(p<0.001)(图1A)。
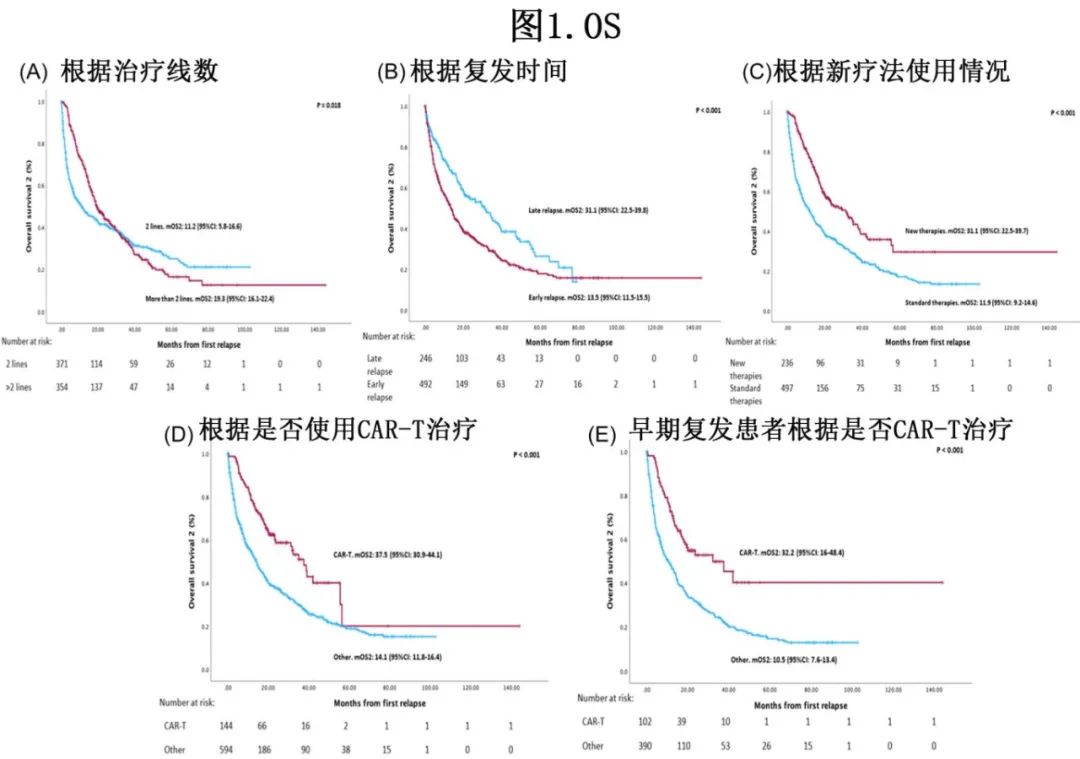
早期复发组的中位OS2显著短于晚期复发组(13.5个月 vs 31.1个月,p<0.001;图1B)。接受NT治疗的复发患者中位OS2为31.1个月,而标准治疗组的中位OS2为11.9个月 (p<0.001)(图1C)。接受CAR-T细胞治疗的患者OS2优于未接受CAR-T细胞治疗的患者(p<0.001)(图1D)。在早期复发患者中,接受CAR-T细胞治疗的患者的中位OS2为32.2个月,而未接受CA-T细胞治疗的患者的中位OS2为10.5个月 (p<0.001)(图1E)。
表1为与OS2相关的因素。多因素分析发现,早期复发(HR=1.68,p<0.001)、年龄≥65岁(HR=1.91,p=0.004)、CAR-T细胞治疗(HR=0.68,p=0.007)、 CAR-T细胞中心(HR=0.7,p<0.001)都是与OS2独立相关的变量。

总结
在真实世界中,年龄和复发时间对侵袭性B细胞淋巴瘤患者的生存有负面影响,其中高级别淋巴瘤等组织学的早期复发风险更高。此外,近年来新药的引入显著提高了生存率,尤其是CAR-T细胞疗法。
参考文献
Bastos-Oreiro M, et al. New therapies for relapsed or refractory aggressive B‐cell lymphoma increase survival: Analysis from the RELINF registry of the GELTAMO group.Hemasphere . 2024 Apr 22;8(4):e70. doi: 10.1002/hem3.70.


