CAR-T治疗后进展LBCL患者的后续治疗及结局
时间:2024-07-02 14:00:35 热度:37.1℃ 作者:网络
研究背景
超过60%的复发/难治性(R/R)大B细胞淋巴瘤(LBCL)患者在接受CAR-T细胞疗法后将出现进展,需要额外的治疗选择。但目前尚没有针对这部分患者的标准治疗方案,患者长期预后不佳,相关的真实世界的结果很少。
本研究为一项回顾性的多中心国际研究,报告了在第三线或更晚的CD19靶向CAR-T细胞治疗后进展的R/R LBCL患者的结果,并提供了一线后续方案后的反应和生存的详细分析。
研究方法
这项研究纳入了387名接受CAR-T细胞治疗后病情恶化的R/R LBCL患者,自输注起中位时间为2.6个月(IQR:1.0-3.3)。
在这些患者中,237例(61%)接受了后续治疗(T组);其余150例(39%)接受了支持性护理或姑息治疗,如单药类固醇或低剂量CT(NT组)。
研究终点
主要终点:OS。其中OS1根据病情进展后接受治疗的情况,对所有患者进行分析;OS2的评估仅适用于T组患者,而不适用于NT组患者。
次要终点:ORR、CR。
研究结果
[1]患者特征
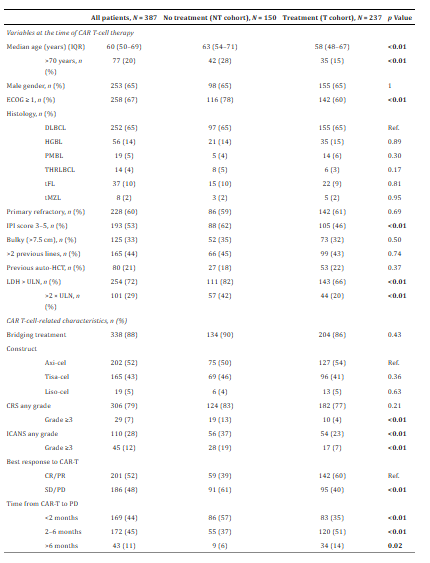
相较于T组患者,NT组患者年龄较大,体能状况较差,并有更多高危IPI评分和乳酸脱氢酶升高的患者;在CAR-T细胞相关数据方面,NT组患者的≥3级CRS、任何级别ICANS 和≥3级ICANS的发生率都高于T组,同时NT组患者早期进展率也更高。
[2]整个人群的结局
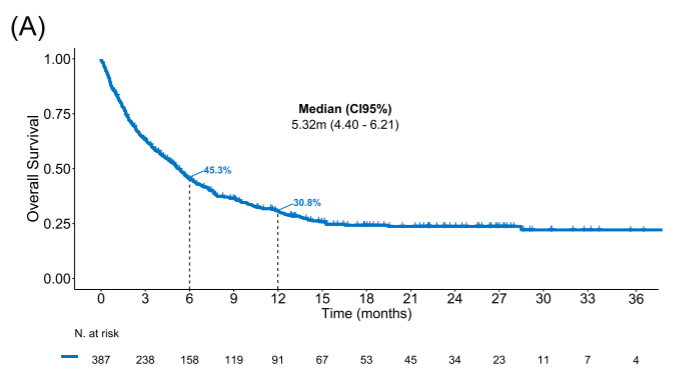
图A:CAR-T细胞治疗进展后中位随访20.4个月,中位OS1为5.3个月,12个月OS1率为31%。
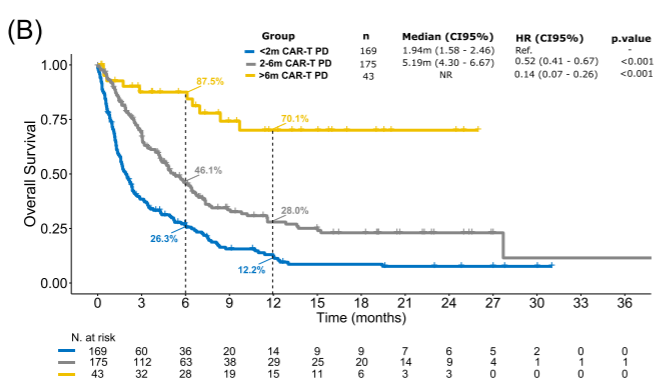
图B:与输注后2-6个月进展和输注后6个月以上进展的患者相比,输注后2个月内进展的患者的中位OS1 (N=169[44%],1.9个月)显著缩短。
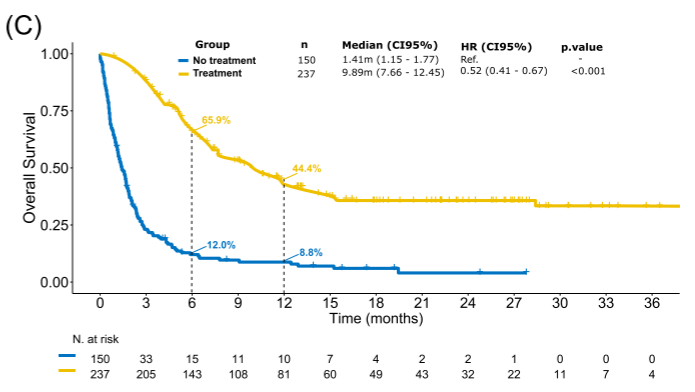
图C:CAR-T失败后的治疗,NT组患者的中位OS1(1.4个月)显著短于T组患者(9.9个月;p<0.01),6个月OS1率分别为12%和66%,12个月 OS1率分别为9%和44%。
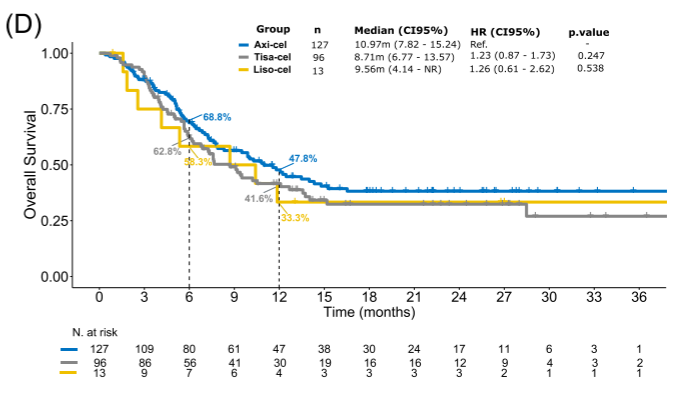
图D:对于T组患者,不同CAR-T细胞产品的中位OS1相似(axi‐cel为10.97个月,tisa‐cel为8.71个月,liso‐ce为9.56个月,p=NS[无统计学意义])()。
[3] CAR-治疗失败后的一线治疗的概况和缓解率
在T组的237例患者中,CAR-T进展后的中位线数为1线。
一线方案包括:
维泊妥珠单抗-利妥昔单抗-苯达莫司汀(POLA) 67例(28%)、
双特异性抗体(BsAb) 34例(14%)、
放疗(RT) 37例(16%)、
免疫检查点抑制剂(ICI) 28例(12%)、
含来那度胺(LENA)方案23例(10%)、
常规化疗41例(17%)、
其他治疗7例(3%)。
211例(89%)患者可评估:
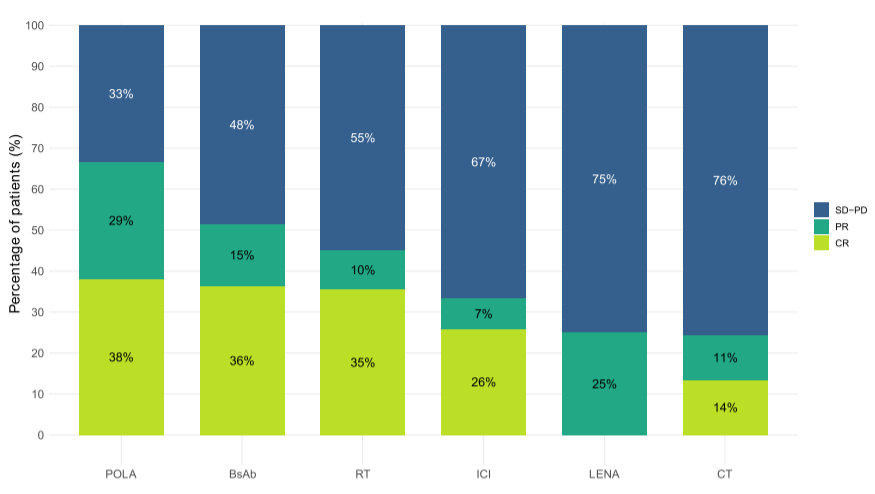
POLA的ORR (CR)为67% (38%),
BsAb为51% (36%),
RT为45% (35%),
ICI为33% (26%),
LENA为25% (0%),
化疗为25%(14%)。
[4] 后续一线治疗的生存结局
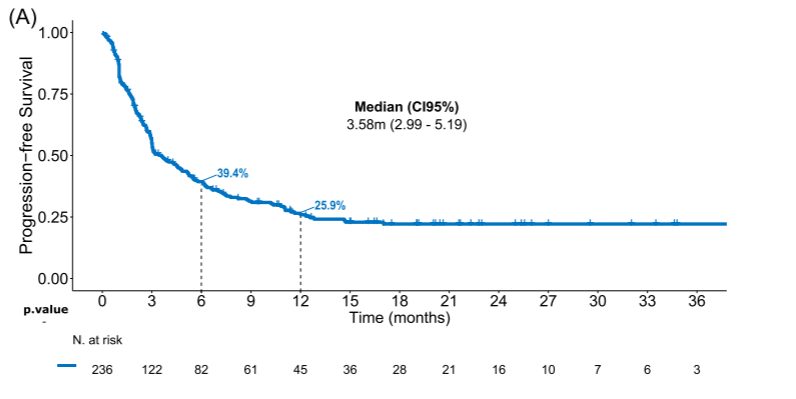
图A:在T组患者中,中位PFS (mPFS)为3.6个月,12个月PFS为26%;CAR-T细胞输注后2个月内进展的患者的mPFS(2.7个月)明显短于2-6个月进展(4.0个月,HR=0.58)和6个月后进展(未达到,HR=0.25)的患者。
疾病组织学方面,高级别B细胞淋巴瘤患者与转化型LBCL患者相比,后续一线治疗的PFS显著缩短(HR=0.53,p=0.044)。
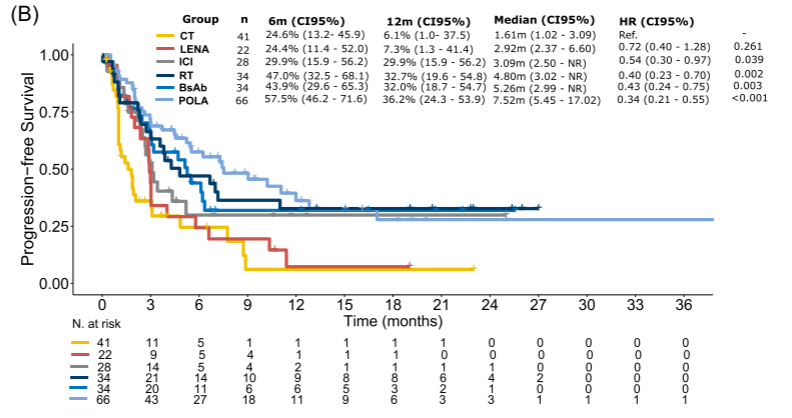
图B:根据后续一线治疗具体到各方案的mPFS(12个月PFS)分别为:
POLA为7.5个月(36.2%),
BsAb为5.3个月(32.0%),
RT为4.8个月(30.8%),
ICI为3.1个月(29.9%),
LENA为2.9个月(7.3%),
化疗为1.6个月(6.1%)。
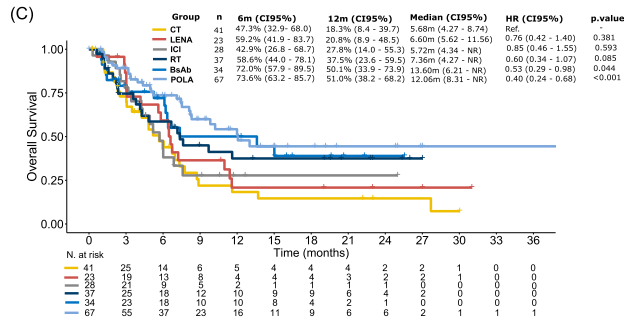
图C:根据后续一线治疗具体到各方案的中位OS2分别为:
POLA为12.1个月(51.0%),
BsAb为13.6个月(50.1%),
RT为7.4个月(37.5%),
ICI为5.7个月(27.8%),
LENA为6.6个月(20.8%),
CT为5.7个月(18.3%)。
[4] CAR-T进展后接受治疗患者的多因素分析
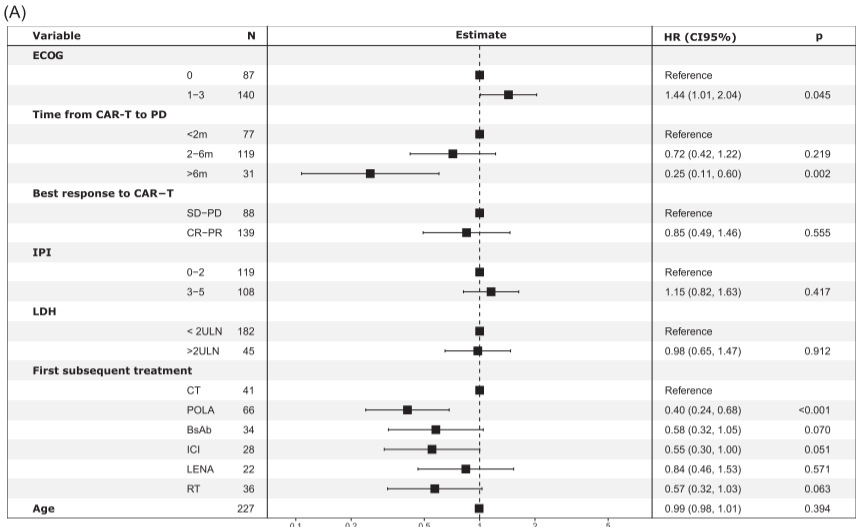
图A:在T组患者的多因素分析中,较好的CAR-T治疗前体能状态(ECOG 0)、CAR-T细胞输注至疾病进展间隔较长(>6个月)以及后续一线POLA治疗与较长的PFS相关。
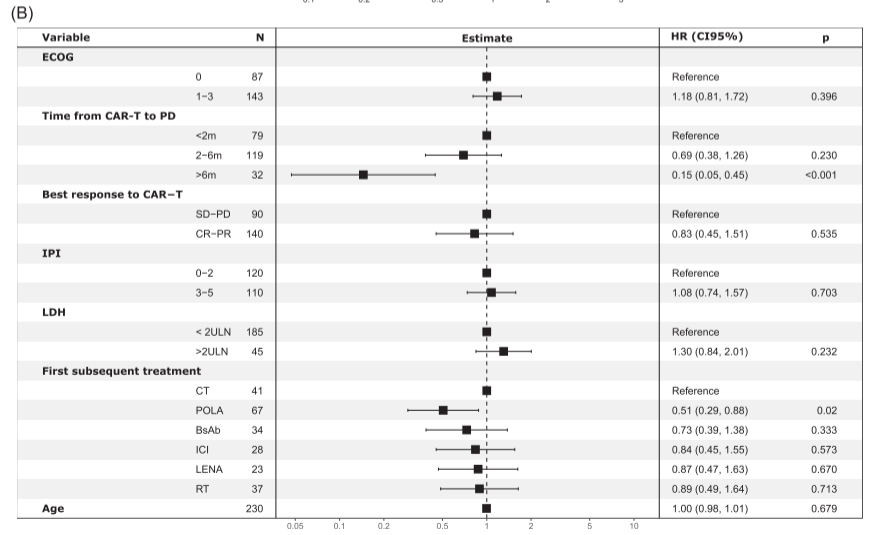
图B:在多因素分析中,从CAR-T细胞输注到疾病进展(>6个月)的间隔较长以及后续POLA治疗对OS保持有利的预后影响。
[5] CAR-T进展后的二线治疗
51例患者(T组237例患者中的22%)在CAR-T治疗失败后接受了二线治疗。
其中3例(6%)接受BsAb, 16例(31%)接受化疗, 15例(29%)接受含维泊妥珠单抗治疗,2例(4%) ICI, 3例(6%)来那度胺为基础方案,3例(6%)RT和9例(18%)其他治疗。
大多数患者对二线治疗的反应率很低,生存期有限。只有14例患者接受三线或后续治疗。
[6]异基因造血干细胞移植巩固的作用
在T组的237例患者中,32例(14%)在CAR-T治疗失败后接受了异基因干细胞移植(allo-HCT)巩固,allo-HCT队列患者明显较其他患者更年轻且体能状态较好。
桥接治疗方案包括POLA (41%)、CT (28%)、ICI (12%)、BsAb (9%)和RT (9%)。
大多数患者在allo-HCT时处于CR (66%)或PR (31%);1例(3%)患者在移植前为PD。
HCT输注后中位随访15.1个月,中位OS未达到,12个月OS为84%。
在数据截止时,7例(22%)患者死于PD (N= 4)、巨细胞病毒脑炎(N=1)、移植物抗宿主病(N=1)和其他原因(N=1)。
研究结论
CAR-T细胞治疗后进展的LBCL患者的预后较差,尤其是2个月内早期进展的患者。新型靶向药物(如维泊妥珠单抗和双特异性抗体)可以在CAR-T细胞治疗失败后延长生存期。对于后续治疗缓解的患者,可以考虑异基因造血干细胞移植巩固。
参考文献
[1] Iacoboni G, Iraola-Truchuelo J, O'Reilly M, Navarro V, Menne T, Kwon M, Martín-López AÁ, Chaganti S, Delgado J, Roddie C, Pérez A, Norman J, Guerreiro M, Gibb A, Caballero AC, Besley C, Martínez-Cibrián N, Mussetti A, Sanderson R, Luzardo H, Iyengar S, Sánchez JM, Jones C, Sancho JM, Barba P, Latif AL, López-Corral L, Hernani R, Reguera JL, Sureda A, Garcia-Sancho AM, Bastos M, Abrisqueta P, Kuhnl A. Treatment outcomes in patients with large B-cell lymphoma after progression to chimeric antigen receptor T-cell therapy. Hemasphere. 2024 May 21;8(5):e62. doi: 10.1002/hem3.62. PMID: 38774657; PMCID: PMC11106798.


