Psychiatry Research: 患者来源的诱导多能干细胞:促进重度抑郁症理解和药物发现的工具
时间:2024-07-07 14:00:46 热度:37.1℃ 作者:网络
重度抑郁症(MDD)是一种多态性疾病,表现出多种症状和严重程度的模式,并在多个相关领域存在可测量的缺陷。诊断为抑郁症的患者所观察到的广泛表型反映了这种非常复杂的疾病,其中生物和外部因素(例如生活事件的反应/处理、内心理因素)汇聚并介导发病机制、临床表现/表型和轨迹。患者来源的诱导多能干细胞(iPSCs)允许将其分化为中枢神经系统中的特化细胞类型,以探索MDD的病理生理学基础。这些模型可以补充动物模型,以促进药物发现和确定治疗方法,如细胞疗法、药物再利用,并在分子/细胞水平上阐明药物代谢、毒性和作用机制,为精准精神病学铺平道路。尽管在过去几十年中取得了显著的科学和临床进展,但该疾病仍然理解不足,其发病率和患病率继续增加,需要更多研究以满足临床需求。

本文旨在总结并对迄今为止使用患者来源的iPSCs进行精神疾病建模的研究进行批判性概述,特别是针对MDD。iPSCs可以从体细胞重编程得到,通常是成纤维细胞和外周血单核细胞,通过mRNA、表观染色体、微环、piggyBac转座子、重组蛋白和含有表达四种重编程因子Oct4、Sox2、Klf4和c-Myc的重组病毒载体的仙台病毒获得。因此,iPSCs可以分化为与供体具有相同遗传背景的细胞,表现出与疾病相关的表型,再现健康和病理组织、器官发育、分子和病理生理途径,从而推动药物开发的新分子靶点的发现。共培养或更复杂的结构,包括脑类器官、组装体和芯片上的类器官/器官被用来开发更真实的疾病模型。
iPSCs衍生的神经元细胞已成为研究人类疾病、筛选候选药物和重新利用药物的重要工具。这些细胞提供了关于人类独特的遗传和表观遗传景观的重要信息,有助于克服获取人类组织的伦理和技术挑战。通过改进重编程过程和基因编辑工具(如CRISPR/Cas9基因编辑)来引入纯合或杂合的修饰,提高了这些细胞的可扩展性和临床相关性,使其成为研究中无限获取人类细胞的资源。为了实现这一目标,正在努力改进iPSCs分化为更多功能、成熟的神经元细胞的方法,这些细胞表达特定脑区的标志物,这些脑区被认为是精神疾病的核心。 在中枢神经系统中,通过模式信号分子来操纵和丰富细胞环境,以诱导神经分化为区域特异性神经元。
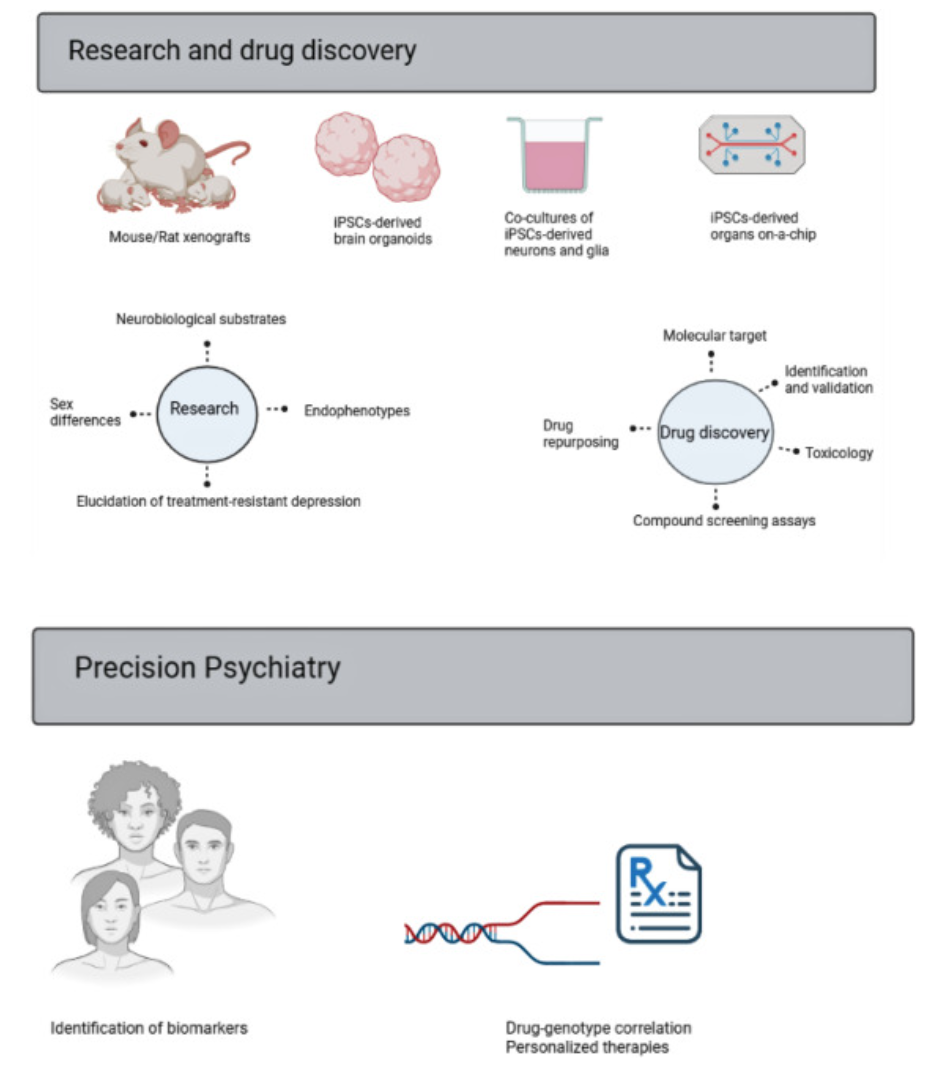
图1. 诱导多能干细胞(iPSCs)模型探索重度抑郁症(MDD)神经生物学基础的潜力,并有助于理解塑造疾病发生的遗传和表观遗传因素和性别差异
最近,研究团队成功地诱导了无饲养层iPSCs分化为表达特定脑区标志物的神经祖细胞(NPCs)。这些NPCs进一步分化为前脑皮层神经元、前脑中间神经元、中脑多巴胺能神经元和脊髓运动神经元。此外,通过补充细胞环境中Sonic Hedgehog(SHH)信号通路拮抗剂、WNT、转化生长因子β、骨形态发生蛋白、Noggin路径,成功诱导了类似于海马齿状回(DG)中发现的NPCs的分化,并从患有精神分裂症的患者中生成并共培养了DG-CA3神经元,以探索内在的神经元活动。
iPSCs衍生的神经元细胞的功能性质的评估对于验证这些模型至关重要。常规进行电生理学分析以检查神经元功能和成熟的标志,包括阈值、上升时间、幅度、半高宽和后超极化幅度、钙、钾和钠电流以及配体门控的GABA受体等。自动贴片夹系统允许对悬浮细胞或包含多/微电极阵列(MEAs)的平台中的细胞进行电生理分析。这些技术的结合可以检测离子通道、神经受体中的异常,并测试药物与离子通道的动态相互作用、药物结合/解离、质子化/去质子化以及药物对离子通道的机制调节在靶向疾病中的相关性
MDD与神经回路完整性的广泛系统功能障碍相关。iPSCs模型的整合将多维度的精神病理学、标志物和数据纳入考量,对于跟踪结果,包括症状进展和高风险患者的表型具有重要意义。尽管研究抗抑郁药在患者来源的iPSCs模型中的作用机制尚未普及,但它肯定会为未来的临床研究提供更有力的证据,并在大规模上实现个性化精神病学。在临床环境中,纵向随访所有年龄、性别和不同严重程度的MDD患者,并使用标准程序收集血液样本和临床数据,将有助于生成有力的证据,以确定表观遗传变化和其他分子/细胞因子,这些因子会影响MDD的风险和/或恢复能力,并生成进展标志物。避免将分析限制在病例对照研究上,并专注于寻找不同情况下的差异,这将扩大对疾病不同维度的理解。
原始出处:
Vaz, A., Salgado, A., Patrício, P., & Pinto, L. (2024). Patient-derived induced pluripotent stem cells: Tools to advance the understanding and drug discovery in Major Depressive Disorder. *Psychiatry Research*, 339, 116033. https://doi.org/10.1016/j.psychres.2024.116033


