邓婷教授:2024年ASCO胃癌围手术期化疗新策略及生物标志物探索
时间:2024-07-09 14:00:26 热度:37.1℃ 作者:网络
编者按:2024年6月11日,第14届CGOG大会成功开幕,众多消化道肿瘤学专家、学者通过线上平台汇聚一堂,共同探讨胃癌治疗的最新进展。在本次大会的首场专题——胃癌ASCO速递中,天津医科大学肿瘤医院的邓婷教授为我们深入探讨了化疗及多维度研究在胃癌治疗中的应用,进一步丰富了我们对胃癌治疗策略的认识。
基于化疗的研究
OGSG1902研究
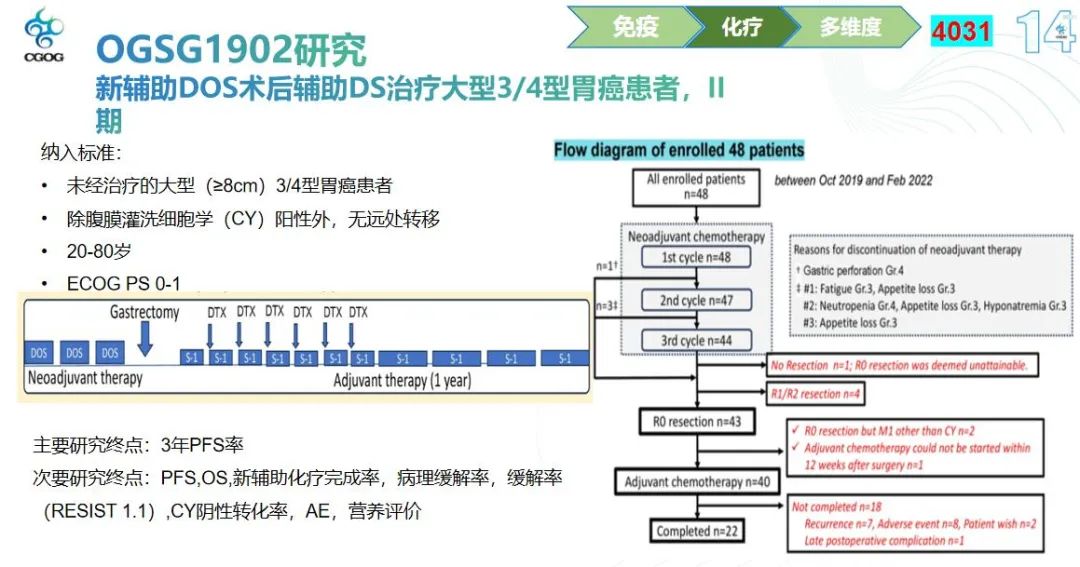
OGSG1902研究是一项针对大型3/4型胃癌患者的II期临床研究,专注于新辅助(术前)和辅助(术后)治疗。该研究特别关注的是肿瘤直径大于8厘米的3/4型胃癌患者,且CY阳性而无远处转移。研究设计包括在术前进行三个周期的新辅助DOS治疗,术后则给予一年的S-1及六个周期的多西他赛的联合治疗,形成了一个强化的围手术期治疗方案。
研究的主要终点为3年的无进展生存率(PFS)。共有48例患者被纳入研究,其中91.7%的患者完成了新辅助治疗,在可测量病灶的患者中,有50%达到了客观缓解(ORR),而在CY阳性的患者群体中,80%的患者实现了转阴。
从这些初步结果来看,新辅助DOS治疗的有效率是令人鼓舞的。尽管整体方案的完成率为45.8%,略低于50%,但这与我们过去在围手术期治疗中观察到的完成率相似,通常在50%左右。值得注意的是,尽管纯化疗模式下的病理完全缓解率(PCR)较低,但整体的有效率和主要病理缓解率(MPR)达到了66.7%,显示出治疗的有效性。此外,治疗的安全性也是可接受的。这些发现为我们提供了对胃癌治疗新策略的深入理解,并为未来的研究方向奠定了基础。
IKF-575/RENAISSANCE 研究
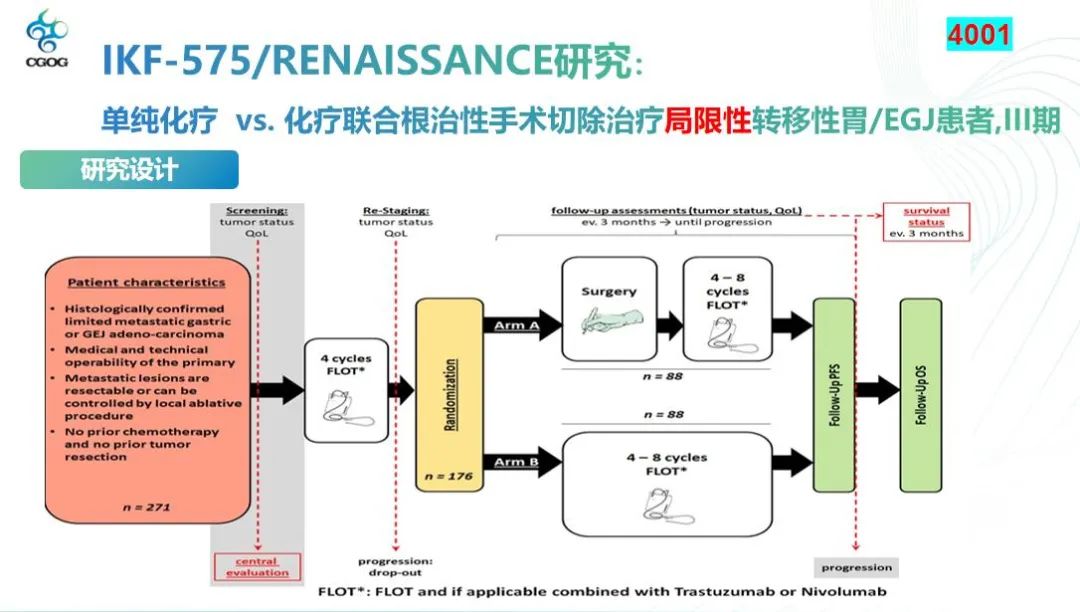
在探讨局限期转移胃癌患者的治疗策略时,我们一直在探索转化治疗的潜力,即手术是否能使一部分晚期患者得到显著的生存获益。IKF-575研究是基于FLOT3的研究开展的随机对照III期研究,旨在评估手术是否能够为局限期转移的患者带来生存上的优势。研究纳入了具有一定局限性转移的患者群体,并给予了四个周期的FLOT方案治疗。随后,患者被随机分配到两组:一组接受手术治疗并于术后进行辅助围手术期化疗;另一组则继续接受FLOT方案的化疗。
在基线特征方面,两组患者在性别、年龄、分期、转移情况以及远处淋巴结转移比例等方面均保持了较好的均衡性。在随机化前,所有患者均完成了四个周期的FLOT治疗。然而,在随机化后,我们观察到A组(手术组)在术后的化疗完成率出现了显著下降,只有66%患者术后接受化疗,而完成围手术期12周期的患者只有4%。术后患者的化疗接受程度是明显下降的。
在B组(非手术组)中,有39%的患者完成了12个周期的连续FLOT治疗,而完成8个周期的患者比例达到了74%。在远处淋巴结转移的亚组中,56%的患者成功切除了原发灶和转移病灶,而在其他器官转移的亚组中,53%的患者进行了原发灶和转移灶的切除,仅切除原发灶的患者占40%。此外,A组中有20%的患者接受了再手术,而90天的死亡率在手术组中相对较高。
在总体生存分析中,两组的生存曲线出现了交叉,中位生存期两组没有差异。有20%的患者有较长的生存期。在亚组分析中,对于远处淋巴结转移人群,可能手术组的患者更为获益。中位总生存时间从17.1个月延长至29.6个月。对于肝转移患者,两组的生存曲线一直非常接近,而对于腹膜转移患者,手术似乎并未带来更好的生存结果,甚至可能更差。
此项研究提示在未来的治疗中,对于局限性转移的晚期胃癌患者,需要对患者进行更细致的分层,探索哪些患者群体能够从手术治疗中获益。
真实世界局部晚期胃癌的辅助FLOT与XELOX化疗的长期生存比较
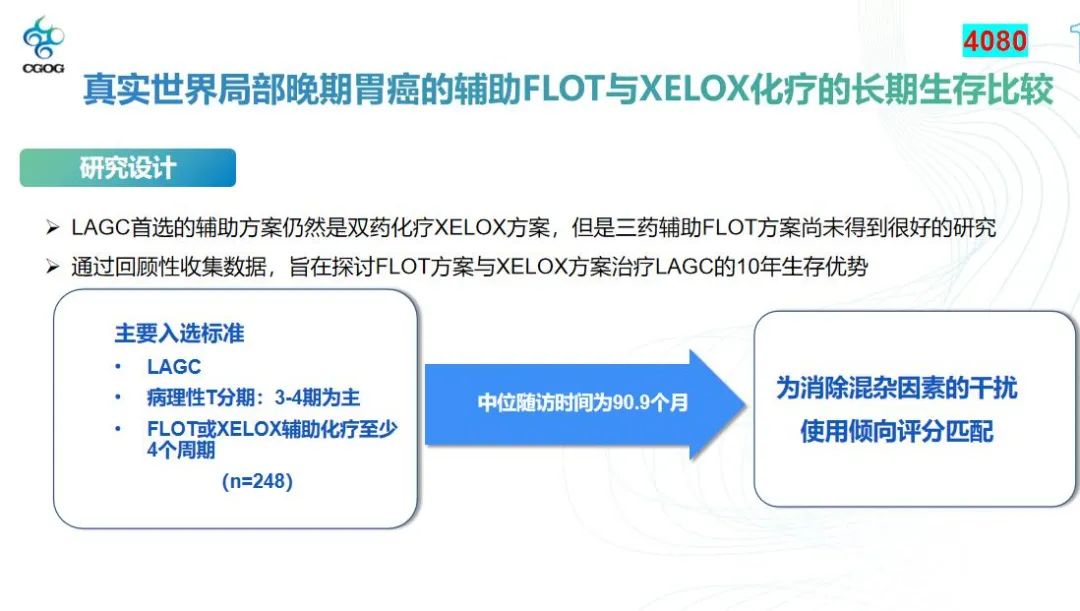
在化疗领域,FLOT(氟尿嘧啶、亚叶酸、奥沙利铂和多西他赛)方案作为辅助治疗在胃癌治疗中已经显示出其潜力。尽管目前还没有随机对照研究直接比较FLOT与XELOX(卡培他滨和奥沙利铂)方案,但基于回顾性数据分析,我们能够观察到一些有趣的趋势。
这项研究比较了局部进展期胃癌患者在术后使用FLOT方案与XELOX方案的10年生存结果。研究结果显示,FLOT方案组的中位总生存期(OS)为44.8个月,而XELOX方案组为34.87个月。在5年生存率方面,FLOT方案组为41.4%,XELOX方案组为25.3%;10年生存率则分别为31.9%和11.8%。这些数据表明,ECOG评分为0或具有T3-4分期的患者在接受三药辅助FLOT方案治疗时,可能获得显著的生存获益。
此外,FLOT方案经过多年的临床应用,整体的安全性和耐受性得到了认可。在今年ASCO年会上,有关食管腺癌的研究也汇报了放化疗与FOLT方案的比较,结果显示FOLT方案在某些情况下表现更优。这些发现促使我们思考,如果术后辅助治疗能够更加强化,是否能够进一步延长患者的生存期。
生物标志物的研究
PLAGAST研究
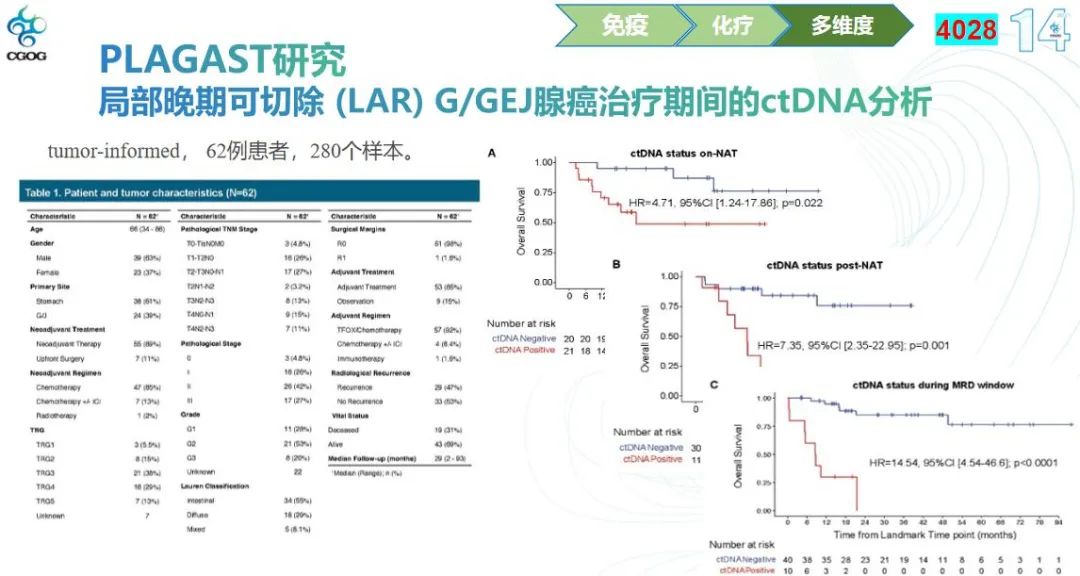
在结直肠癌领域,循环肿瘤DNA(ctDNA)和微小残留病灶(MRD)的研究已经取得了显著进展,而在胃癌领域,我们仍处于探索阶段。PLAGAST研究针对局部晚期胃癌患者,采用了肿瘤知情策略(tumor-informed)模式,通过在新辅助治疗前、中、后以及手术后的MRD窗口期采集了280个ctDNA样本,来探索其与疗效的相关性。
研究结果显示,在新辅助治疗期间,ctDNA阴性与阳性患者的生存曲线存在明显差异。如果新辅助治疗后ctDNA仍为阳性,生存差异进一步加大,预后更差。此外,如果在MRD窗口期进行ctDNA检测,呈现阳性结果,患者的预后会进一步降低。
ctDNA的动态变化对于评估治疗效果和预测预后具有重要意义。无论是无病生存率(RFS)还是总生存率(OS),ctDNA的清除与更好的预后一致。在术后病理分级(TRG)方面,ctDNA阴性且TRG为1~3级的患者整体生存更佳。相反,如果TRG为4~5级,无论ctDNA阴性或阳性,患者的RFS和OS均较差。
本研究显示"tumor-informed" ctDNA有助于指导胃癌新辅助治疗后的临床决策。
总结
胃癌围手术期治疗模式的布局,包括联合免疫治疗的策略,有待III期结果来指导临床实践,也需要进一步选择优势人群,在精准治疗的框架下进行排兵布阵的模式优化,让患者获得更长的生存。


