Circ Res:南京医科大学陈琪/张瀚文合作揭示了参与肥胖引起的心功能障碍的关键巨噬细胞群!
时间:2024-07-29 14:00:21 热度:37.1℃ 作者:网络
巨噬细胞是肥胖相关心血管疾病的关键参与者,其特征是炎症和免疫改变。然而,巨噬细胞在肥胖引起的心脏炎症中的病理生理机制尚不完全清楚。
2024年7月26日,南京医科大学陈琪、张瀚文共同通讯在Circulation Research在线发表题为“Lysozyme 1 Inflamed CCR2+ Macrophages Promote Obesity-Induced Cardiac Dysfunction”的研究论文,该研究确定了参与肥胖引起的心功能障碍的关键巨噬细胞群,并揭示了促进炎症反应的分子机制。
研究人员发现Ccr2簇经历了从稳态维持到促炎症的功能转变。强调了代谢挑战下心脏功能障碍时巨噬细胞行为的特定变化。一致地,通过双重重组酶谱系追踪方法或选择性删除巨噬细胞C-C趋化因子受体2 (CCR2)诱导消融CCR2+CX3CR1+巨噬细胞可预防肥胖诱导的心功能障碍。在机制水平上,证明了肥胖诱导的巨噬细胞表达CCR2的功能转移是由CCR2/ATF3/lysozyme 1/NF-κB(核因子κB)信号通路介导的。研究结果表明,lysozyme 1作为转录激活因子的非规范作用,它与RelA启动子结合,驱动NF-κB信号传导,并在肥胖中强烈促进炎症和心功能障碍。

肥胖引起心脏和全身炎症,而这种炎症主要由巨噬细胞介导心脏巨噬细胞是散布在心脏内的异质细胞群。在稳态状态下,大部分心脏巨噬细胞来源于胚胎发育期间的造血祖细胞。心脏巨噬细胞对C-C趋化因子受体2 (CCR2)呈阴性,在免疫监视、炎症消退、组织修复和电传导中发挥作用。随着时间的推移,单核细胞来源的巨噬细胞(MDMs)起源于骨髓中的造血干细胞并迁移到心脏;这些细胞是自我再生的,主要是CCR2+,但功能难以捉摸。
肥胖等压力会促使单核细胞从循环系统向心脏聚集,并在心脏分化为巨噬细胞。基于CCR2阳性,MDMs由2个不同的亚组组成CCR2+ MDMs具有促炎作用,因为它们能够通过表达趋化因子,如C-X-C趋化因子配体2、C-X-C趋化因子配体5或C-C基序趋化因子配体2 (CCL2)和CCL7,将中性粒细胞和单核细胞募集到心肌中。CCR2+ MDMs还促进单核细胞向巨噬细胞分化,分泌IL(白细胞介素)-1β、IL-6、TNF-α(肿瘤坏死因子-α)等炎性细胞因子,产生活性氧,导致心脏结构和功能受损。然而,CCR2+巨噬细胞是否在应激反应中具有功能性适应尚不清楚。
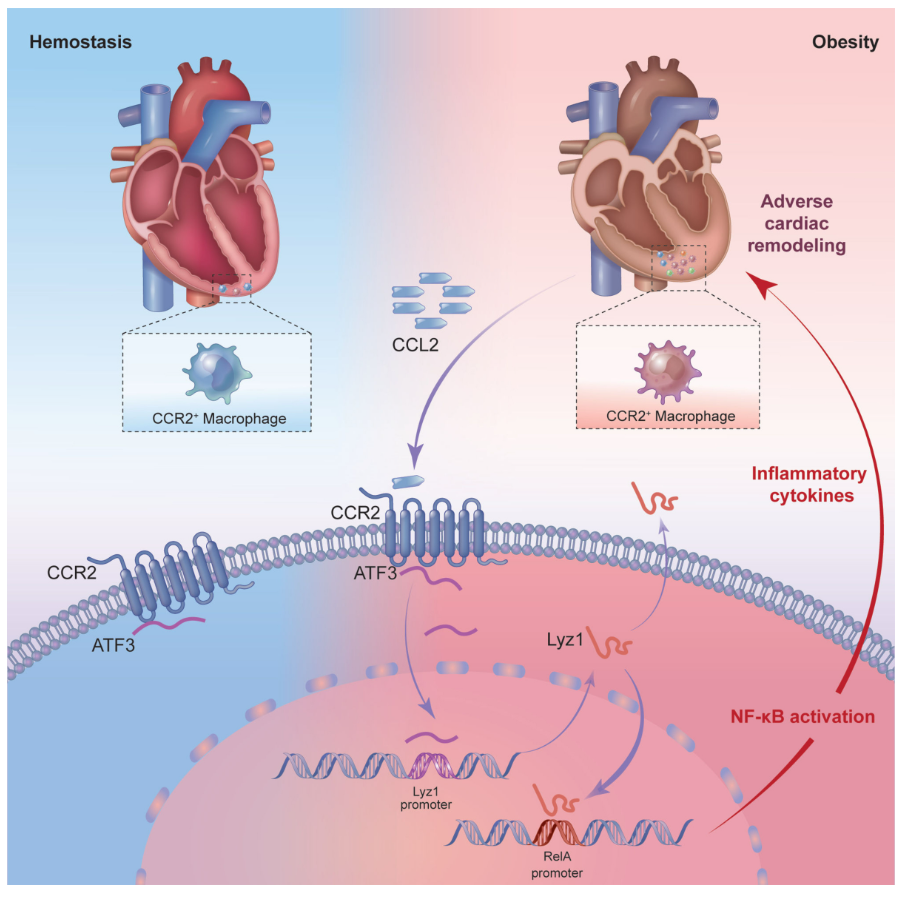
机理模式图(图源自Circulation Research)
在该研究中,作者通过单细胞RNA测序(scRNA-seq)分析发现CCR2+心脏巨噬细胞经历了从稳态维持到促炎症的功能转变,并证明细胞内溶菌酶1 (Lyz1),一种能够激活Toll样受体的溶菌酶是巨噬细胞中CCR2激活的关键介质。此外,Lyz1通过促进NF-κB(核因子κB)通路RelA的转录激活CCR2+巨噬细胞,从而加剧巨噬细胞介导的炎症和肥胖诱导的心功能障碍。综上所述,Lyz1可能是CCR2+巨噬细胞在肥胖应激反应中通过多种机制放大炎症的关键触发因子。靶向Lyz1可能是预防和治疗肥胖引起的心脏病的一种很有前途的方法。
参考信息:
https://www.ahajournals.org/doi/10.1161/CIRCRESAHA.124.324106#con21


