Cancer Letters:潜在基因治疗“药物”—环状RNA可通过编码肽抑制神经母细胞瘤
时间:2024-09-01 18:00:26 热度:37.1℃ 作者:网络
神经母细胞瘤(NB)是儿童最常见颅外实体恶性肿瘤,被称为“儿童肿瘤之王”。约50%的患儿在诊断时已出现远处转移,该类患儿即便接受包括手术、大剂量化疗、放疗和自体造血干细胞移植在内的多种治疗方案,其5年总生存率仍低于60%(New England Journal of Medicine, 2023)。因此,亟需寻找新的治疗策略以改善NB患儿的生存状况。
2023年10月,诺贝尔生理学或医学奖授予了核苷酸类似物修饰mRNA来延长其半衰期和降低免疫原性的研究。当月,Nature 也发文称“环状RNA将是下一代RNA疗法的重磅技术”(Nature, 2023)。相较于mRNA,环状RNA(circRNA)独特的闭合环状结构使其对细胞内的外切酶具有一定抵抗力,从而提高其在细胞内的稳定性;另外,circRNA还具有较低的免疫原性,不易引发免疫系统过度激活,从而降低了产生过敏反应的可能性。这些特点使其在基因治疗中具有显著的优势,有广阔的应用前景。
近期,国家儿童医学中心(北京)/ 国家儿童肿瘤监测中心/ 首都医科大学附属北京儿童医院/ 北京市儿科研究所,儿童肿瘤基础-临床研究团队 倪鑫教授、王焕民教授、金雅琼研究员 为共同通讯作者,首都医科大学附属北京儿童医院 常赛朔博士 、北京市儿科研究所 任冬博士 为共同第一作者,在 Cancer Letters 发表题为Therapeutic SHPRH-146aa encoded by circ-SHPRH dynamically upregulates P21 to inhibit CDKs in neuroblastoma 的文章,深入探讨了circ-SHPRH及其编码肽对NB治疗的重要作用和调控机制。

目前,circRNA在NB中的研究相对有限:以往研究大多集中在circRNA如何促进肿瘤发生和恶性进展,而忽视了对具有抗癌功能的circRNA治疗潜力的探索。本文主要关注由SHPRH反向剪接形成的circ-SHPRH(图1A)主要通过编码肽SHPRH-146aa显著抑制NB恶性进展。因此,circ-SHPRH作为一种罕见的NB肿瘤抑制性circRNA分子,具有潜在的治疗应用价值。
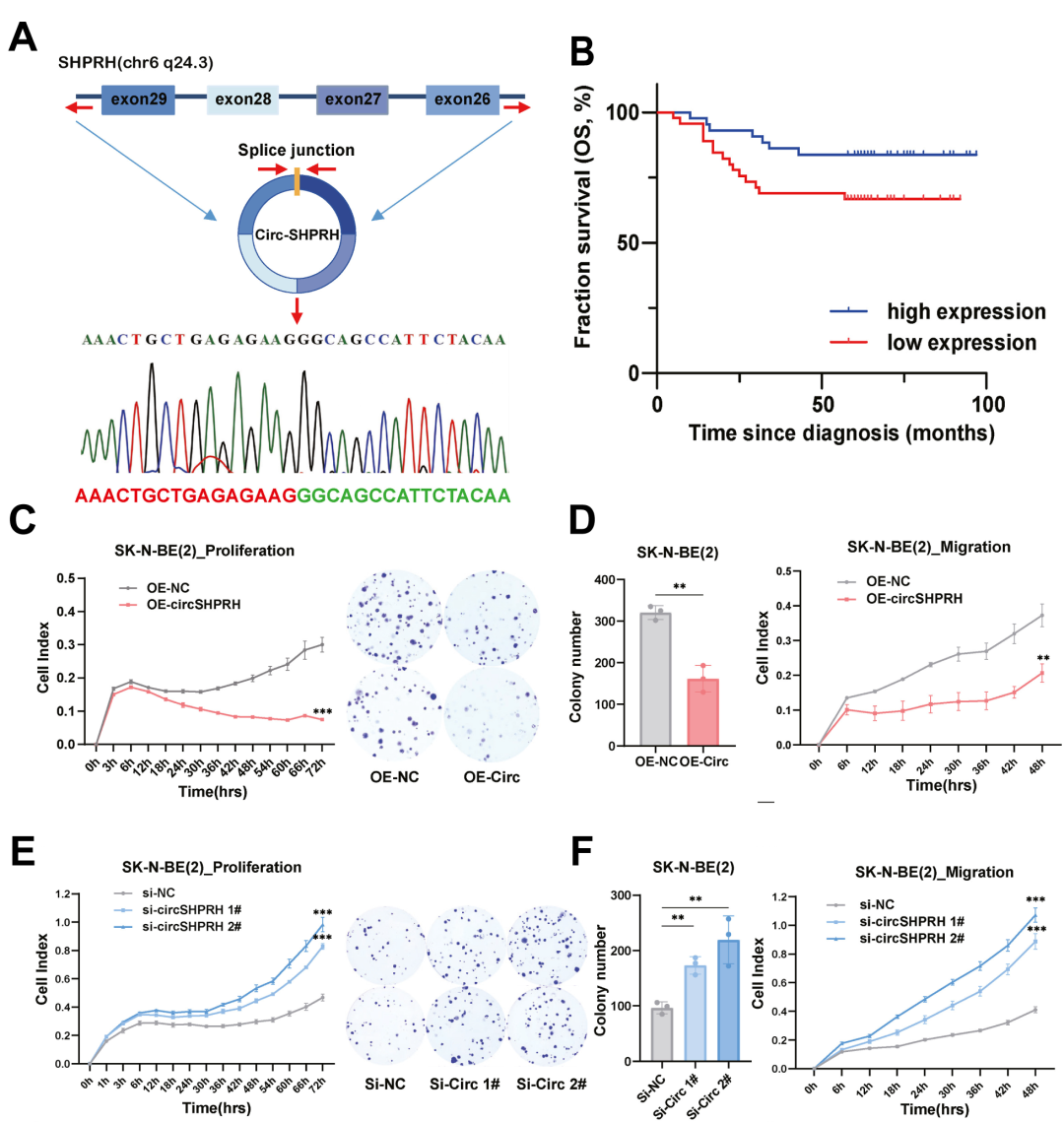
图1 circ-SHPRH与患儿预后正相关及体外实验。A)circ-SHPRH的形成。B)circ-SHPRH与患儿预后良好正相关。C-F)体外试验中,circ-SHPRH对NB的抑制作用。
研究人员在临床样本中发现,circ-SHPRH与患儿预后良好呈正相关(图1B);并通过体外、体内实验明确了circ-SHPRH的NB抑制作用(图1C-F;图2)。机制上,circ-SHPRH主要通过编码SHPRH-146aa诱导P21的表达,从而抑制CDK4-cyclin D复合物活化,进而阻滞细胞周期进程(图3A-C)。可见,circ-SHPRH可作为基因治疗药物,发挥CDK抑制剂的功能。
此外,研究人员还探讨了circ-SHPRH在增强其他小分子药物治疗效果方面的潜力。依维莫司是一种选择性mTOR抑制剂,近年来已广泛用于神经系统肿瘤的治疗。研究发现circ-SHPRH与依维莫司联合应用能显著抑制NB细胞的增殖,进一步提高依维莫司疗效(图3D)。总之,这些发现表明circ-SHPRH有潜力作为NB的一种新的生物标志物和基因治疗药物。
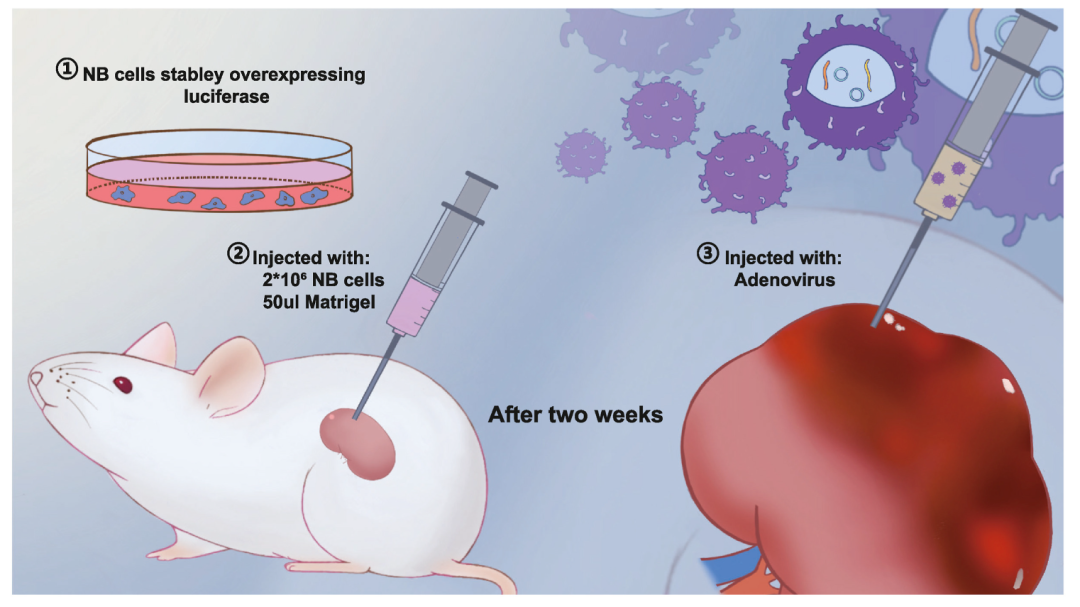
图2 circ-SHPRH体内实验示意图。
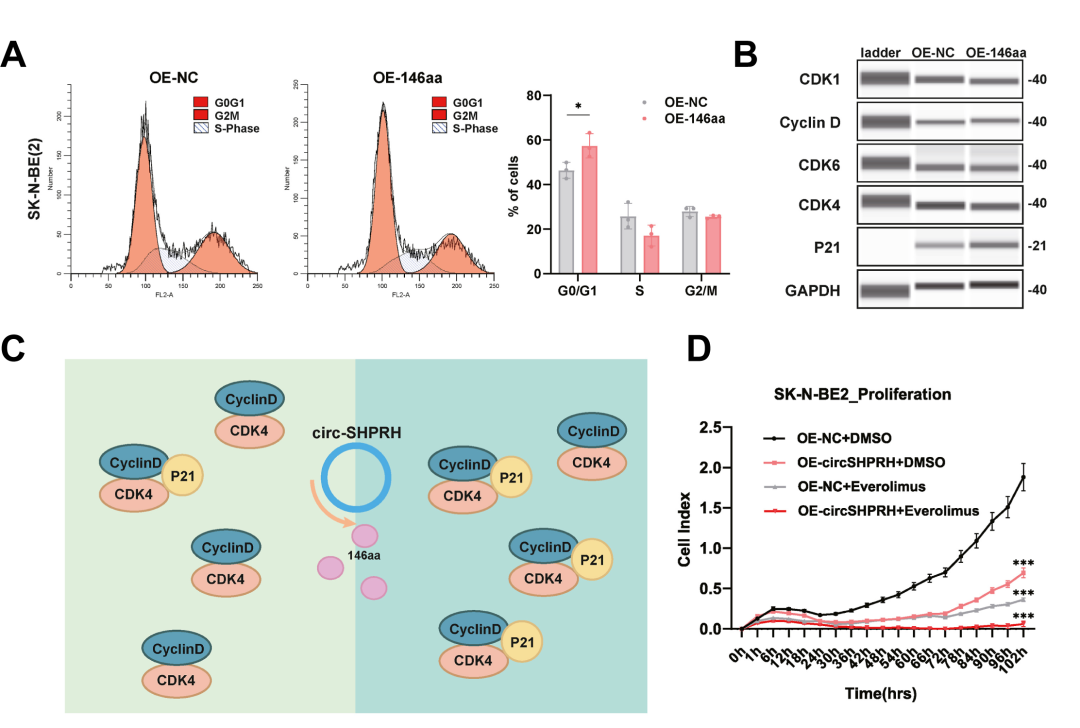
图3 circ-SHPRH的作用机制及联合应用。A-C)SHPRH-146aa阻滞细胞周期进程。D)circ-SHPRH与依维莫司联合应用可提高依维莫司疗效。
综上所述,此项研究发现了一种新的有潜力应用于NB基因治疗的分子circ-SHPRH,其有望对NB的治疗带来新策略、延长NB患儿生存时间、提高患儿生存质量。

