2024 ESMO LBA | 妇科肿瘤研究精粹
时间:2024-10-23 14:00:34 热度:37.1℃ 作者:网络
前言
2024年欧洲肿瘤内科学会(ESMO)年会已于当地时间9月13日至17日在西班牙 巴塞罗那以线上+线下形式召开。会议旨在为来自世界各地的肿瘤领域专家学者提供一个学习平台,传递有望改变临床实践现状的科研数据,进一步丰富患者的治疗选择。
LBA(Late-breaking abstract,最新突破性摘要)研究作为所有研究的重中之重,可能对临床实践产生重大影响。e路新干线小编特选取本次会议中5篇妇科肿瘤药物治疗相关LBA重点研究进行整理,涉及子宫内膜癌和卵巢癌两大领域,供各位医学同道参考。
01 子宫内膜癌
LBA28
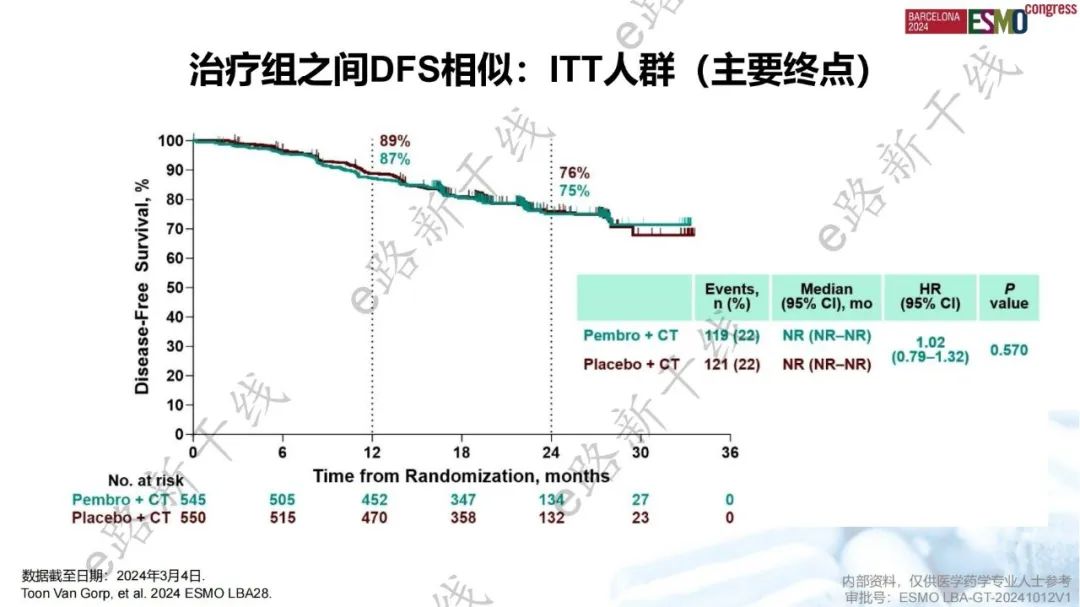
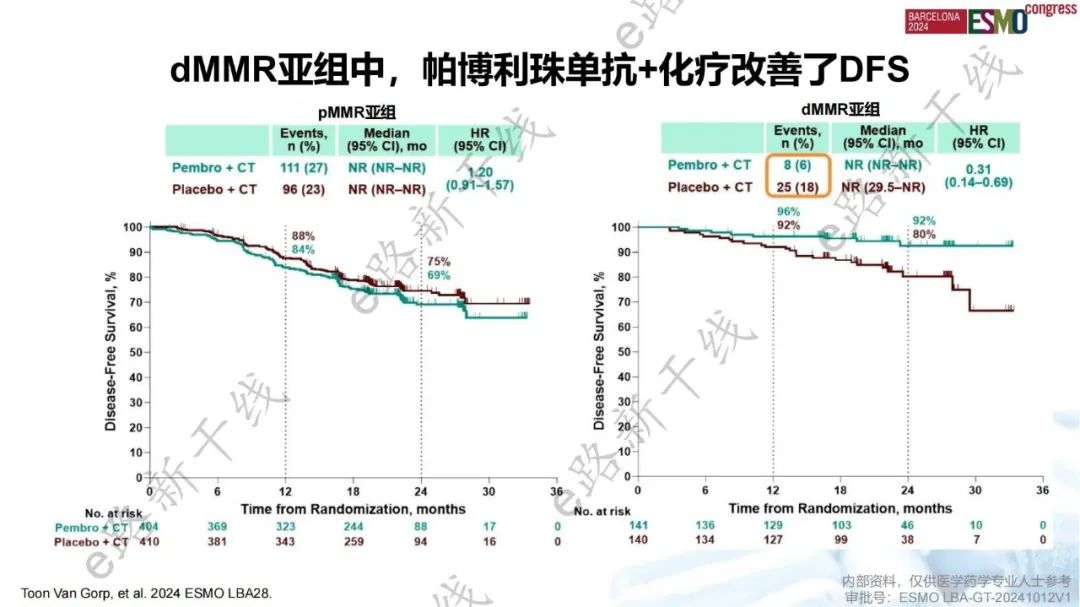
KEYNOTE-B21研究第三次期中分析结果:在辅助化疗中加入帕博利珠单抗未改善新诊断高危子宫内膜癌患者ITT人群的DFS,dMMR亚组的DFS HR倾向于帕博利珠单抗+化疗组
KEYNOTE-B21研究是一项评估帕博利珠单抗+化疗±放疗 vs. 安慰剂+化疗±放疗辅助治疗术后高危子宫内膜癌患者疗效的Ⅲ期研究。结果显示,在新诊断高危子宫内膜癌患者中,中位随访23.9个月,与安慰剂+化疗相比,帕博利珠单抗+化疗未改善DFS(主要终点,中位数:NR vs. NR,HR 1.02,P=0.570)。预先指定的亚组分析中,dMMR亚组患者的DFS HR倾向于帕博利珠单抗+化疗组(中位数:NR vs. NR,HR 0.31)。
02 卵巢癌
新诊断卵巢癌
LBA29
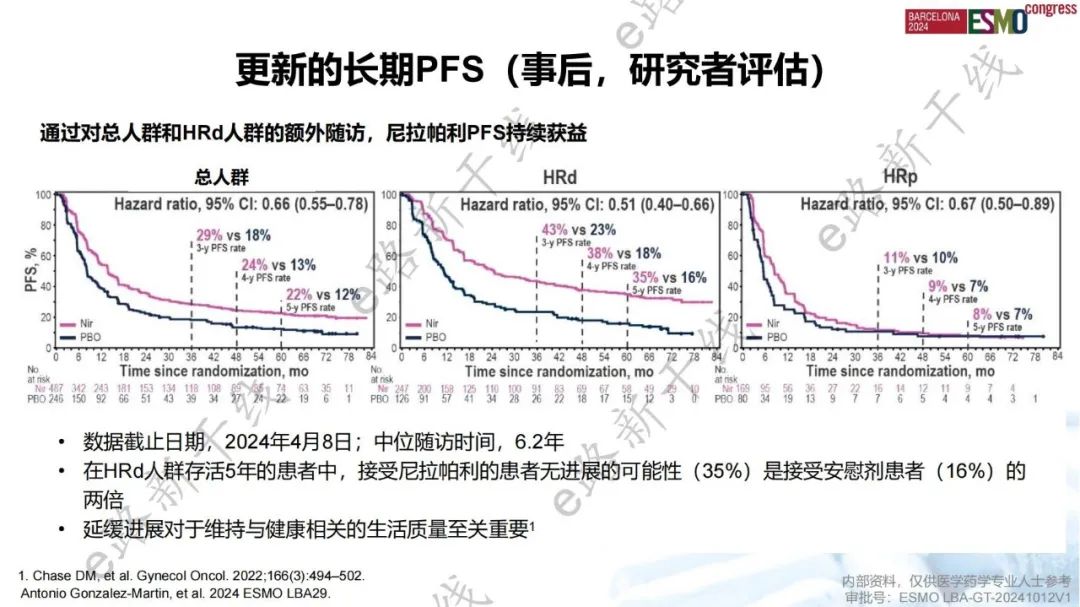
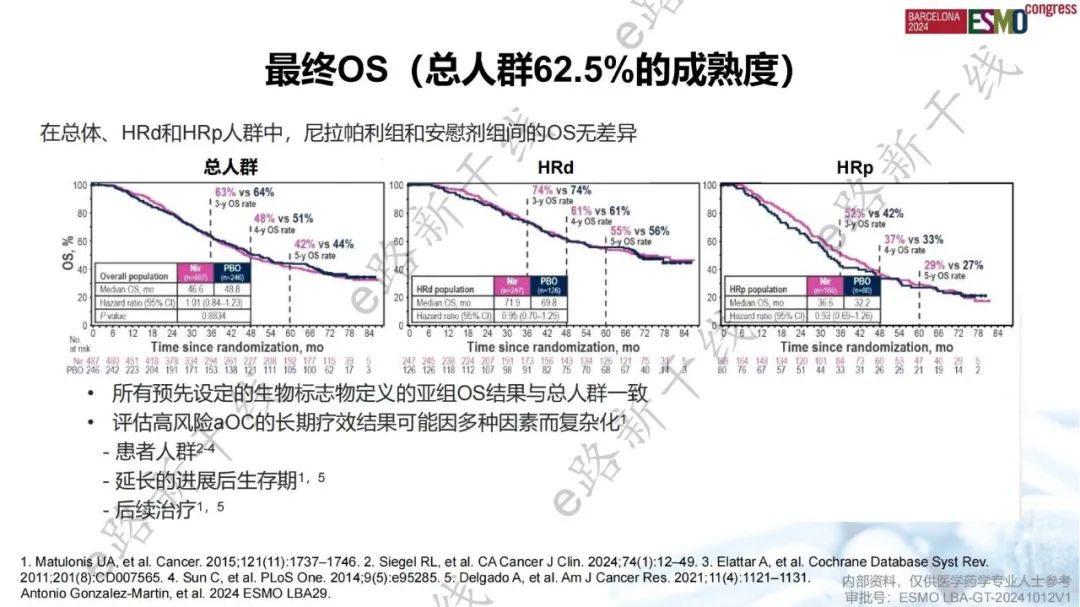
PRIMA研究最终OS结果:相比于安慰剂,尼拉帕利一线维持治疗新诊断晚期卵巢癌患者显著延长了总人群和HRd人群的PFS;总人群、HRd人群和HRp人群中,尼拉帕利组和安慰剂组间的OS无差异
PRIMA研究是一项旨在评估新诊断晚期卵巢癌患者接受含铂化疗达到完全缓解或部分缓解后,接受尼拉帕利一线维持治疗疗效的Ⅲ期研究。结果显示,中位随访6.2年,总人群及同源重组缺陷(HRd)人群中,尼拉帕利组PFS(主要终点)获益与首次报道的3.5年随访结果保持一致,与安慰剂相比,尼拉帕利改善了总人群的PFS(HR 0.66),也改善了HRd人群的PFS(HR 0.51);尼拉帕利一线维持治疗新诊断晚期卵巢癌患者的mOS为46.6个月,5年生存率为42%,但与安慰剂相比,尼拉帕利未显著改善总人群的OS(中位数:46.6 vs. 48.8个月,HR 1.01,P=0.8834);HRd人群中,两组OS也无差异(中位数:71.9 vs. 69.8个月,HR 0.95)。
LBA30
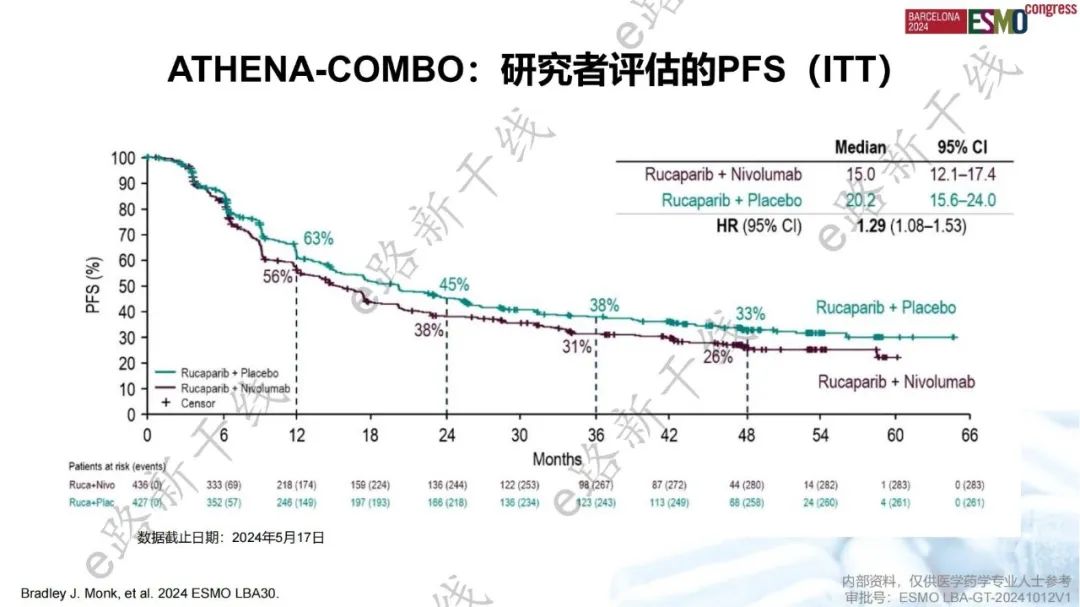
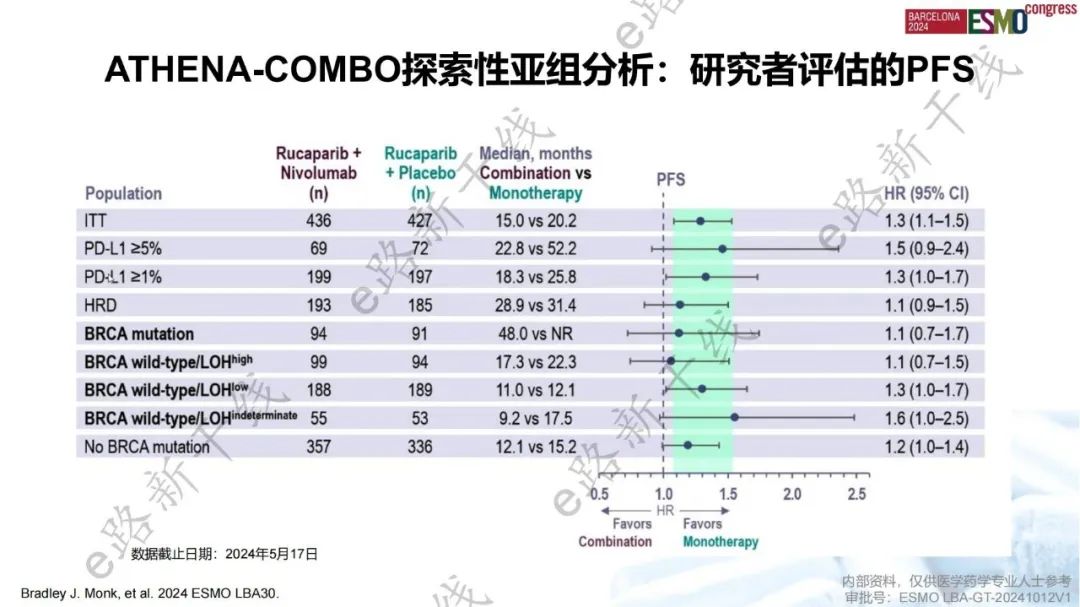
ATHENA-COMBO研究:相比于卢卡帕利单药,卢卡帕利+纳武利尤单抗一线维持治疗新诊断晚期卵巢癌患者并未延长PFS
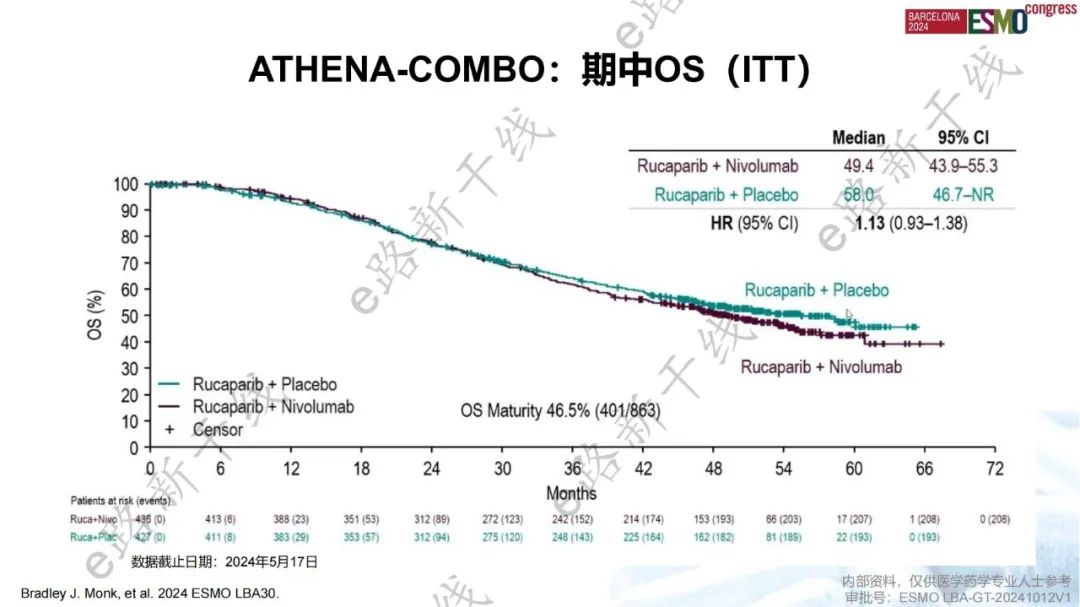
ATHENA-COMBO研究是一项旨在评估卢卡帕利+纳武利尤单抗 vs. 卢卡帕利单药维持治疗对一线铂类化疗有缓解的新诊断晚期卵巢癌患者疗效的Ⅲ期研究。结果显示,与卢卡帕利单药相比,卢卡帕利+纳武利尤单抗联合疗法未改善ITT人群的PFS(主要终点,研究者评估的mPFS:15.0 vs. 20.2个月,HR 1.29),联合用药的疾病进展或死亡风险增加了29%。联合用药组和单药组的12个月PFS率分别为56%和63%,48个月PFS率分别为26%和33%。这种PFS趋势在各个亚组中一致,包括HRD亚组(mPFS:28.9 vs. 31.4个月)和PD-L1≥1%(mPFS:18.3 vs. 25.8个月)和PD-L1≥5%亚组(mPFS:22.8 vs. 52.2个月)。OS数据尚不成熟,但两组之间无差异(mOS:49.4 vs. 58.0个月,HR 1.13)。
铂敏感复发卵巢癌
LBA33
ICON9研究:相比于奥拉帕利,奥拉帕利+西地尼布维持治疗对铂基化疗有缓解的铂敏感复发卵巢癌患者的PFS或OS改善均无统计学意义
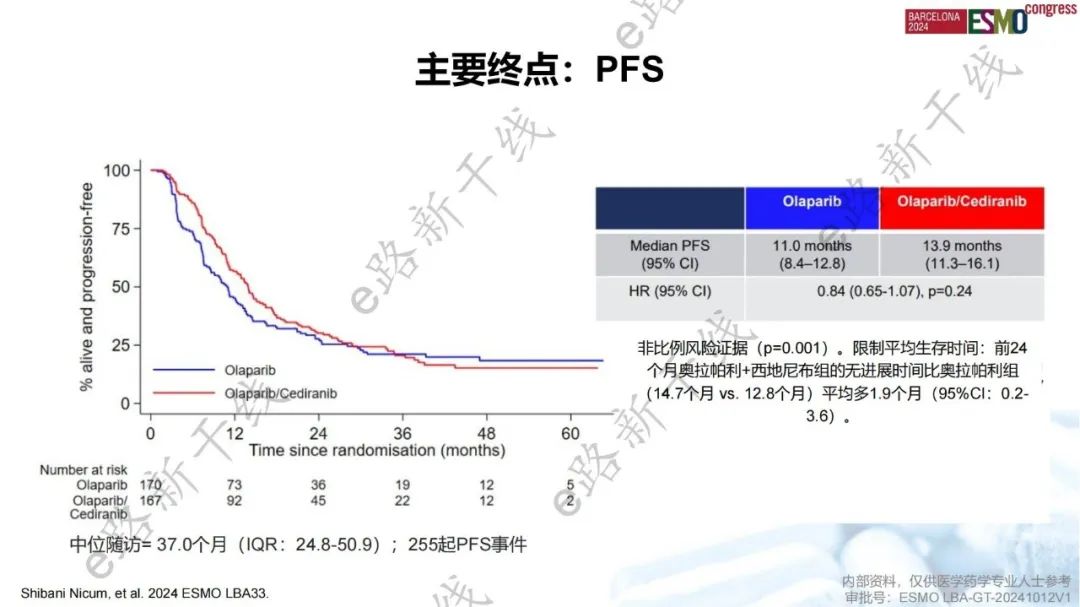
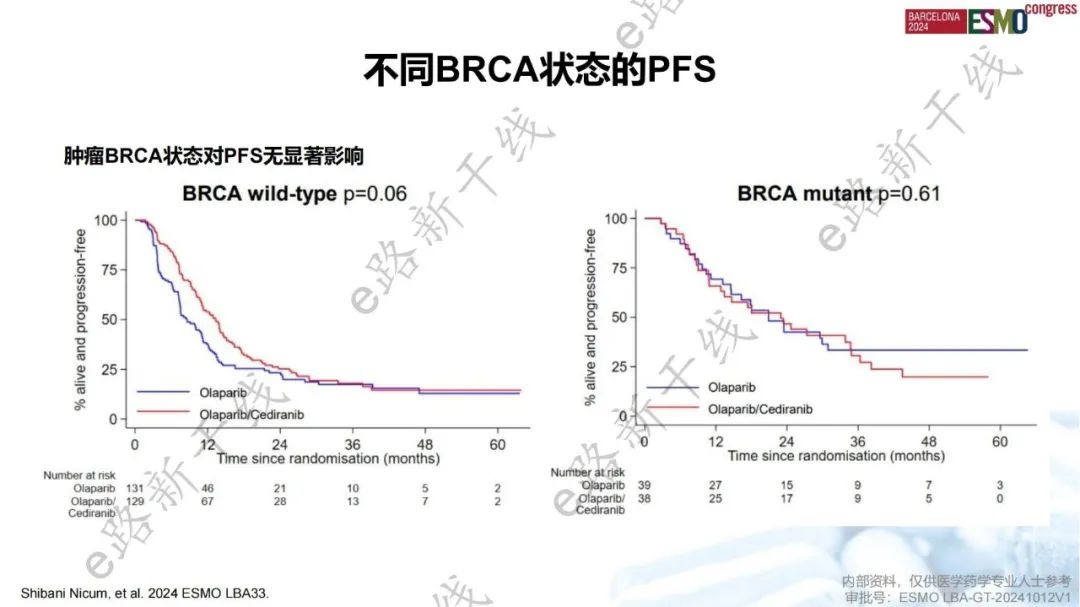
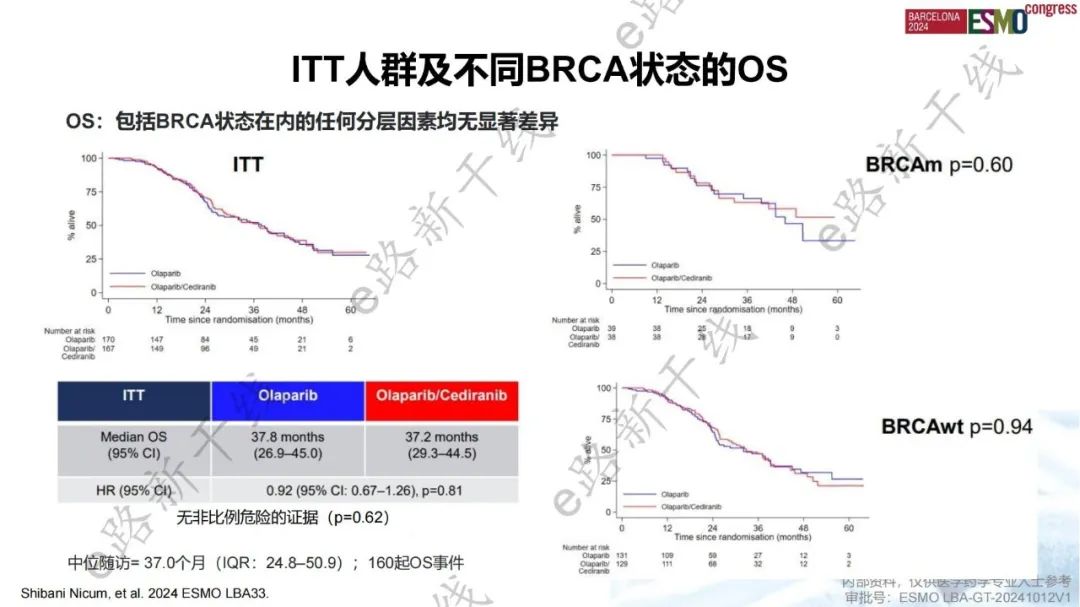
ICON9研究是一项旨在评估奥拉帕利+西地尼布 vs. 奥拉帕利维持治疗对铂基化疗有缓解的铂敏感复发卵巢癌患者疗效的Ⅲ期研究。结果显示,中位随访37.0个月,相比于奥拉帕利组,奥拉帕利+西地尼布组的PFS未显著改善(主要终点,中位数:13.9 vs. 11.0个月,HR 0.84,P=0.24)。基于肿瘤BRCA状态分析PFS,未能证明联合治疗有PFS获益,在BRCA突变和BRCA野生型患者中P值分别为0.61和0.06。相比于奥拉帕利组,奥拉帕利+西地尼布组的OS未显著改善(中位数:37.2 vs. 37.8个月,HR 0.92,P=0.81)。根据任何分层因素(包括BRCA状态)分析OS,均显示联合方案和单药方案的OS无显著差异,BRCA突变和BRCA野生型患者中P值分别为0.60和0.94。
铂耐药卵巢癌
LBA32
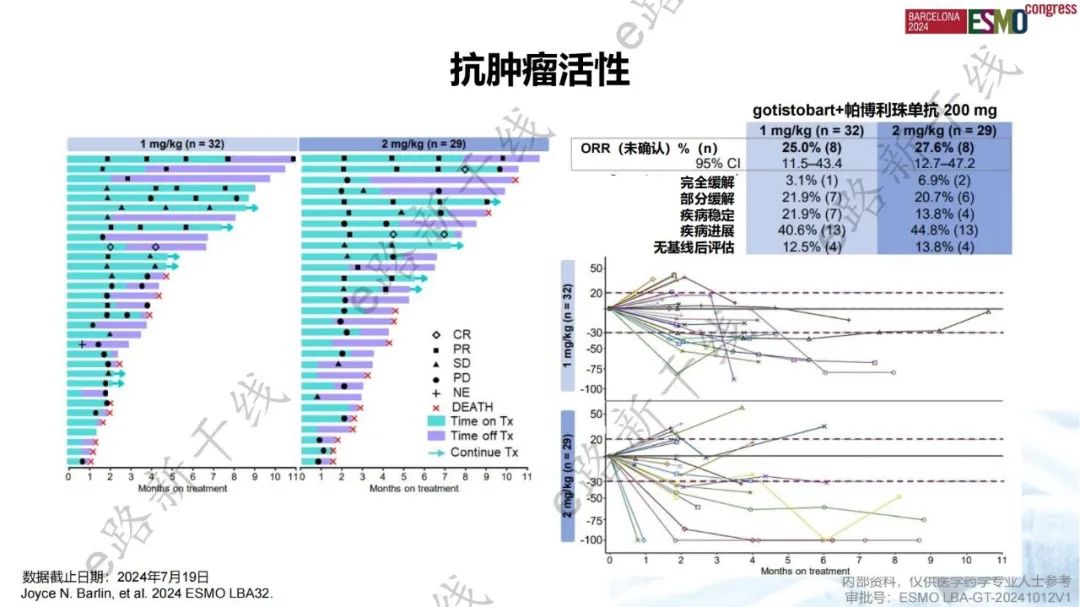
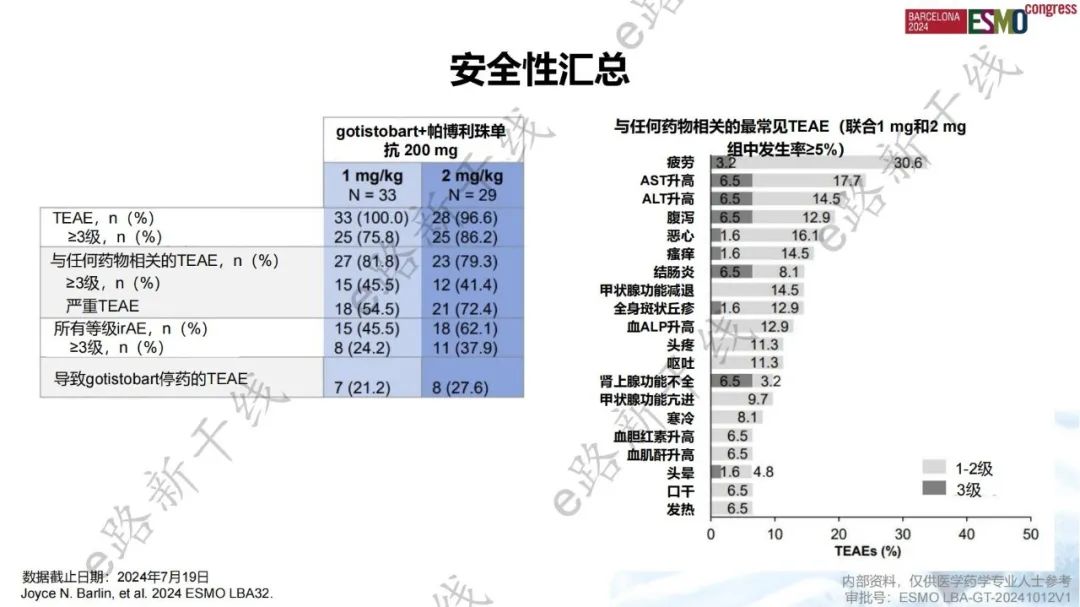
PRESERVE-004研究:gotistobart+帕博利珠单抗治疗铂耐药卵巢癌患者初步疗效结果令人鼓舞,gotistobart两种剂量水平下,安全性均可控,无新的安全性事件发生
PRESERVE-004研究是一项旨在评估gotistobart(pH敏感的抗CTLA-4抗体)+帕博利珠单抗治疗铂耐药卵巢癌患者有效性和安全性的Ⅱ期研究。结果显示,gotistobart(1 mg/kg)+帕博利珠单抗(200 mg)治疗铂耐药卵巢癌患者未确认的ORR为25.0%,gotistobart(2 mg/kg)+帕博利珠单抗(200 mg)治疗铂耐药卵巢癌患者未确认的ORR为27.6%。两种剂量水平下,gotistobart+帕博利珠单抗的耐受性良好,安全性可控。