Nat Neurosci:甘莉团队揭示Tau蛋白激活小胶质细胞炎症反应引起认知功能障碍
时间:2023-05-01 11:24:32 热度:37.1℃ 作者:网络
环GMP-AMP合成酶(cGAS)是一种重要的DNA病毒传感器,可通过触发I型干扰素(IFN)信号激活干扰素基因刺激因子(STING),催化环GMP-AMP (cGAMP)形成,从而启动病毒免疫反应。抗病毒反应通路在阿尔茨海默病(AD)中上调,并调节小胶质细胞疾病相关反应。
在帕金森病、肌萎缩性侧索硬化症和亨廷顿病等多种神经系统疾病中cGAS-STING通路驱动炎症性IFN信号的激活,在AD小鼠模型促进Aβ淀粉样蛋白的沉积。
2023年4月24日威尔康奈尔医学院费尔家族大脑研究所甘莉团队揭示了tau蛋白病变激活小胶质细胞IFN信号,降低神经元Mef2c表达,引起认知功能障碍。
1
Tau蛋白驱动小胶质细胞IFN相关的炎症反应
P301S小鼠是一种表达人微管相关蛋白tau的P301S突变体,表现出与人类类似的AD病理学特征。研究人员通过单细胞测序发现8月龄P301S小鼠海马组织IFN信号通路相关基因和cGAS-STING通路核心成分cGAS、STING 和 TBK1基因表达显着上调。分子实验也进一步证实P301S小鼠海马组织TBK1蛋白磷酸化水平升高,在AD患者海马组织也检测到这种变化。免疫荧光实验发现该模型小鼠小胶质细胞STING 表达显着增加。
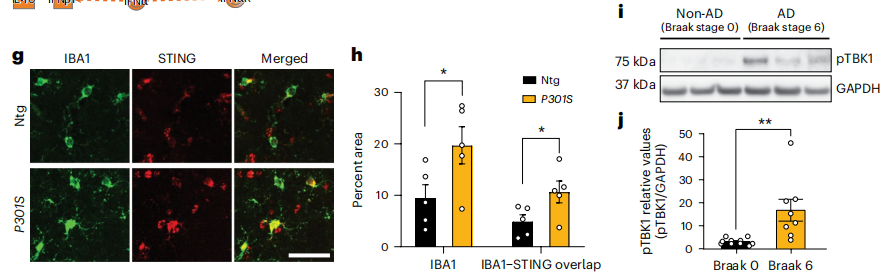
图1:P301S小鼠小胶质细胞上表达STING蛋白增加
2
Tau蛋白激活小胶质细胞IFN通路依赖于cGAS
离体细胞实验发现tau蛋白纤维可促进小胶质细胞IFNβ, CXCL10和CCL5蛋白的表达,也促进TBK1蛋白磷酸化水平升高,在敲除Cgas 后可阻断tau蛋白纤维诱发的炎症因子水平升高。tau蛋白纤维可促进线粒体DNA (mtDNA)释放到小胶质细胞细胞质中,电子显微镜发现位于tau蛋白溶酶体和线粒体中,在清除mtDNA可减弱tau蛋白激活小胶质细胞IFN信号通路。
在敲除P301S小鼠Cgas 后海马组织IFN信号通路激活减弱,小胶质细胞TBK1蛋白磷酸化水平降低。电生理实验表明敲除Cgas 后,P301S小鼠海马长时程可塑性障碍得到改善,免疫荧光实验发现海马脑区突触密度增加,行为学实验表明P301S小鼠的空间记忆能力得到改善,这些结果表明AD模型小鼠海马小胶质细胞IFN信号通路激活依赖于cGAS。
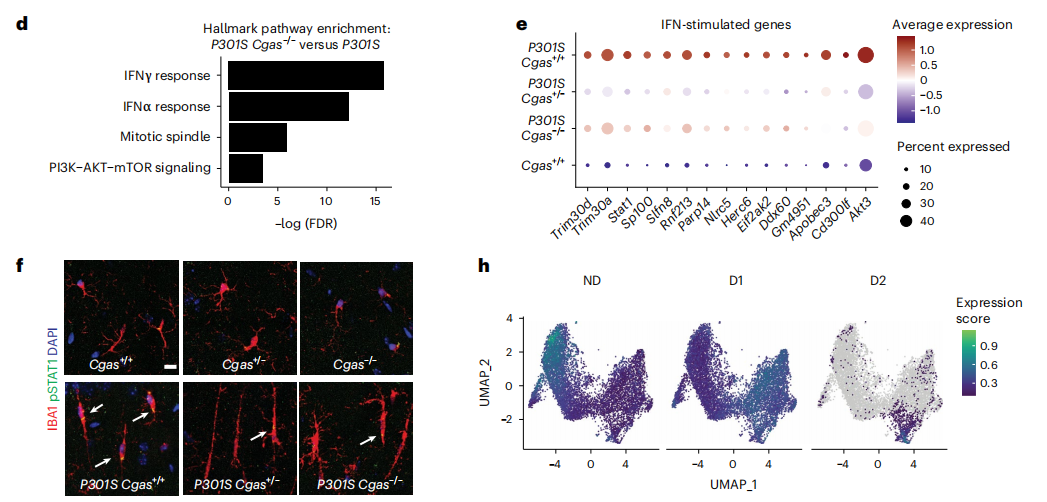
图2.AD模型小鼠小胶质细胞IFN信号通路依赖于cGAS
3
Tau蛋白减弱神经元Mef2c转录网络的神经保护作用
进一步对敲除P301S小鼠Cgas 后海马组织进行单细胞测序,发现兴奋性神经元和抑制性神经元差异性表达基因均上调的是肌细胞增强因子2c(Mef2c),神经元来源Mef2c表达的水平与小胶质细胞IFN信号反应成负相关关系。
敲除Cgas 后可逆转P301S小鼠海马组织中Mef2c靶向轴突导向、生长和突触的维持等信号相关基因的表达。P301S小鼠在接受cGAS 特异性抑制剂处理后可同样促进海马组织突触密度的增加,改善海马突触可塑性,改善空间记忆障碍,并能够促进Mef2c转录靶向基因的表达。这就表明敲除Cgas 通过靶向Mef2c转录网络发挥神经保护作用。
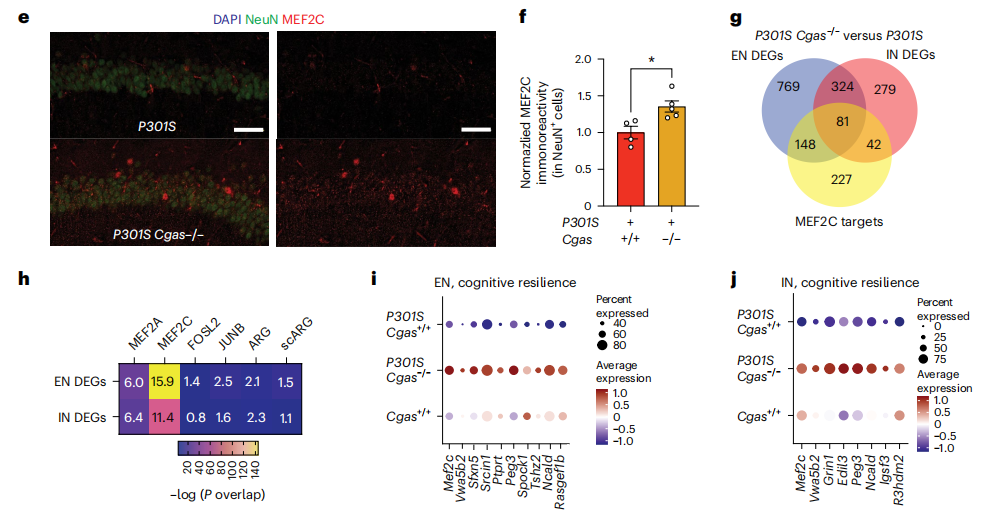
图3:Tau蛋白减弱神经元Mef2c转录网络神经保护作用
总结
本文揭示了在AD发病进程中cGAS-STING通路驱动小胶质细胞炎症性IFN信号的激活,降低神经元Mef2c转录靶向基因的表达,引起突触功能障碍和空间学习障碍。
原始出处:
Udeochu, J.C., Amin, S., Huang, Y. et al. Tau activation of microglial cGAS–IFN reduces MEF2C-mediated cognitive resilience. Nat Neurosci (2023). https://doi.org/10.1038/s41593-023-01315-6.


