J Clin Oncol: Amivantamab治疗铂类进展的EGFR 20外显子插入突变非小细胞肺癌的安全性和疗效:I期研究CHRYSALIS的初次分析结果
时间:2021-08-03 22:02:39 热度:37.1℃ 作者:网络
非小细胞肺癌(NSCLC)中EGFR突变是常见的驱动基因,其中85%突变为19外显子的缺失或21外显子21 L858R点突变。第三常见的为20外显子的插入突变(Exon20ins),约占≤12%。但是,Exon20ins NSCLC患者对于目前常见的TKI反应率很低,约0%-9%。因此,目前的标准治疗仍是以铂类为基础的化疗,中位OS只有16个月,而EGFR-TKI敏感突变患者的中位OS达到39个月。Amivantamab (JNJ-61186372)是EGFR-MET双特异性抗体,可直接激活免疫细胞。国外研究团队开展了一项I期研究CHRYSALIS,评估Amivantamab治疗铂类进展的EGFR 20外显子插入突变非小细胞肺癌的安全性和疗效。相关结果发表在Journal of Clinical Oncology杂志上。

2016年5月27日至2020年6月8日,纳入362例患者。其中77例进行安全性和药代动力学研究。经过剂量爬坡研究,258例患者进入推荐剂量研究,amivantamab用药方式: 1,050 mg (1,400 mg ≥80 kg时) 前四周每周一次,第5周开始2周一次。安全数据截止2020年6月8日时,中位随访时间为5.1个月 (range, 0.2-29.3个月)。
疗效人群中(n=81例),中位年龄为62岁(range, 42-84岁),48例(59%) 为女性, 40 例(49%)为亚洲人群, 所有患者接受过铂类为基础化疗。既往中位接受治疗线数为2(range, 1-7),20 例(25%) 接受过EGFR TKIs, 37例(46%) 接受过免疫治疗。疗效数据截止时间2020年10月8日时,中位随访时间为9.7个月(range,1.1-29.3个月)。
安全性人群(n=114)评估中,不良事件(AEs)跟EGFR抑制有关的有皮疹发生在98例患者(86%),甲沟炎51 例(45%), 口腔炎24例 (21%), 瘙痒19例 (17%), 和腹泻14例(12%)。和MET 抑制有关的有低蛋白血症31例 (27%) 和外周四肢水肿21例 (18%)。间质性肺病(包括肺炎)在5例患者中报道(4%)。
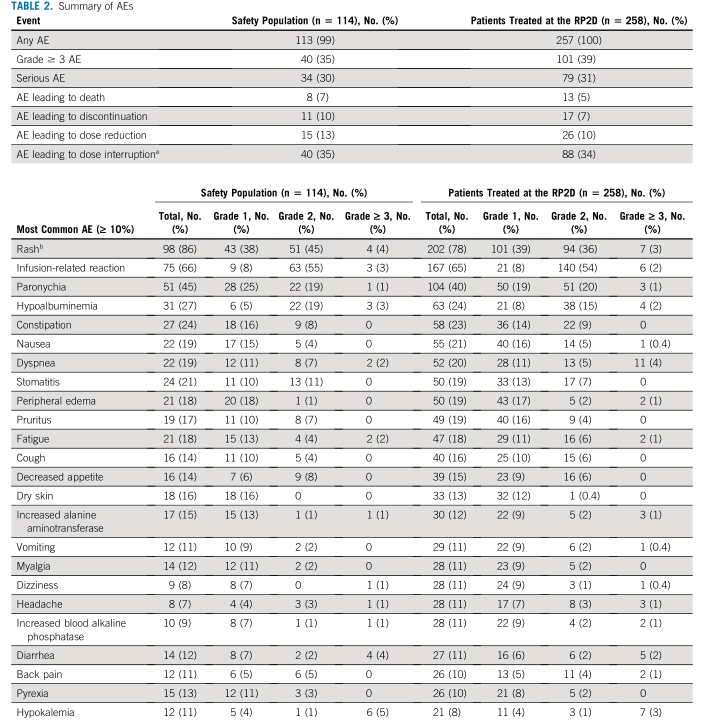
不良事件
常见的3-4级不良事件为低血钾(5%),皮疹(4%),肺栓塞(4%),腹泻(4%),和中性粒细胞减少(4%)。治疗相关剂量减少和中止治疗的比例分别为13% 和4%。

疗效评估
客观缓解率(ORR)为40%(95% CI, 29 to 51),其中3例完全缓解(CR)和29例部分缓解(PR)。15例仍在应答患者的中位持续缓解时间(DOR)为 11.1个月 (95% CI, 6.9-未达到), 75%患者出现应答在第一次疗效评估时。中位PFS 为8.3个月 (95% CI, 6.5-10.9),而中位OS为22.8个月 (95% CI, 14.6-未达到)。
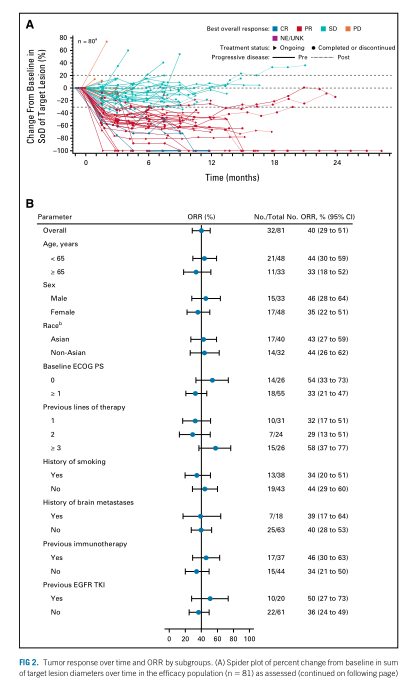
ORR
综上, Amivantamab治疗铂类进展的EGFR 20外显子插入突变非小细胞肺癌(NSCLC)患者呈现出良好的抗肿瘤活性以及安全性。
原始出处:
Park K, Haura EB, Leighl NB, et al. Amivantamab in EGFR Exon 20 Insertion-Mutated Non-Small-Cell Lung Cancer Progressing on Platinum Chemotherapy: Initial Results From the CHRYSALIS Phase I Study. J Clin Oncol. 2021 Aug 2:JCO2100662. doi: 10.1200/JCO.21.00662. Epub ahead of print. PMID: 34339292.


