【JAMA Oncol】肾脏AL型淀粉样变性治疗后的24小时尿蛋白可预测生存期和进展风险
时间:2024-09-18 14:03:02 热度:37.1℃ 作者:网络
AL型淀粉样变性
轻链(AL)型淀粉样变性可累及多个器官,其中肾脏受累的发生率为50%-70%,肾脏受累的主要临床表现为蛋白尿(通常在肾病范围内)和肾衰竭,30%-40%的患者在整个病程中可发展为终末期肾病。肾脏AL型淀粉样变性存在进展为肾脏替代治疗 (KRT) 和死亡的风险。
十年前发表的肾脏反应标准根据24小时尿蛋白水平将治疗后反应分为肾脏完全缓解、非常好的部分缓解、部分缓解和无缓解,抗克隆治疗后蛋白尿的减少幅度与结局改善相关。为了验证分级肾脏反应标准与KRT和总生存期 (OS) 的相关性,学者开展了一项回顾性、多中心队列研究,近日发表于《JAMA Oncology》,通讯作者为梅奥诊所Eli Muchtar教授。

研究方法
该研究纳入可以评价肾脏反应(24小时蛋白尿>0.5g)的肾脏AL型淀粉样变性患者,并且在诊断后12个月内至少实现血液学部分缓解。在关键时间点(6、12和24个月)评估肾脏反应和最佳肾脏反应。主要终点为进展到KRT的累积发生率和OS。
基于治疗前24小时尿蛋白水平的降低情况,分为4个肾脏反应类别:肾脏完全缓解(kidCR,24小时尿蛋白≤200mg)、非常好的部分缓解(kidVGPR,24小时尿蛋白降低>60%)、部分缓解(kidPR,降低31%-60%)和无缓解(kidNR,降低≤30%)。
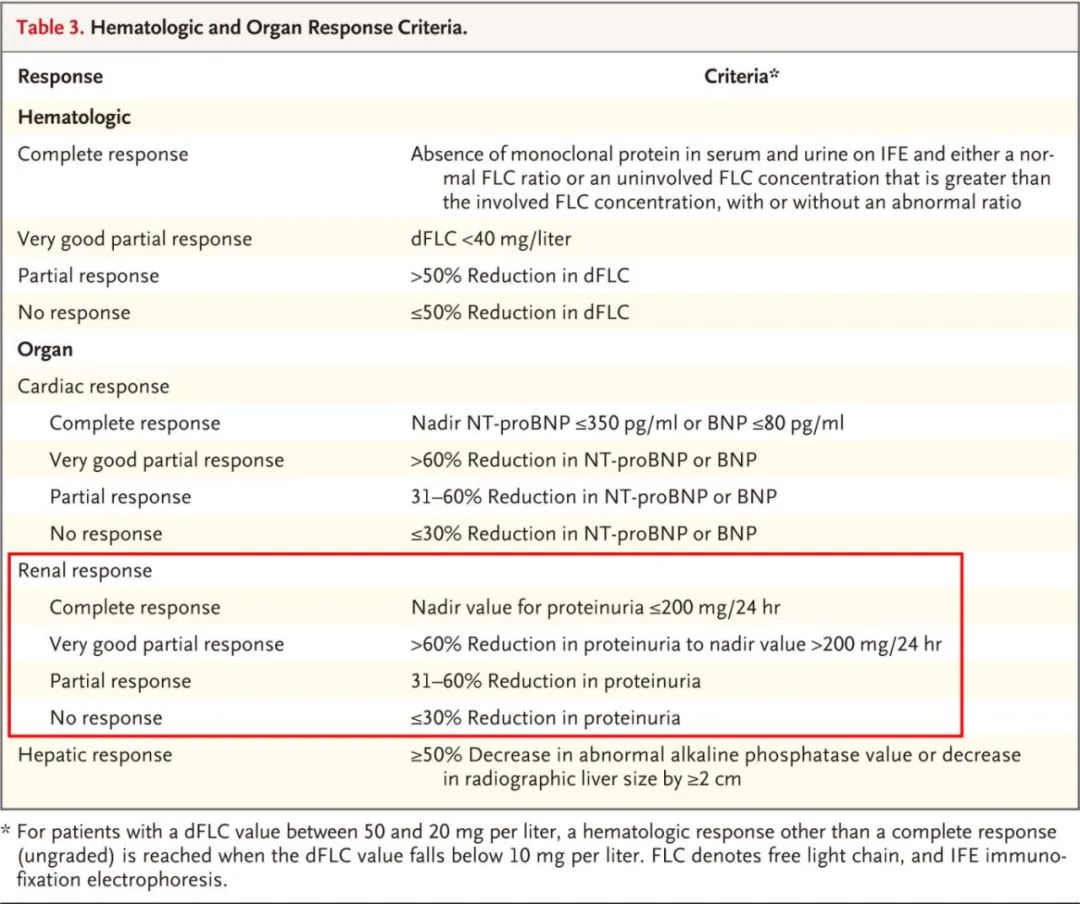
研究结果
研究纳入732例患者(335例女性 [45.8%]),中位年龄为63岁。中位随访时间为69个月。中位基线24小时蛋白尿和估计的肾小球滤过率分别为5.3g/24小时和72mL/min/1.73 m2。24小时蛋白尿随时间而降低,6个月、12个月和24个月分别降低34%、50%和71%,相应的缓解深度也逐渐加深,最佳缓解情况下kidCR、kidVGPR、kidPR和kidNR分别为26.1%、31.7%、14.5%和27.7%。至最佳肾脏缓解的中位时间为16.0个月,kidCR(22.1个月)长于kidVGPR(16.2个月)或kidPR(10.3个月)。
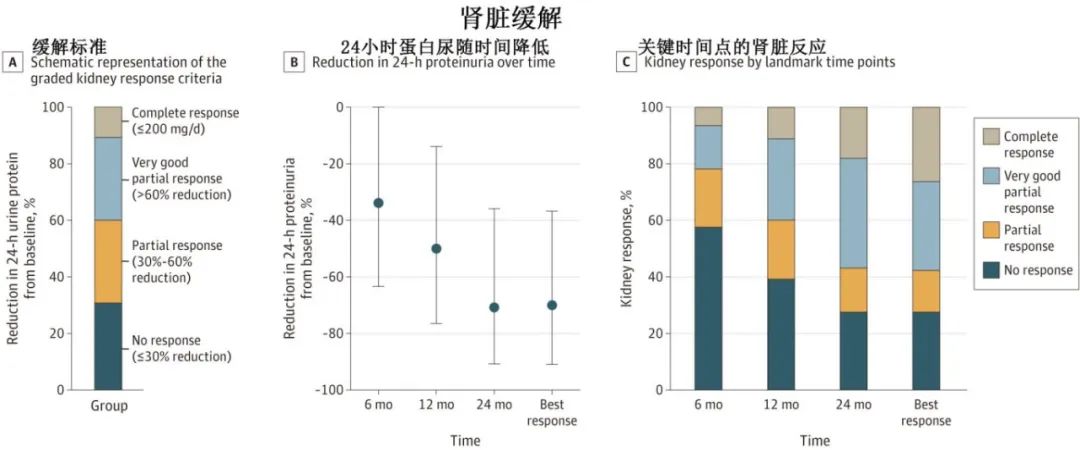
在竞争风险分析中,进展为 KRT 的5年累积发生率随着肾脏反应的加深而降低,例如治疗开始后6个月的关键时间点(kidNR、kidPR、kidVGPR和 kidCR 患者分别为11%、12%、2.1%和0%;P=0.002),且在12个月和24个月的关键时间点以及最佳肾脏反应时维持该趋势。6个月和12个月时kidCR患者均未进展为KRT。
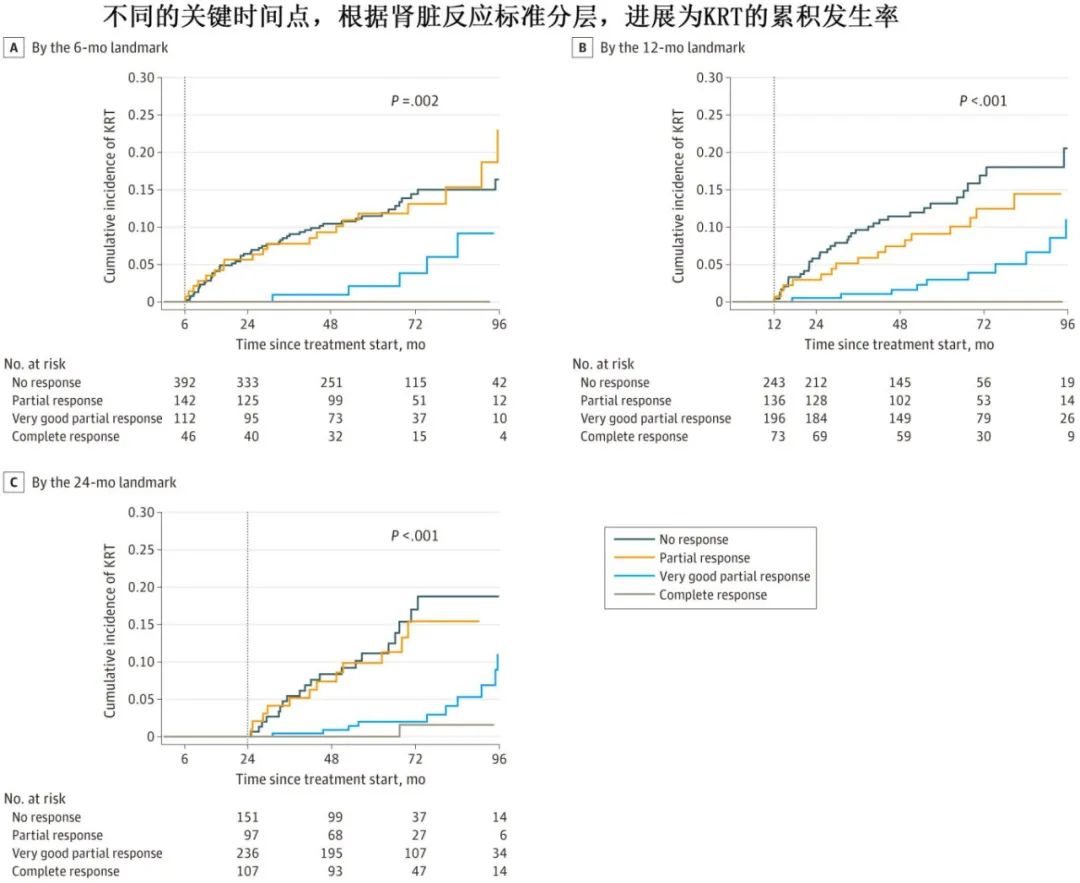
与 kidPR/kidNR 相比,24个月关键时间点时达到 kidCR/kidVGPR的患者的 OS 显著更好(kidNR、kidPR、kidVGPR和 kidCR 患者的5年OS分别为75.2%、79.7%、91.4%、91.6% ;P<0.001),且进展为 KRT 的的风险更低(5年KRT率分别为11%、9.9%、2.0%和0%;P<0.001)。根据6个月时缓解情况分层的OS无差异,从12个月关键时间点开始kidNR与其他患者有差异(kidNR、kidPR、kidVGPR和 kidCR 患者的5年OS分别为72.3%、84.7%、86.2%、85.6% ;P<0.001)。此外,根据最佳缓解时的反应,OS(kidNR、kidPR、kidVGPR和 kidCR 患者的5年OS分别为54%、66%、85%、90% ;P<0.001)和KRT(5年KRT分别为33%、18%、3.1%、0%;P<0.001)风险也有显著差异。
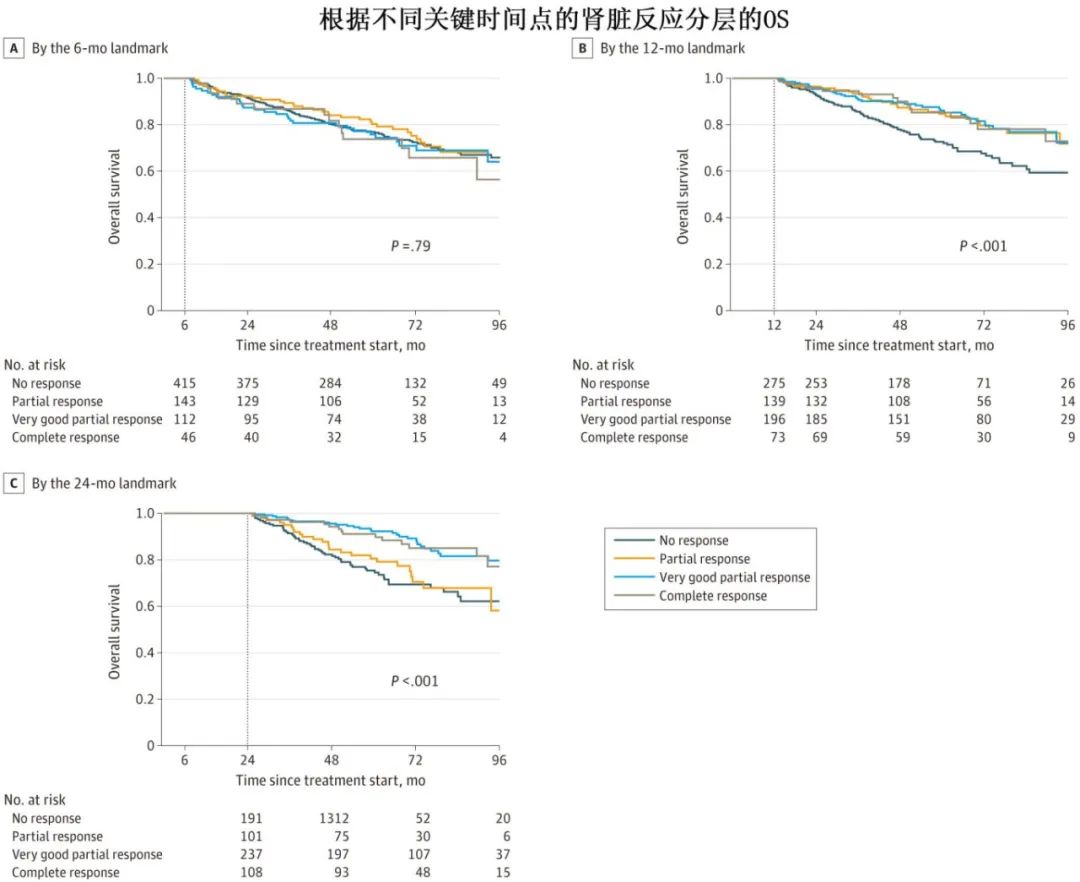
肾脏进展定义为估计的肾小球滤过率降低≥25%,与进展至 KRT 和 OS 的累积发生率相关:肾脏进展相对于肾脏未进展,5年KRT分别为42% vs 7.6%(P<0.001),5年OS分别为65% vs 80%(P<0.001)。
总结
该队列研究的结果表明,分级的肾脏反应标准可为治疗肾脏 AL 型淀粉样变性患者提供具有临床意义和预后意义的信息,24小时蛋白尿水平降低的深度可告知KRT风险和生存期,更好地评估治疗有效性,并证明与 kidPR/kidNR 相比,能够达到 kidCR/kidVGPR 的患者具有 OS 优势。在固定点应用这些标准可提供基于肾脏反应时间的目标,以最大化结局。
肾脏 AL 型淀粉样变性的治疗目标应该是治疗开始后6个月实现kidPR,12个月和24个月实现kidVGPR,以最终改善肾脏和患者生存率;未能达到这些终点应提示考虑替代治疗。随着 AL 型淀粉样变性管理的改善,还可能会出现实现这些器官缓解目标的早期标志物。
参考文献
Muchtar E, et al. Graded Organ Response and Progression Criteria for Kidney Immunoglobulin Light Chain Amyloidosis.JAMA Oncol . 2024 Aug 1:e242629. doi: 10.1001/jamaoncol.2024.2629.


