ACS Nano | 南方医科大学涂盈锋/中山大学彭飞开发了一种基于微电机的胰岛素口服微型片剂,实现长效血糖控制
时间:2022-12-27 15:00:24 热度:37.1℃ 作者:网络
糖尿病是一种代谢疾病,其特征是由于胰岛素分泌缺陷或其生物学功能障碍引起的高血糖。然而,频繁皮下注射胰岛素往往会引起不适和局部组织感染。
2022年12月22日,南方医科大学涂盈锋及中山大学彭飞共同通讯在ACS Nano(IF=18)在线发表题为“Micromotor Based Mini-Tablet for Oral Delivery of Insulin”的研究论文,该研究开发了一种基于微电机的胰岛素口服微型片剂。
该研究展示了一种基于自驱动微电机的微型片剂系统的成功制造,该系统具有生物相容性和生物可降解性,用于口服结肠给药胰岛素。胰岛素层首先通过静电相互作用构建到镁基微电机表面,然后进行片剂处理。然后,所得到的微型片剂涂上具有结肠降解能力的酯化淀粉,从而实现结肠区域内嵌入的微电机的可控释放。同时,释放的微电机自主运动,速度可达76.22 μm·s−1,进一步增强了胰岛素的结肠吸收和吸收,实现了5小时以上的长期血糖控制。基于微电机的微型片剂系统不仅拓宽了新兴自驱动微电机的生物医学应用领域,也为口服胰岛素为代表的生物大分子药物提供了一种有价值的策略。
糖尿病是一种代谢性疾病,由于胰岛素分泌不足或对胰岛素的敏感性降低而导致血浆葡萄糖水平升高。临床上通常需要定期皮下注射胰岛素来控制糖尿病患者的血糖,尤其是饭前注射胰岛素。然而,高强度胰岛素注射带来依从性不足、组织感染和低血糖风险增加,可能导致脑损伤、癫痫发作、意识丧失,甚至死亡。因此,迫切需要一种方便有效的胰岛素给药方法。
口服生物大分子药物作为一种理想的策略,为需要定期针注射的患者提供了最佳的选择。然而,胃酸、胃蛋白酶、胰蛋白酶等恶劣的消化环境导致生物大分子结构迅速降解,导致生物大分子失活。同时,由致密上皮细胞和黏液层组成的肠屏障,进一步阻止了生物大分子的吸收。结肠作为消化系统的一部分,其滞留时间较长,黏膜层较薄,上皮细胞排列较松,消化条件较温和,能够同时促进生物大分子药物的吸收和活性滞留。在结肠淋巴组织中直接吸收生物大分子也可以避免肝磷脂的首过效应,从而进一步提高其生物利用度。因此,结肠给药在以胰岛素为代表的生物大分子药物的高效口服给药方面具有广阔的应用前景。
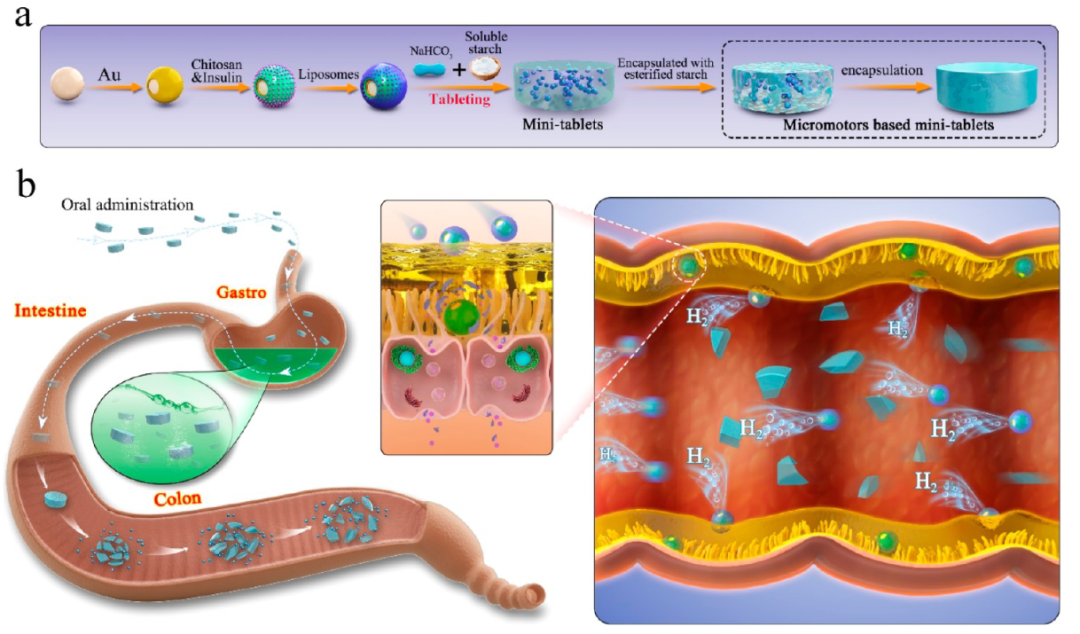
胰岛素口服微电机微型片剂系统示意图(S@dMTs)(图源自ACS Nano )
为了提高口服胰岛素对恶劣消化环境的耐受性,在过去几十年中,基于多糖微粒和纳米颗粒或纳米乳液胶束的各种策略被用于口服-结肠递送胰岛素。然而,传统的微纳米载体被动扩散导致胰岛素传递效率有限。微/纳米电机作为自其驱动电机,能够将化学或物理能量转化为机械运动,由于其在生物医学领域的应用前景广阔,特别是药物输送,引起了广泛的研究兴趣。由于自主运动,微/纳米电机可以有效地增强药物的保留、穿透、细胞摄取和吸收。因此,它们的运动能够主动和精确地运送货物,以提高胃感染、口服疫苗、恶性胶质瘤、干细胞移植的疗效,使微/纳米电机成为下一代药物输送系统。近年来,镁基微电机由于在局部体液作用下不断产生氢泡并产生强大驱动力而得到广泛应用。此外,生成的Mg2+也是机体必需的重要微量元素之一。因此,镁微电机的易调性和可生物降解性使其在生物医学领域具有广阔的应用前景。
在本报告中,作者展示了一种胰岛素负载微型片剂系统的设计和制造,该系统可以克服恶劣的消化环境和粘膜吸收障碍,用于主动口服胰岛素输送。通过使用辅助崩解辅料和随后的酯化淀粉包封胰岛素负载Mg微电机,形成的微型片剂提供有效的保护负载胰岛素从直接接触复杂的消化液和结肠引发的分解。值得注意的是,Mg微电机的释放和结肠驱动进一步实现了负载胰岛素在结肠局部的可控释放和增强扩散,从而实现了糖尿病大鼠相对长期的血糖控制。减少给药间隔时间和改善系统的糖尿病依从性可能为口服胰岛素治疗糖尿病迈出了具体的一步。研究人员认为,所提出的策略具有良好的依从性,易于制造,提高疗效,显示出口服大多数生物大分子药物的巨大潜力。
原文链接:
https://pubs.acs.org/doi/10.1021/acsnano.2c07953


