Advanced Science | 山东大学初波等团队合作发现色氨酸代谢是促进肿瘤细胞生长的新型抗铁死亡途径
时间:2023-01-15 12:01:45 热度:37.1℃ 作者:网络
新证据表明,氨基酸代谢在细胞铁死亡中起着重要作用。半胱氨酸缺乏时,甲硫氨酸通过转氨作用转化为半胱氨酸的转化可保护肿瘤细胞免受铁死亡。然而,氨基酸产生的代谢物是否不依赖于半胱氨酸途径,独立参与铁死亡机制尚不清楚。
2023年1月10日,山东大学初波、东南大学/南通大学/电子科技大学柴人杰及深圳湾实验室尹成骞共同通讯在Advanced Science 在线发表题为“Tryptophan Metabolism Acts as a New Anti-Ferroptotic Pathway to Mediate Tumor Growth”的研究论文,该研究表明色氨酸代谢物血清素(5-HT)和3-羟基邻氨基苯甲酸(3-HA)明显帮助肿瘤细胞逃避铁死亡,与半胱氨酸介导的铁死亡抑制不同。从机制上讲,5-HT和3-HA均作为自由基捕获抗氧化剂(RTA)消除脂质过氧化,从而抑制细胞铁死亡。单胺氧化酶A(MAOA)通过降解5-HT显著消除5-HT的保护作用, MAOA的缺乏使癌细胞在5-HT治疗后对铁死亡产生抗性。
犬尿素酶(KYNU)对3-HA的产生至关重要,赋予细胞抵抗铁死亡的能力,而3-羟基邻氨基苯甲酸酯3,4-双加氧酶(HAAO)通过消耗3-HA阻断3-HA介导的细胞铁死亡逃避。此外,HAAO的表达水平与脂质过氧化和临床治疗效果呈正相关。总之,上述发现表明色氨酸代谢是促进肿瘤生长的一种新型抗铁死亡途径来,靶向该途径进行癌症治疗具有广阔的前景。

铁死亡是一种新发现的程序性细胞死亡模式,不同于细胞凋亡和n3-羟基邻氨基苯甲酸3,4-双加氧酶(HAAO)分泌过多,嗜铁细胞死亡的开始是由铁依赖性方式积累的过氧化磷脂诱导的。脂质氢过氧化物(PUFA-OOH)被谷胱甘肽过氧化物酶4 (GPX4)、铁死亡抑制蛋白1(FSP1)、四氢生物蝶呤(BH4)系统或新鉴定的二氢乳清酸脱氢酶(DHODH)转化为无毒的脂质醇(PUFA-OH)。最新研究表明,铁死亡与癌症免疫治疗和肿瘤抑制有关。在这四种已确定的抗铁死亡途径中,GPX4-GSH通路在抵抗癌细胞铁死亡方面占据主导地位。
半胱氨酸已被证明可以通过谷胱甘肽的生物合成来抑制铁死亡。谷胱甘肽是GPX4 减少氧化脂质的反应底物,半胱氨酸的来源则取决于细胞外摄取和从头生物合成。溶质载体家族7成员11(SLC7A11)是胱氨酸/谷氨酸逆向转运系统xc(slc7a 11/slc3a 2)的催化亚单位,是细胞外胱氨酸的主要质膜转运蛋白。继而细胞内胱氨酸迅速还原为半胱氨酸,用于随后的谷胱甘肽合成。GPX4利用GSH保护细胞免受膜脂质过氧化来消除脂质氢过氧化物。因此,通过胱氨酸饥饿或Erastin治疗阻断SLC7A11介导的胱氨酸摄取会使细胞对铁死亡敏感。
在胱氨酸稀少或缺乏的情况下,肿瘤细胞可以通过转氨途径将蛋氨酸转化为半胱氨酸来抵抗铁死亡。越来越多的研究表明,其他氨基酸(如谷氨酸和谷氨酰胺)通过半胱氨酸相关途径参与铁死亡。然而,很少有人知道氨基酸衍生的代谢物是否独立于半胱氨酸介导的铁死亡而影响肿瘤细胞的铁死亡敏感性。
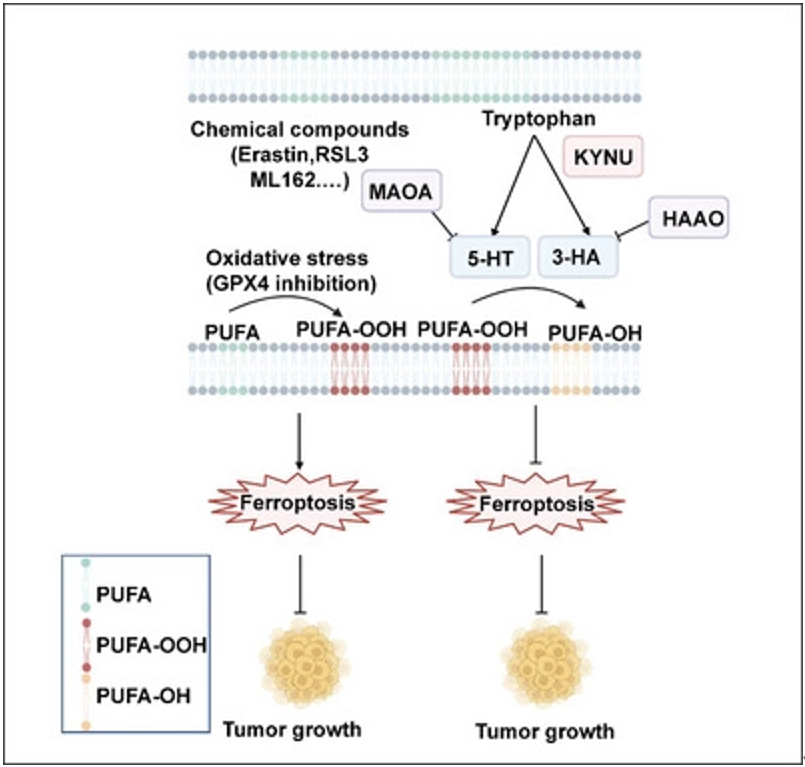
色氨酸代谢作为介导肿瘤生长的抗铁死亡途径示意图(摘自Advanced Science )
该研究验证了色氨酸代谢途径介导的抗铁死亡过程。研究表明,色氨酸代谢物5-HT和3-HA在相对较低的浓度下显著增强肿瘤细胞的抗铁死亡活性。从机制上讲,5-HT和3-HA都明显消除了作为有效自由基捕获抗氧化剂(RTA)的氧化磷脂。通过研究参与5-HT和3-HA代谢的酶,作者发现MAOA降解5-HT显著消除了5-HT的保护作用。 MAOA的缺失有效地改善了5-HT介导的铁死亡抑制。
KYNU通过产生3-HA赋予肿瘤细胞的抗铁死亡性能,而KYNU的缺乏显著增强细胞的铁死亡敏感性。相比之下,HAAO则显著消除了3-HA介导的铁死亡抑制。此外,HAAO的表达水平与脂质过氧化呈正相关,并改善了多种类型癌症患者的总生存期。总之,该研究表明色氨酸代谢是肿瘤细胞逃离铁死亡的新途径,靶向这一途径将有利于改善癌症治疗。
参考消息:
https://onlinelibrary.wiley.com/doi/10.1002/advs.202204006

