Nature:北京大学刘志博团队报道靶向共价放射性药物
时间:2024-05-24 10:02:49 热度:37.1℃ 作者:网络
靶向放射性核素治疗,即放射性药物将强效放射性核素输送到肿瘤进行局部照射,解决了未满足的临床需求,改善了癌症患者的预后。治疗性放射性药物必须实现可持续的肿瘤靶向和快速清除健康组织,这仍然是一个重大挑战。
2024年5月22日,北京大学刘志博团队(希洋、李詝及孔梓任为论文共同第一作者。)在Nature 在线发表题为“Covalent targeted radioligands potentiate radionuclide therapy”的研究论文,该研究发现共价靶向放射性配体能够增强放射性核素治疗。该研究在放射性药物上安装了一个基于硫(VI)氟交换(SuFEx)化学的连接器,以防止过快的肿瘤清除。当工程放射性药物与肿瘤特异性蛋白结合时,该系统经历了从结合到连接的转变,并通过“点击”SuFEx反应很容易与酪氨酸残基结合。将该策略应用于成纤维细胞活化蛋白(FAP)抑制剂(FAPI),可触发与该蛋白80%以上的共价结合,并且在6天内几乎没有解离。
在小鼠中,SuFEx工程的FAPI显示,与原始FAPI相比,肿瘤摄取增加了257%,肿瘤保留增加了13倍。在健康组织中的摄取被迅速清除。在一项初步影像学研究中,该策略比其他方法在癌症患者中识别出更多的肿瘤病变。SuFEx工程化FAPI也成功实现了靶向β-和α-放射性核素治疗,使小鼠肿瘤几乎完全消退。另一种SuFEx工程放射配体靶向前列腺特异性膜抗原(PSMA)也显示出增强的治疗效果。考虑到可以连接到SuFEx“弹头”的蛋白质的广泛范围,有可能将这种策略应用于其他癌症目标。

靶向放射性核素治疗(TRT)是治疗转移性癌症的一种范式转变的治疗方式,转移性癌症导致所有癌症中大多数死亡。TRT依赖于放射性配体,它以高亲和力结合癌症相关或特定靶标,并提供有效的β-颗粒或α-颗粒进行局部照射。作为临床癌症治疗的一种新方式,它具有固有的治疗特性,具有“交叉火力”效应(消除不一定靶向的癌细胞),并且不依赖于结合靶点的生物学途径。FDA批准的放射性配体已被常规用于治疗转移性癌症患者。值得注意的是,TRT的临床需求预计会增加,因为它在早期治疗和其他适应症中出现了临床益处。
治疗性放射性核素的成功需要出色的肿瘤靶向性,快速的血液清除和足够的肿瘤保留,因为大多数治疗性放射性核素的半衰期为3至10天。然而,平衡药物的血液清除率和肿瘤潴留往往是一个挑战。传统的放射性配体通常是一种双功能共轭物,将放射性核素标记模块与肿瘤靶向配体连接起来。由于大多数配体的可逆相互作用,传统放射性配体的肿瘤保留往往不足,这损害了TRT的疗效。
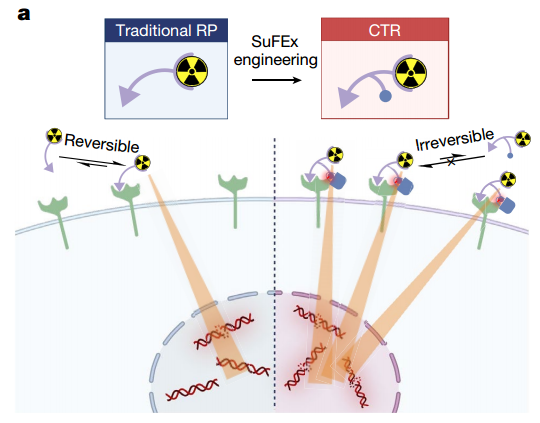
对于TRT而言,CTRs相对于传统放射性药物(RPs)的潜在益处示意图(图源自Nature )
该研究发现放射配体的肿瘤靶向性和药代动力学可以通过使用SuFEx工程连接体进行全面优化。研究表明,在荷瘤小鼠中,SuFEx工程的小分子偶联物,如FAPI-mFS,与原始FAPI相比,可以使肿瘤积累增加近13倍,其余的通过肾脏系统迅速排出。试点蛋白口袋筛选表明,活性残基广泛应用于许多临床重要靶标。这一强有力的策略将使研究人员和制药行业能够开发出具有小分子、多肽、适体或抗体片段的肿瘤靶向偶联物。
原文链接:
https://www.nature.com/articles/s41586-024-07461-6


