Nature Communications:emo了?竟是肠道菌群惹的祸!学会这一研究思路,离高分文章更进一步
时间:2024-05-26 06:01:47 热度:37.1℃ 作者:网络
肠道菌群是指定植在人体肠道内、长期与人体相互依存的微生物群,因其细胞数量是人体自身细胞的10倍,所编码的基因有100万个以上,被称为人体的“第二基因组〞。肠道菌群不仅会影响食物消化吸收为身体供能,还有着调节免疫功能参与机体代谢的作用,甚至能影响机体内分泌功能(调节能量、血糖、炎症反应等)。
近年来,越来越多的研究证实,诸多人类疾病的发生发展都与肠道菌群异常相关。已有大量研究证明,调节肠道菌群能够干预治疗各类疾病,如:糖尿病、肥胖症、高血压、自闭症等等。
在2023年批准的国自然项目中,有197个项目与肠道菌群有关,位居国自然热点前列,值得研究人员的长期关注。因此,小编整理了近期肠道菌群相关文章的研究思路,希望能给大家带来些许帮助。
近日,来自山西医科大学的研究员们在Nature出版集团旗下刊物《Nature Communications》发表了题为“Immunoregulatory role of the gut microbiota in inflammatory depression”的研究论文,确定了肠道菌群紊乱会干扰免疫系统和炎症因子,最终导致抑郁症的发生,以及脂肪酸代谢异常。不过,在进行粪便微生物群移植和益生菌补充后,肠道菌群逐渐正常化,并很大程度上减少了炎症因子,是炎症抑郁症有希望的治疗靶点。

一、研究背景
重度抑郁症(MDD)是一类常见的精神障碍,以情绪或心境低落为主要表现,患者伴有不同程度的认知和行为改变。由于高度异质性和多因素影响,MDD的预防和治疗仍然存在很大的挑战。有研究表明,炎症在MDD的中发挥着重要作用,抑郁症的发生与多个促炎因子的增加有关。因此,探索炎症及其致病机制对开发更有效的治疗方法至关重要。
肠道中紊乱的微生物群,可能是导致神经炎症的主要因素之一。肠道微生物群可以直接调节免疫系统——比如,生态失调期间表达的微生物相关分子模式(MAMP)可以被模式识别受体(PRR)、NLRP3炎症小体等识别,增加肠道通透性并破坏血脑屏障(BBB)。然后,激活中枢神经系统(CNS)中的小胶质细胞,促进促炎因子的分泌,从而改变大脑结构和功能,导致抑郁症。当然,也有研究发现,肠道微生物群可以产生一系列有益的代谢物(如短链脂肪酸(SCFA)),通过穿过血脑屏障、调节大脑功能,来调控肠粘膜和中枢神经系统的免疫和炎症反应,或可能影响抑郁症。肠道微生物群紊乱可能是低炎症的根源,但其免疫调控机制及在抑郁症中的具体作用仍不确定。
二、研究思路方法与结论
研究思路1:针对MDD受试者和健康对照(HC)受试者的体内研究
研究方法:
(1)检测MDD和HC的临床特征(如汉密尔顿抑郁量表(HAMD)、汉密尔顿焦虑量表(HAMA))、炎症因子(如hs-CRP、IL-1β、IL-6、IL-10、TNF-α等)和SCFA(如丙酸、丁酸、乙酸、异丁酸、戊酸和己酸等)水平。
(2)通过Alpha/Beta多样性分析和线性判别(LEfSe)分析,对比MDD和HC的肠道微生物群组成差异。
(3)通过相关性分析,对比肠道菌群、hs-CRP、SCFAs与抑郁症之间的关系。
(4)对肠粘膜样本进行多个炎症蛋白筛选,探索MDD和HC受试者的肠粘膜炎症因子和肠道通透性生物标志物。并通过酶联免疫吸附(ELISA)进一步量化,免疫组化进行验证。
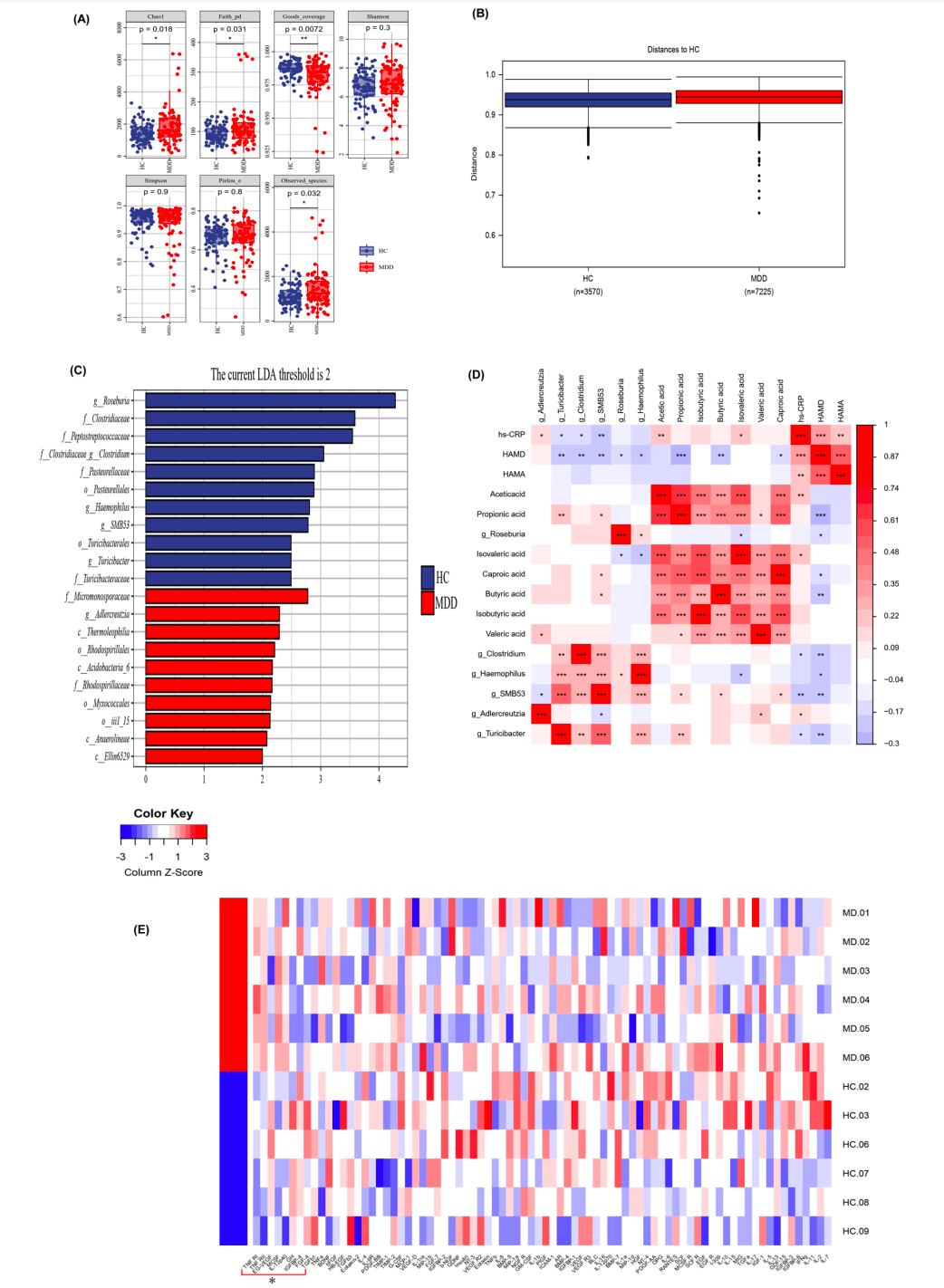
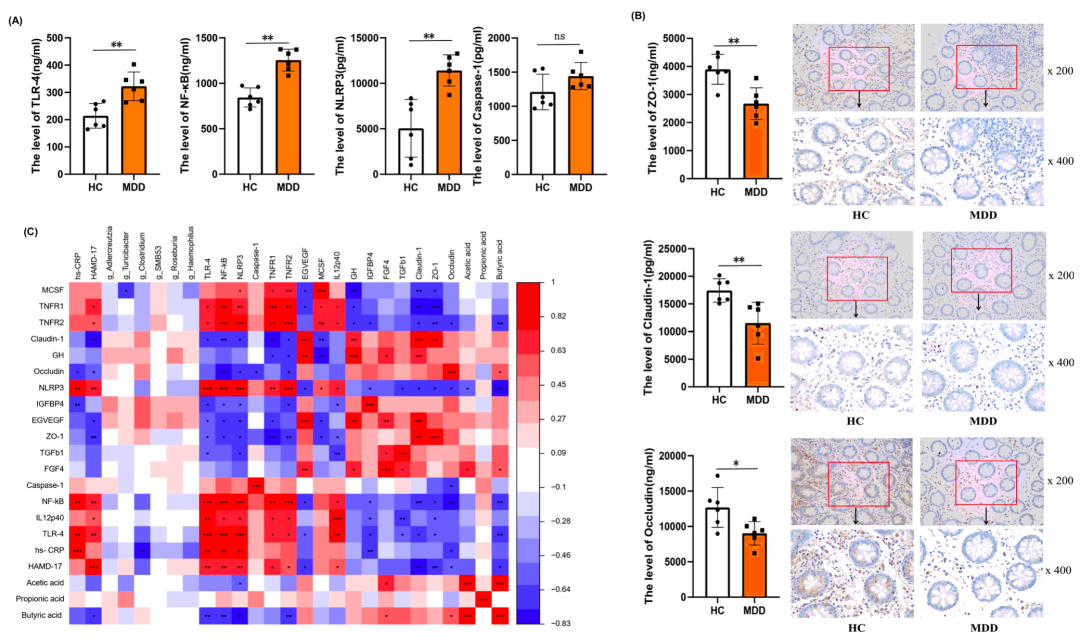
研究思路2:针对炎症性抑郁症、非炎症性抑郁症和HC受试者的体内研究
研究方法:
(1)根据血浆hs-CRP水平将MDD患者分为炎症性抑郁症组和非炎症性抑郁症组,通过LEfSe分析肠道微生物群在炎症抑郁症中的特征。确定属水平上三组(炎症性抑郁症、HC、非炎症性抑郁症患者)的生物标志物,构建受试者工作特征(ROC)曲线。
(2)通过鸟枪法宏基因组测序对炎症抑郁症患者和HC的粪便样本进行分析。结合不同物种ROC曲线创建炎症抑郁症诊断模型,并进行KEGG和KO对比分析两组的功能基因序列。
(3)对比两组肠黏膜的炎症因子和肠道通透性生物标志物水平。
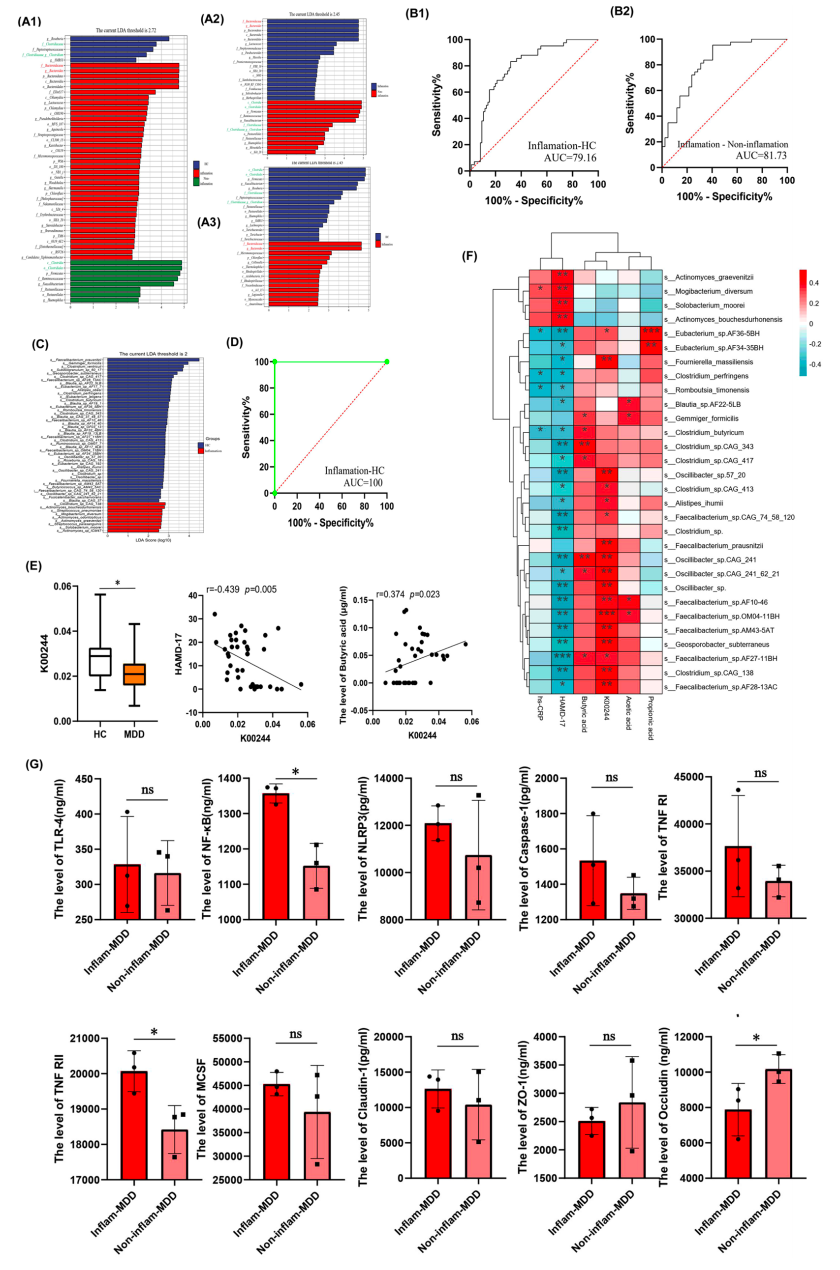
研究思路3:FMT建立小鼠炎症抑郁模型
研究方法:
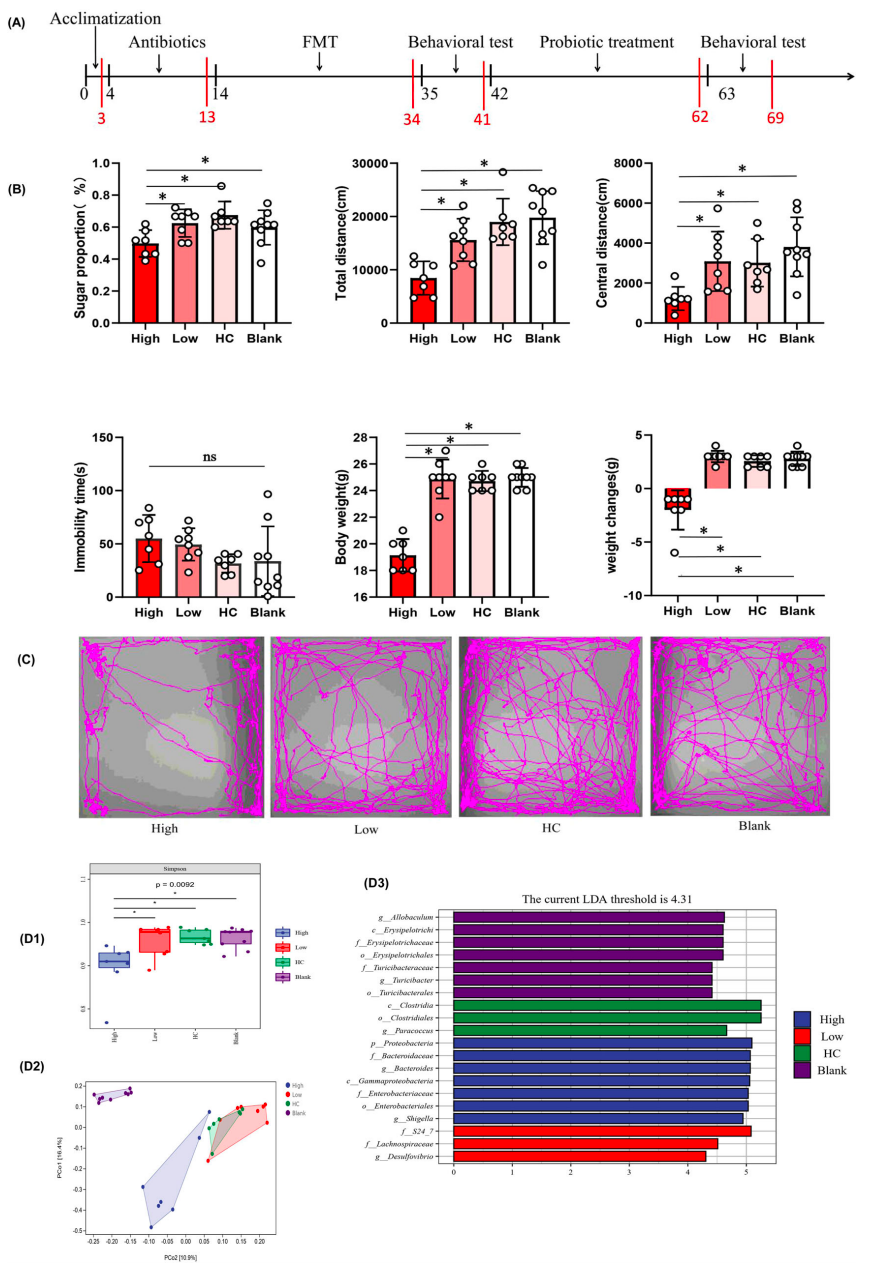
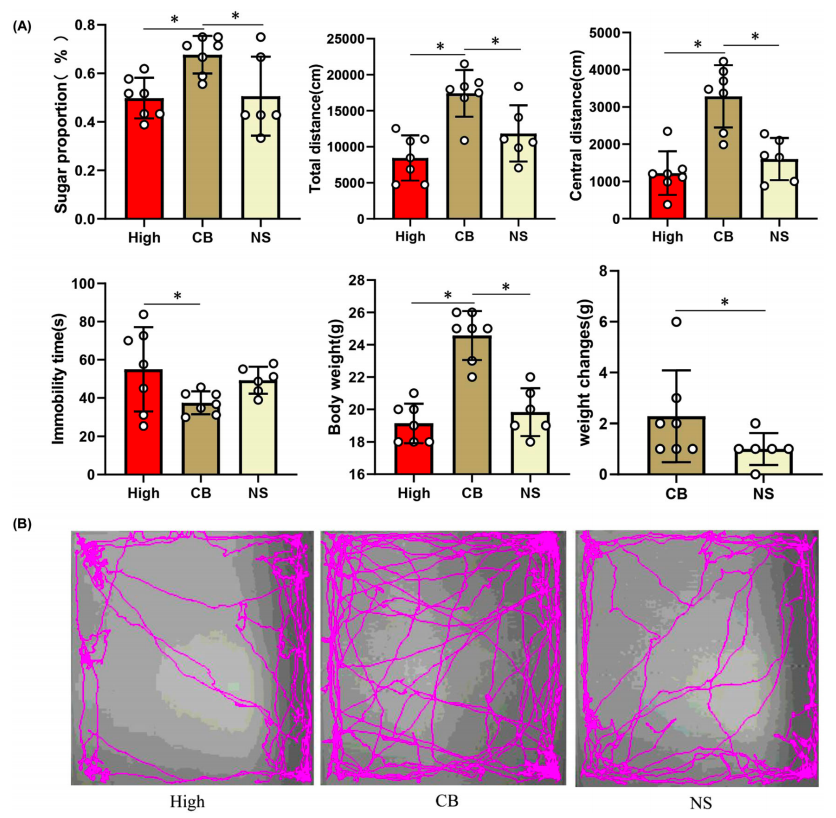
(1)通过FMT(肠道菌群移植)实验确定抑郁相关行为表型是否与肠道微生物群紊乱有关。通过蔗糖偏好测试(SPT)、旷场测试(OFT)、尾部悬吊试验(TST)等行为测试以及期间小鼠的总液体摄入量,分析移植了炎症性抑郁症患者微生物群的小鼠其体重、活动、焦虑和抑郁样行为变化。
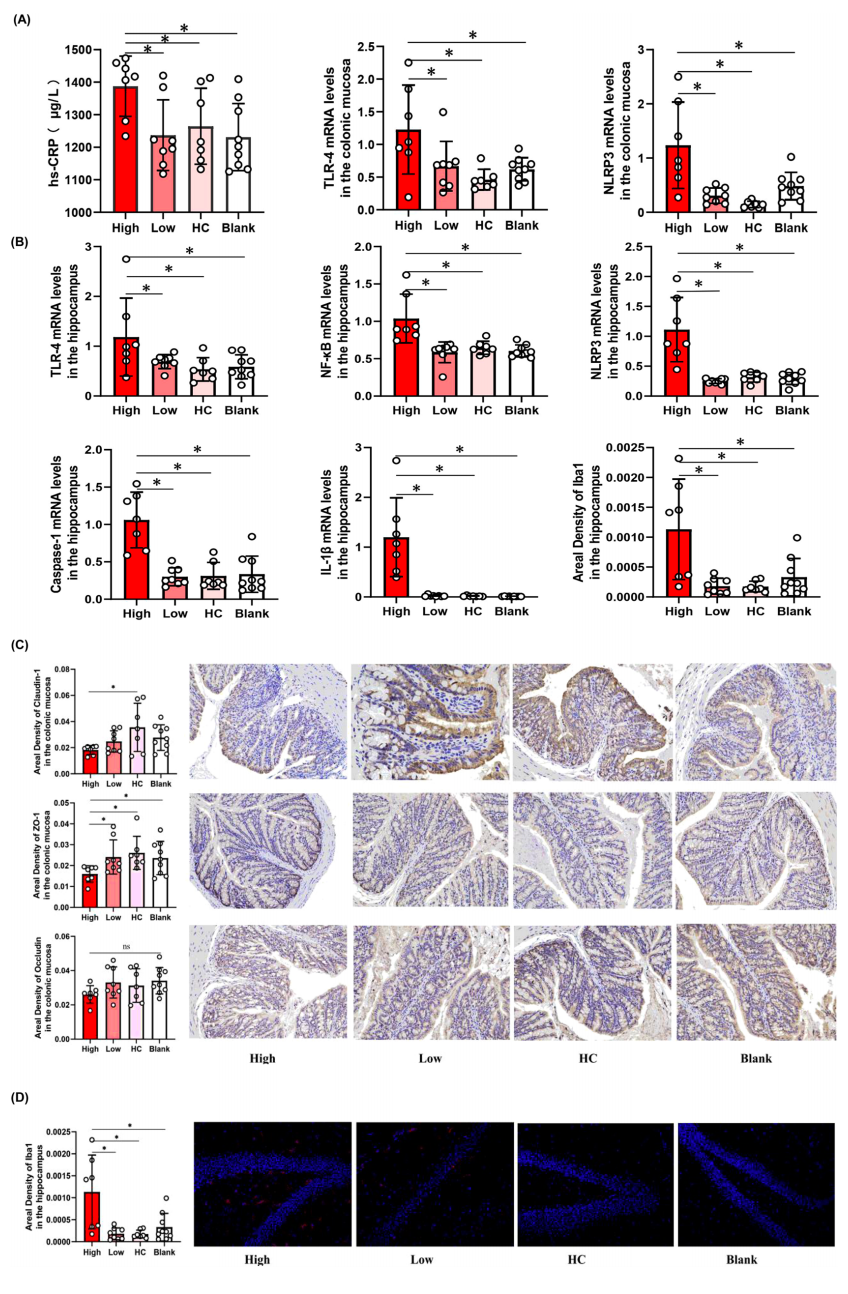
(2)对肠道微生物组成进行表征,通过Alpha/Beta多样性分析、LEfSe分析,对比四组(高炎症、低炎症组、HC组和空白组)微生物群差异。
(3)通过qPCR和免疫组化探究四组肠道微生物群在炎症中的影响,检测多个炎症因子水平,分析肠粘膜的通透性。免疫荧光评估海马小胶质细胞的数量和形态。
(4)进行相关性分析,确定肠道微生物群、炎症标志物、通透性标志物和抑郁样行为之间的相关性。
研究思路4:益生菌丁酸梭菌(CB)对小鼠炎症抑郁模型的影响
研究方法:
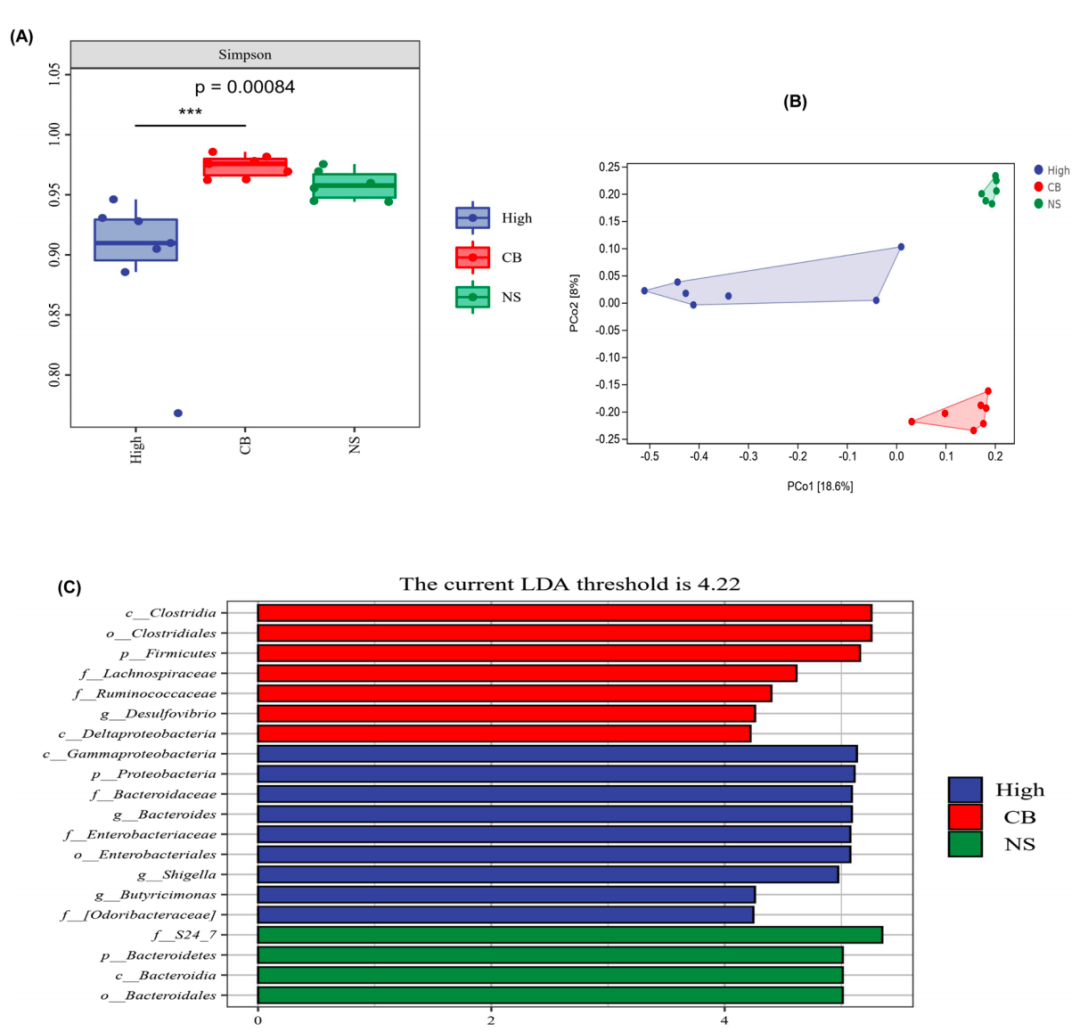
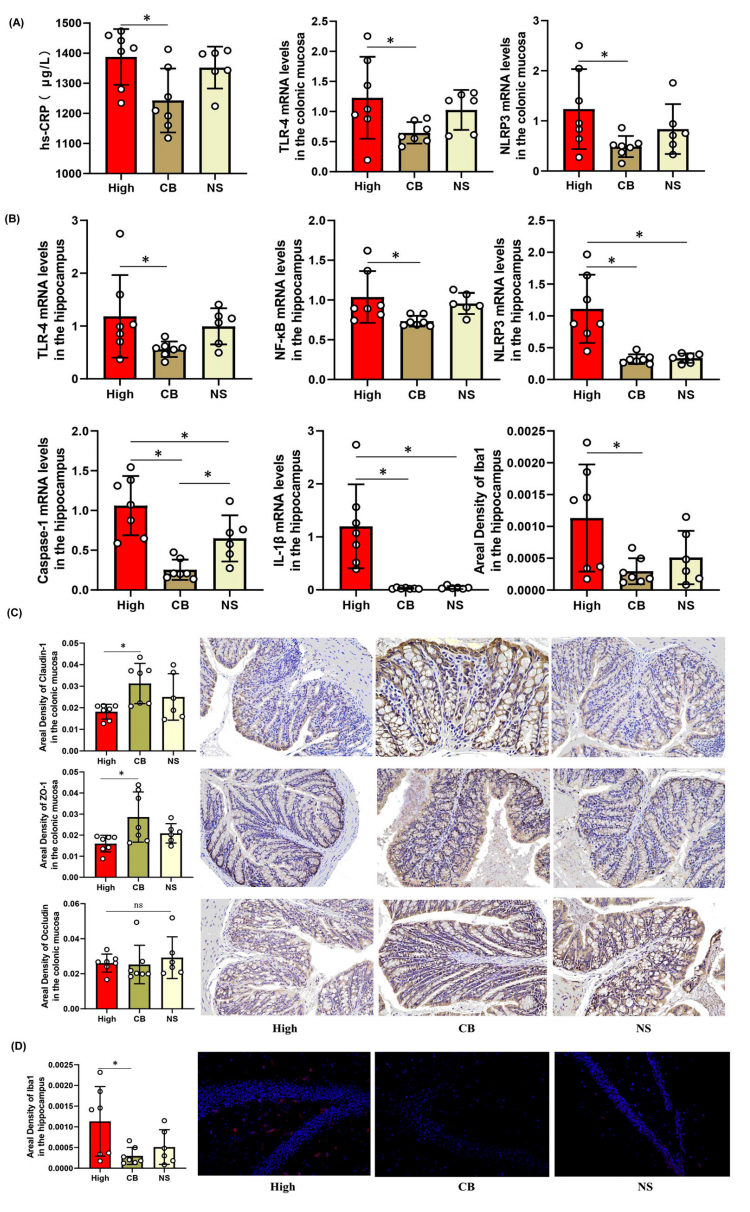
(1)给高炎症小鼠补充产生丁酸的抗炎细菌(CB),并进行α多样性分析和LEfSe分析,探究高炎症小鼠肠道微生物群与抑郁症状之间的关系。
(2)检测肠黏膜、血清中、大脑中炎症因子表达量以及海马小胶质细胞数量和分支变化。
(3)利用行为测试评估CB组抑郁样行为。
三、小结
本研究首先分析了炎症性抑郁症患者粪便中的肠道微生物群组成、血浆和肠粘膜中的炎症因子、短链脂肪酸(SCFA)、肠道通透性标志物水平等。炎症性抑郁症患者的肠道微生物群表现出较高的拟杆菌和较低的梭状芽胞杆菌水平,并且SCFA(丁酸)代谢异常。
在进行粪便微生物群移植(FMT)和益生菌补充后,发现炎症抑郁组的肠道菌群其外周、中枢炎症因子以及肠粘膜通透性增加。丁酸梭菌补给后,可以使肠道微生物群正常化,减少炎症因子,并在炎症性抑郁症小鼠模型中显示出抗抑郁样表型。上述研究表明,源自肠道微生物群的炎症过程可能参与神经炎症,肠道微生物群是炎症抑郁症有希望的治疗靶点,并为未来研究提供了科学依据。
参考来源:
Liu P, et al. Immunoregulatory role of the gut microbiota in inflammatory depression. Nat Commun. 2024 Apr 8;15(1):3003. doi: 10.1038/s41467-024-47273-w.


