赵维莅/王黎教授团队证实18F-FDG PET/CT在CAR-T治疗LBCL中的预后价值
时间:2024-09-19 11:01:13 热度:37.1℃ 作者:网络
CAR-T
CAR-T细胞疗法极大地改善了大 B 细胞淋巴瘤 (LBCL) 复发难治患者的预后,但仍有部分患者未获得缓解或在缓解后复发,早期识别和干预可能对 CAR-T 细胞治疗反应不佳的患者,将有助于提高疗效。
有研究表明,单采前和输注前总代谢肿瘤体积(tMTV)可预测生存,单采前或输注前tMTV值越高,则无进展生存期(PFS)和总生存期(OS)越短。此外输注前tMTV与≥2级细胞因子释放综合征(CRS)相关,最大标准化摄取值(SUVmax)与未达到CR相关。基于输注前tMTV联合乳酸脱氢酶(LDH)的预测模型可预测CAR-T细胞治疗后的预后。
上海交通大学医学院附属瑞金医院赵维莅/王黎教授团队开展回顾性研究,探索了筛选期18F-FDG PET/CT的预后价值,结果近日发表于《Biomarker Research》。

研究结果
作者分析了该中心90例接受 CAR-T 细胞治疗并在筛选阶段(中位至输注时间53.5天)、CAR-T细胞输注后1个月和3个月接受 18F-FDG PET/CT扫描的患者,此外在筛选期对47例患者进行了RNA 测序。
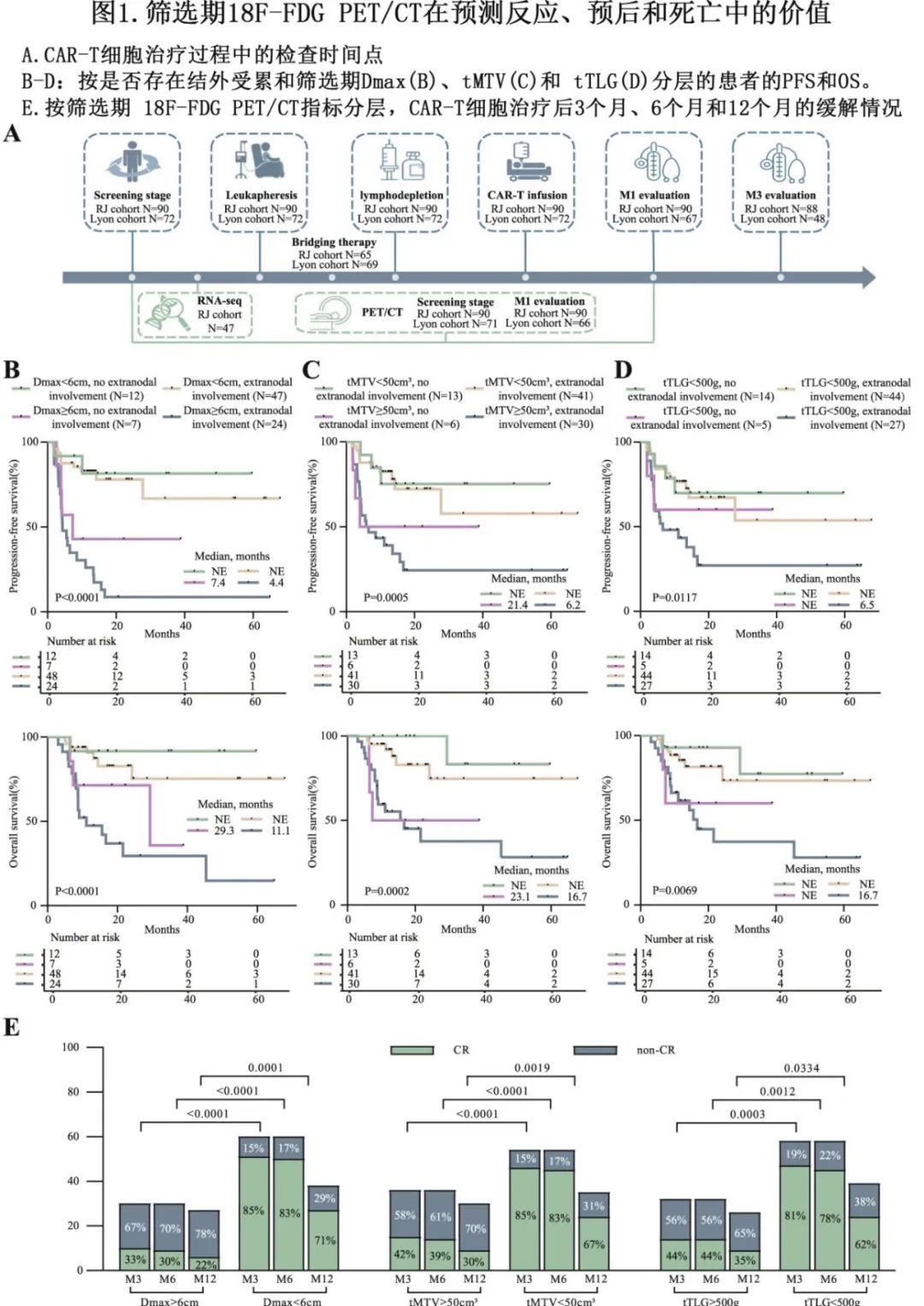
筛选期最大病灶最大直径 (Dmax) <6cm的患者 (N=60) 的3个月完全缓解(CR)率 (85.0% vs. 33.3%,P<0.001)、无进展生存期 (HR=0.17;P<0.001) 和总生存期(HR=0.18,P<0.001)显著优于Dmax≥6cm的患者 (N=30)。同样,tMTV< 50cm3和总病灶糖酵解 (tTLG) <500g的患者具有更高的3个月CR率、PFS和OS。此外,在筛选期,Dmax联合结外受累在区分患者结局方面优于tMTV或tTLG联合结外受累(下图B-D)。筛选期tMTV和tTLG的最佳cut-off值分别为 50cm3和500g。
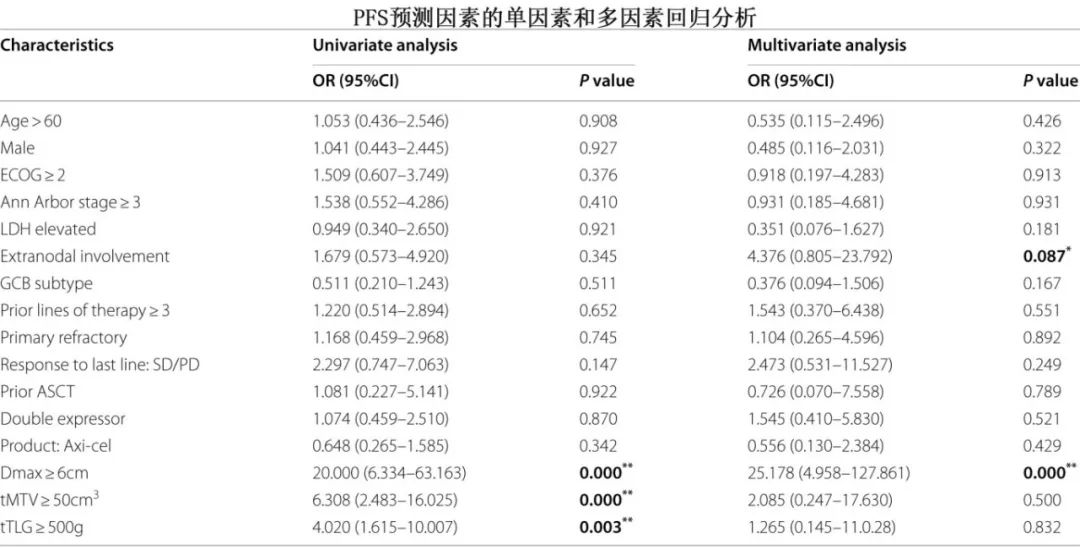
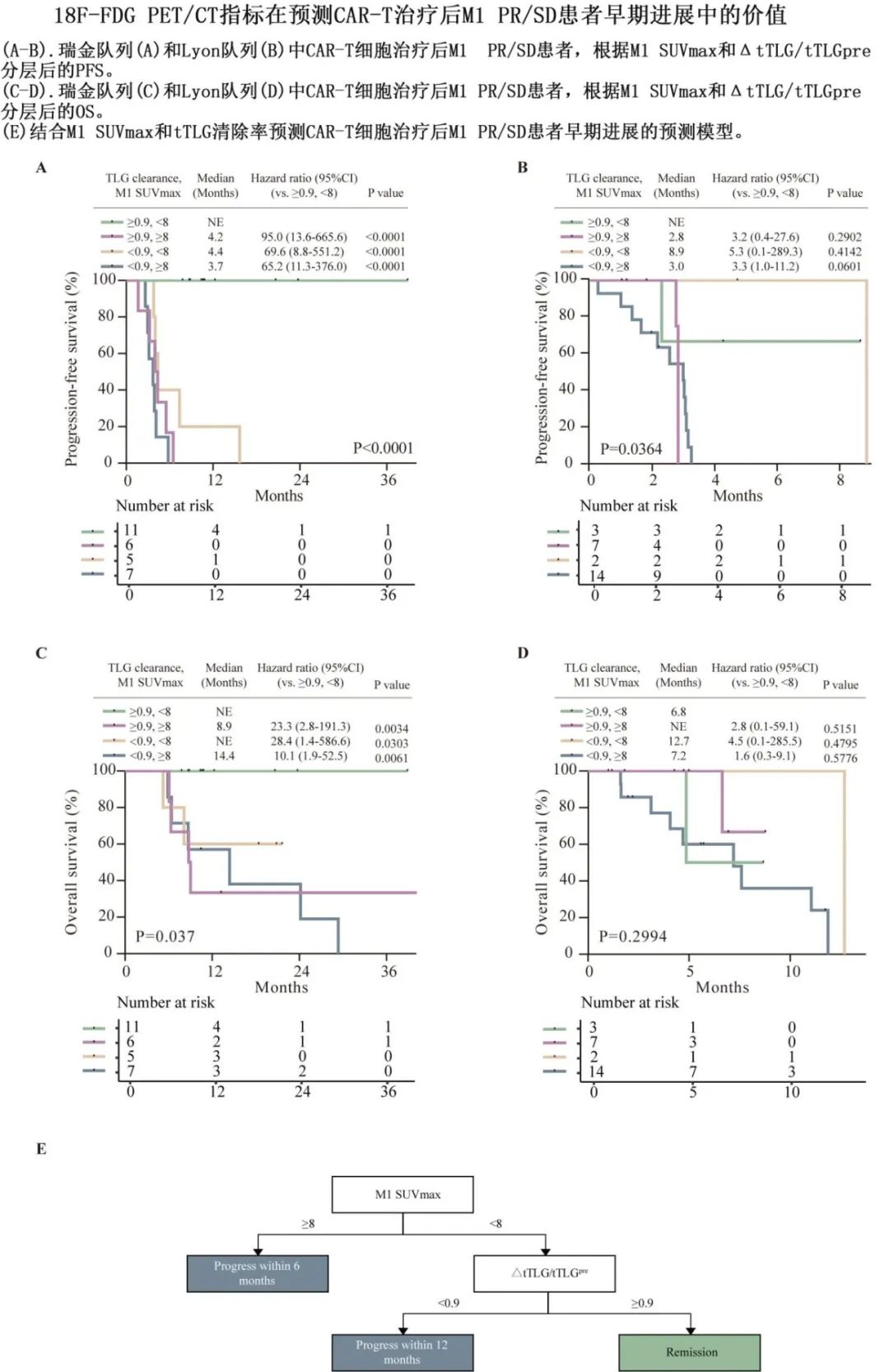
识别即将发生早期进展的患者对于实施抢先治疗策略至关重要,因此作者利用 CAR-T 治疗后1个月部分缓解 (PR)/疾病稳定 (SD) 患者的放射组学数据建立了早期进展的预测模型。作者结合 CAR-T 细胞治疗后1个月 (M1) 最大标准摄取值 (SUVmax) 和 tTLG 清除率建立了预测模型(ΔtTLG/ tTLGpre= [筛选期tTLG]-[M1时tTLG])/筛选期tTLG),可预测 CAR-T 细胞治疗后 M1 时评价的部分缓解/疾病稳定患者的早期进展风险。M1 SUVmax<8和ΔtTLG/tTLGpre≥0.9(N=11,未达到中位PFS)可预测持续缓解状态,而SUVmax≥8表明6个月内疾病进展,无论 tTLG 清除率如何(tTLG清除率≥0.9,N=6,中位PFS 4.2个月,HR=95.0;tTLG清除率<0.9,N=7,中位PFS 3.7个月,HR=65.2),而M1 SUVmax<8和 tTLG 清除率<0.9(N=5,中位PFS 4.4个月,HR=69.6)表明12个月进展。此外模型也在 Lyon 队列中进行验证。
在接受 axicabtagene ciloleucel 治疗的患者中发现,CAR-T细胞治疗后,两个最远病灶之间的距离(按体表面积标准化)与神经毒性严重程度相关 (AUC=0.74;P=0.034);最远病灶距离<0.15m-1的患者无神经毒性发生,而最远病灶距离≥0.15m-1的患者有34.8%出现神经毒性。但relmacabtagene autoleucel(relma-cel)患者未观察到强相关性。不同 CAR-T 细胞的 CRS 和神经毒性发生率不同,可能是由于 CAR-T 细胞共刺激分子的差异,也可能是由于样本量较小。
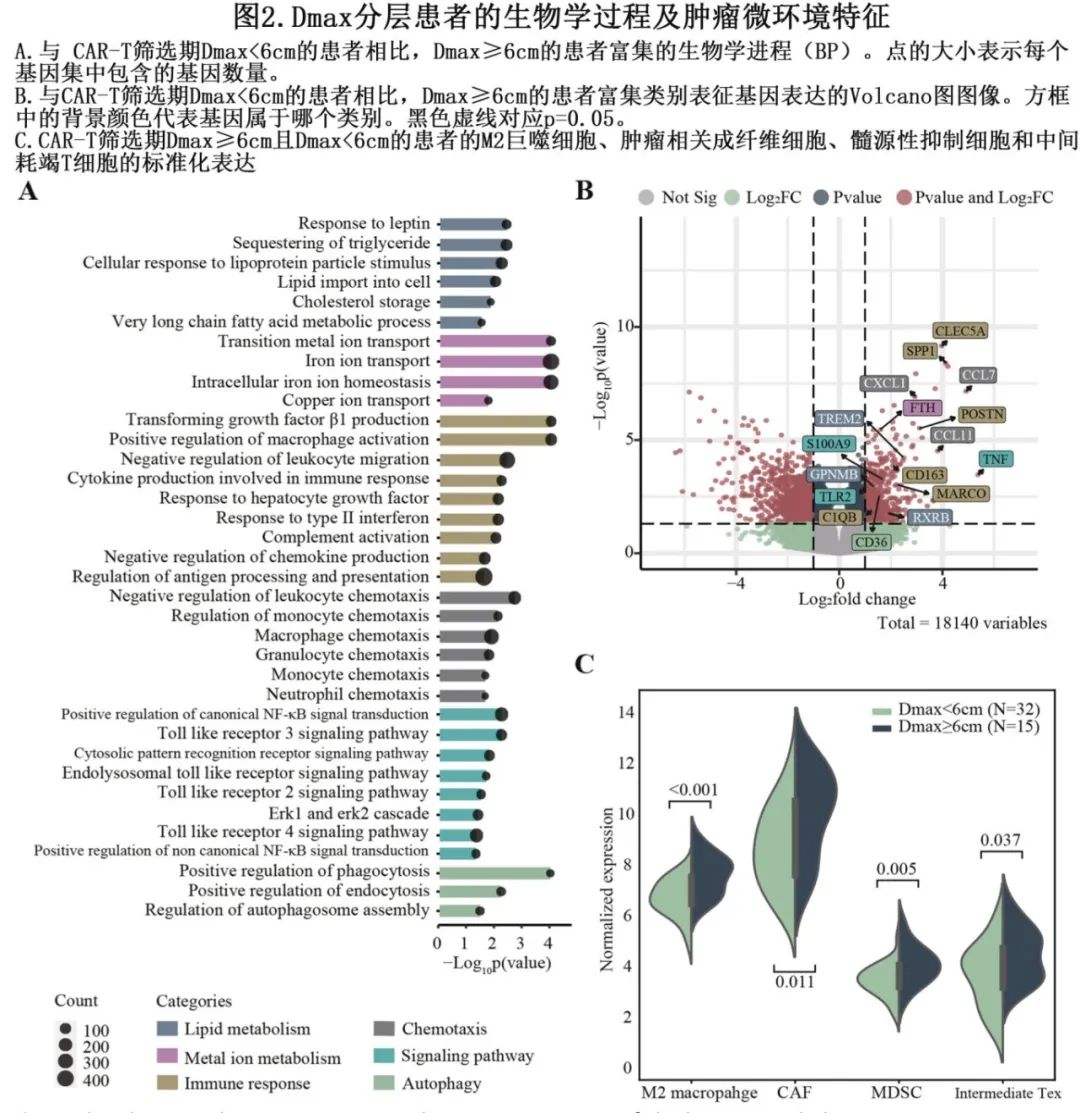
RNA测序数据的基因集富集分析 (GSEA) 显示,Dmax≥6cm的患者富集免疫抑制剂相关的生物学过程。肿瘤微环境 (TME) 分析发现,这些患者的 M2 巨噬细胞、肿瘤相关成纤维细胞 (CAF)、髓源性抑制细胞 (MDSC) 和中间耗竭 T 细胞水平较高,提示免疫抑制性微环境是高肿瘤负荷患者 CAR-T 细胞治疗失败的可能原因。伴随 TME 内免疫抑制细胞的增加,脂质代谢、铁/铜离子转运、巨噬细胞、粒细胞、单核细胞趋化和自噬途径被显著激活 (Dmax≥6 cm)。在高肿瘤负荷下,肿瘤细胞倾向于通过代谢改变和随后诱导的 T 细胞耗竭募集并激活更多的免疫抑制细胞。
总结
18F-FDG PET/CT 的影像学指标,尤其是筛选期 Dmax 具有预测 CAR-T 治疗的临床疗效、进展和死亡的价值,而最远病灶的距离与神经毒性的发生相关。此外作者建立了一个预测模型,结合 M1 SUVmax 和 tTLG 清除率来预测 CAR-T 治疗后 M1 PR/SD 患者的早期进展。对于对 CAR-T 细胞治疗反应不佳的高肿瘤负荷患者,免疫抑制性肿瘤微环境是可能的机制及不良预后指标。
参考文献
Sheng, LS., Shen, R., Yan, ZX. et al. 18F-FDG PET/CT metrics-based stratification of large B-cell lymphoma receiving CAR-T cell therapy: immunosuppressive tumor microenvironment as a negative prognostic indicator in patients with high tumor burden. Biomark Res 12, 104 (2024). https://doi.org/10.1186/s40364-024-00650-5

