Lupus Science & Medicine:COVID-19刺突蛋白对系统性红斑狼疮的发病和进展的影响
时间:2024-10-11 16:00:41 热度:37.1℃ 作者:网络
系统性红斑狼疮(SLE)是一种复杂的自身免疫性疾病,主要特征包括多器官炎症、自身抗体生成及血栓形成。近年来,COVID-19感染被发现能诱发多种自身免疫疾病,包括SLE,然而其具体影响机制尚不明确。已有研究表明,COVID-19通过其刺突蛋白激活免疫系统,导致炎症反应加剧,但其对SLE的具体作用尚需进一步探讨。本研究旨在通过三个不同的SLE小鼠模型,评估COVID-19刺突蛋白对SLE的发病和进展的影响,重点观察其在自身抗体生成、组织纤维化及血栓形成方面的作用,以揭示COVID-19对SLE患者潜在的病理影响机制,并为未来的治疗和预防策略提供科学依据。

本研究为随机、双盲、安慰剂对照试验,使用三种不同的SLE小鼠模型评估COVID-19刺突蛋白的影响。实验动物包括R848诱导的BALB/C型狼疮小鼠、R848诱导的IL-1受体拮抗剂敲除(KO)小鼠及MRL/lpr自发性狼疮小鼠。各组小鼠分别接受编码SARS-CoV-2刺突蛋白及ACE2受体的质粒注射,作为COVID-19感染模拟组;对照组则注射空载体质粒或车辆溶剂。注射方式为静脉注射,持续6周。实验期间,定期采集血清样本,检测白蛋白和自身抗体水平,通过流式细胞术分析淋巴细胞表型,并进行组织病理学分析评估器官损伤及纤维化程度。
结果显示,在R848诱导的BALB/C型狼疮小鼠中,注射刺突蛋白后,抗双链DNA抗体(总IgG:0.499 mg/mL vs. mock组0.389 mg/mL,p<0.05)、IgG1(0.153 mg/mL vs. mock组0.093 mg/mL,p<0.05)和IgG2a(0.267 OD vs. mock组0.223 OD,p<0.05)水平显著升高。白蛋白水平也显著增加(148.813 μg/mL vs. mock组76.226 μg/mL,p<0.05)。此外,刺突蛋白组小鼠脾脏增大程度显著高于对照组(p<0.05),T辅助1细胞数量增加(p<0.05),组织学分析显示肾脏和肺部组织的损伤及纤维化程度显著加重,α-平滑肌肌动蛋白表达水平显著升高(p<0.05)。
在MRL/lpr自发性狼疮小鼠模型中,刺突蛋白组的总IgG(22.892 mg/mL vs. mock组18.471 mg/mL,p<0.05)、IgG2a(26.659 mg/mL vs. mock组18.828 mg/mL,p<0.05)和抗双链DNA IgG2a(0.502 OD vs. mock组0.057 OD,p<0.05)水平显著升高。刺突蛋白组的小鼠肾脏和肺部损伤及纤维化程度显著加重,尿白蛋白和血清CXCL4/PF4水平显著增加(白蛋白:18.26 μg/mL vs. mock组7.454 μg/mL,p<0.05;CXCL4/PF4:273.72 pg/mL vs. mock组188.7 pg/mL,p<0.05)。
在R848诱导的IL-1Ra KO小鼠模型中,刺突蛋白组表现出脾脏增大、严重的肾损伤及显著的肺纤维化(p<0.05)。这些结果表明,COVID-19刺突蛋白显著加剧了SLE的发病和进展,表现为自身抗体水平的升高、组织纤维化及血栓形成的加剧。
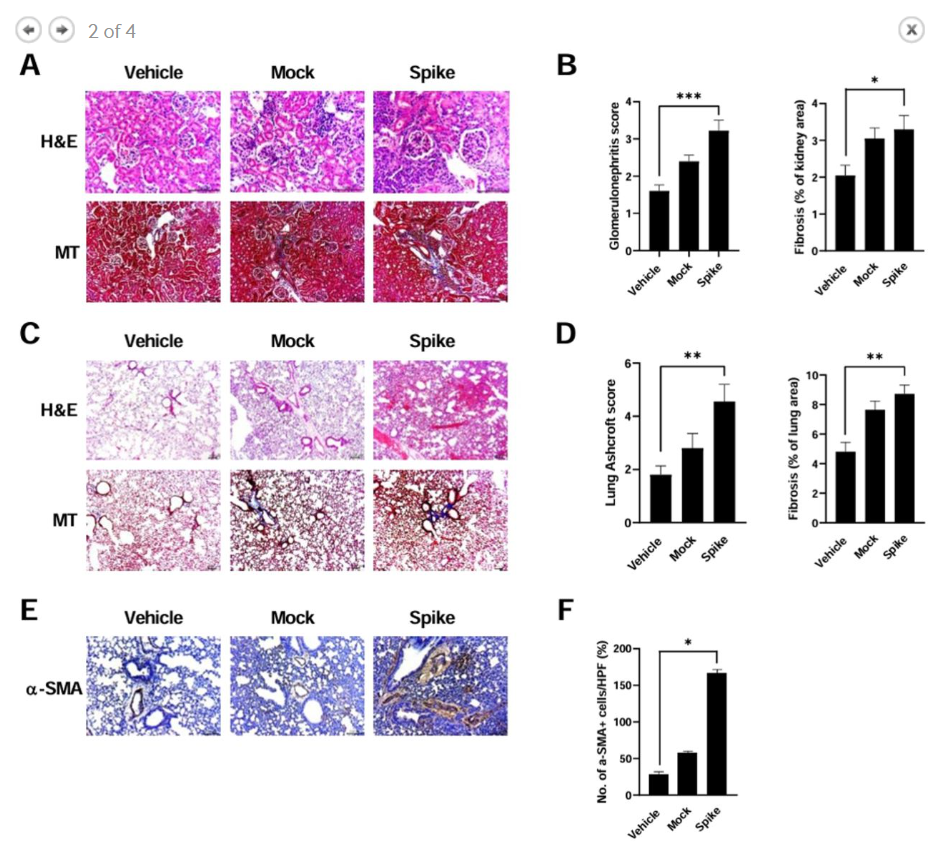
COVID-19刺突蛋白加速狼疮性肾炎和组织纤维化
本研究通过三个不同的SLE小鼠模型,系统评估了COVID-19刺突蛋白对SLE发病和进展的影响。结果显示,刺突蛋白显著促进了自身抗体的生成,加剧了肾脏和肺部的组织损伤及纤维化,且在MRL/lpr小鼠中还增加了血栓标志物CXCL4/PF4的水平。这些发现表明COVID-19感染可能通过其刺突蛋白加速SLE的发展和恶化,导致炎症反应和组织损伤的加重。研究结果为理解COVID-19在自身免疫疾病,特别是SLE中的作用机制提供了重要的动物实验依据,同时为未来制定预防和治疗策略提供了科学依据。然而,研究也存在一些局限性,如动物模型无法完全模拟人类SLE的复杂病理特征,且仅观察了刺突蛋白的短期影响,未来需开展更多研究以验证其长期作用及临床相关性。
原始出处:
SARS-CoV-2 spike aggravates lupus nephritis and lung fibrosis in systemic lupus erythematosus,
